Hallo! Meine Benutzer-Seite ist eine Art Steinbruch, in der hauptsächlich für mich wichtige Vorlagen liegen und einige Tests laufen...
[[1]]
Arbeitsauftrag Biologie7 (verpflichtend)
- Die folgende verpflichtende Unterrichtseinheit hat eine Bearbeitungszeit von ca. 30 Minuten.
- Ihr benötigt für die Bearbeitung: Das Schulbuch, einen Zettel, Stift und Ruhe.
- Bitte bearbeitet die gestellten Aufgaben tatsächlich erst selbst, bevor ihr auf "Lösung" klickt!
Ziel
Langfristig möchte ich mit euch den Begriff "ökologische Nische" klären. In dieser Einheit wird das aber noch nicht geschehen. Um diesen Begriff zu verdeutlichen, werde ich bestimmten Grafiken arbeiten. Grafiken, die etwas komplizierter sind, als ihr gewohnt seid.
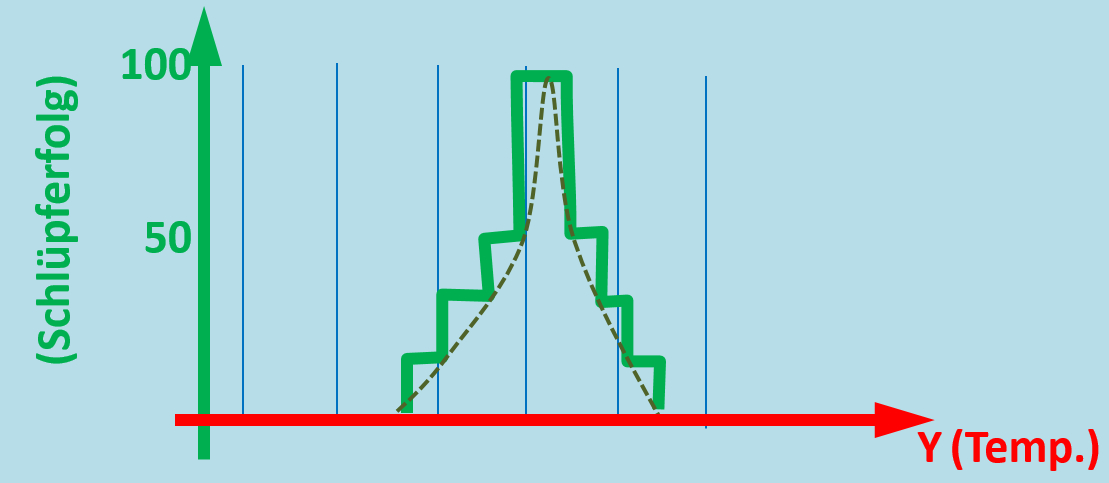
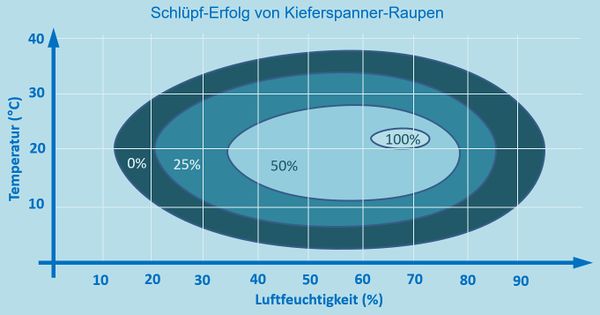
Eine Grafik, die so ähnlich auch in eurem Buch auf der S. 71 enthalten ist, seht ihr hier:
Wiederholung
Normalerweise beginnt ihr beim Interpretieren einer Grafik zunächst mit einer bestimmten Floskel: "Die Grafik zeigt... in Abhängigkeit von...". Das funktioniert bei der oberen Grafik nicht! Zur Wiederholung noch einmal anhand einer einfacheren Grafik. Wendet die Floskel an:
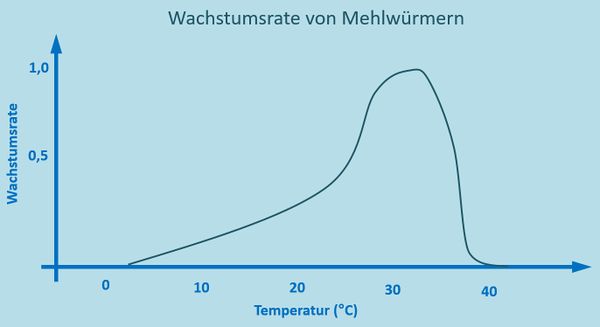
- Die Grafik zeigt die Wachstumsrate von Mehlwürmern in Abhängigkeit von der Temperatur.
- Man erkennt eine typische Optimuskurve mit einer optimalen Wachstumsrate bei ca. 30%...
- usw...
Zerlegung der Grafik in Komponenten
Die Floskel kann auf die eingangs gezeigte Grafik nicht angewendet werden, weil hier DREI Parameter dargestellt sind, während die Grafik von den Mehlwürmern nur ZWEI Parameter enthält.
- Mehlwurmkurve: Temperatur, Wachstumsrate
- Kiefernspinner: Temperatur, Luftfeuchtigkeit, Schlüpferfolg
Normalerweise braucht man für jeden Parameter eine eigene Achse. Im Bild vom Kiefernspinner ist die dritte Achse einfach weggelassen, bzw. kommt sie auf euch zu! Das folgende Bild zeigt, wie man sich die Grafik dreidimensional auch vorstellen könnte:
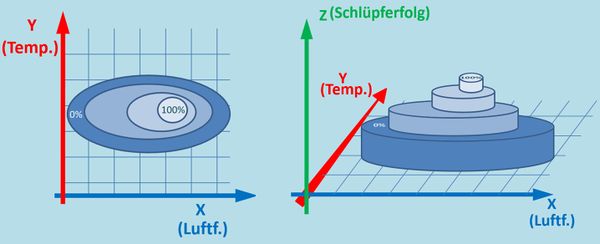
Vielleicht kennt ihr solche Darstellungen aus eurem Atlas: Auch da werden Berge mit "Höhenlinien" dargestellt. Man kann aus der aufgeschlagenen Seite eines Atlas ja kein Gebirge herauswachsen lassen.
Mit dieser Darstellung solltet ihr jetzt auch etwas besser die Floskel anwenden können: Das was in einer zweidimensionalen Grafik die y-Achse ist, ist hier die z-Achse. Und das was in einer zweidimensionalen Grafik die x-Achse ist, ist hier die x- und die y-Achse. Versucht es jetzt mit der Floskel!
Die Grafik zeigt den Schlüpferfolg von Kieferspannern in Abhängigkeit von der Temperatur und der Luftfeuchtigkeit.
Wenn ihr das hinbekommen habt: TOLL! :)
Man kann aus dieser dreidimensionalen Darstellung auch wieder zweidimensionale Grafiken machen, indem man einen Paramater einfach konstant lässt. Zum Beispiel: Man kann den Schlüpferfolg von Kieferspannern in Abhängigkeit von der Luftfeuchtigkeit in eine Grafik zeichnen. Die Temperatur soll in allen Fällen immer gleich bei 20°C bleiben. Versucht diese Grafik zu zeichnen. Dazu ist in der folgenden dreidimensionalen Abbildung eine Hilfslinie hervorgehoben (die rote 20°C-Linie):
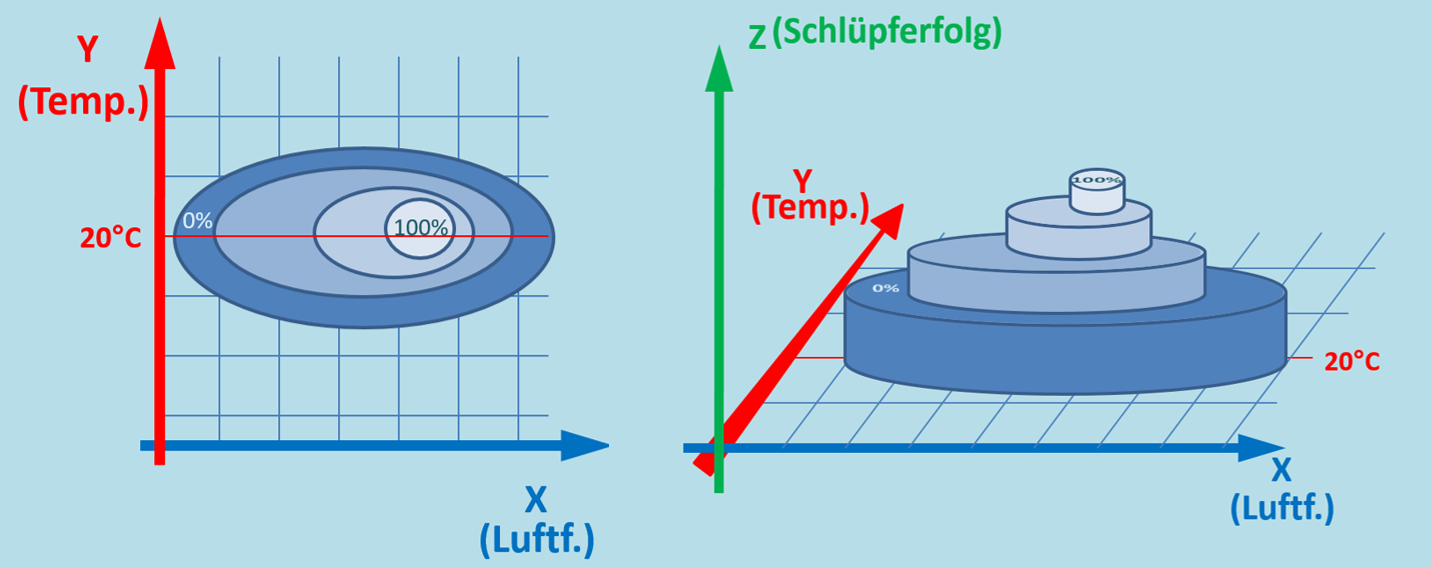
- Zeichnet zunächst ein Achsensystem (y-Achse: Schlüpferfolg, x-Achse: Luftfeuchtigkeit)
- Fahrt dann mit eurem Finger die rote Linie auf dem Diagramm hier am Bildschirm entlang und übertragt die Werte, bei denen sich euer Finger gerade befindet in die passende Stelle eures gezeichneten Koordinatenkreuzes.
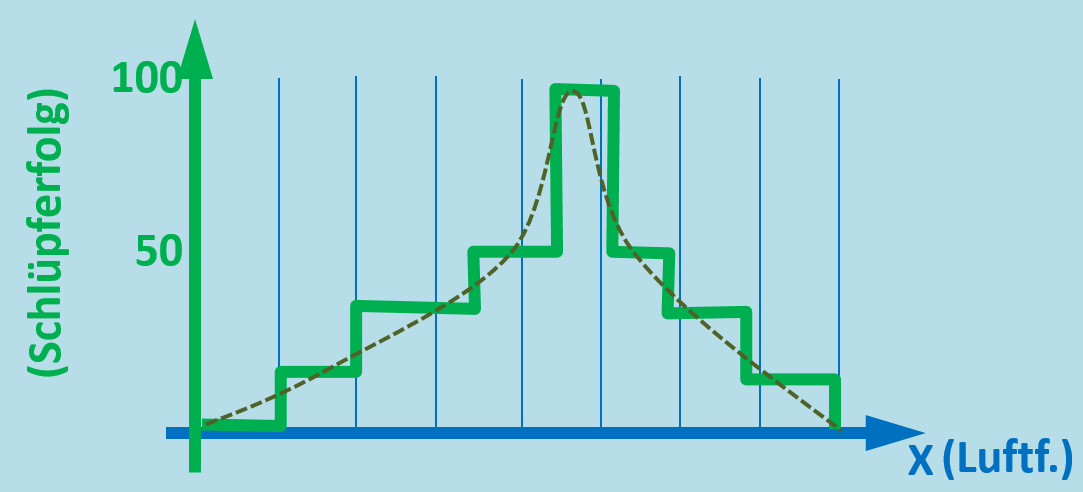
Die geschrichelte Linie ist eine "geglättete" Linie. Die ist etwas realistischer
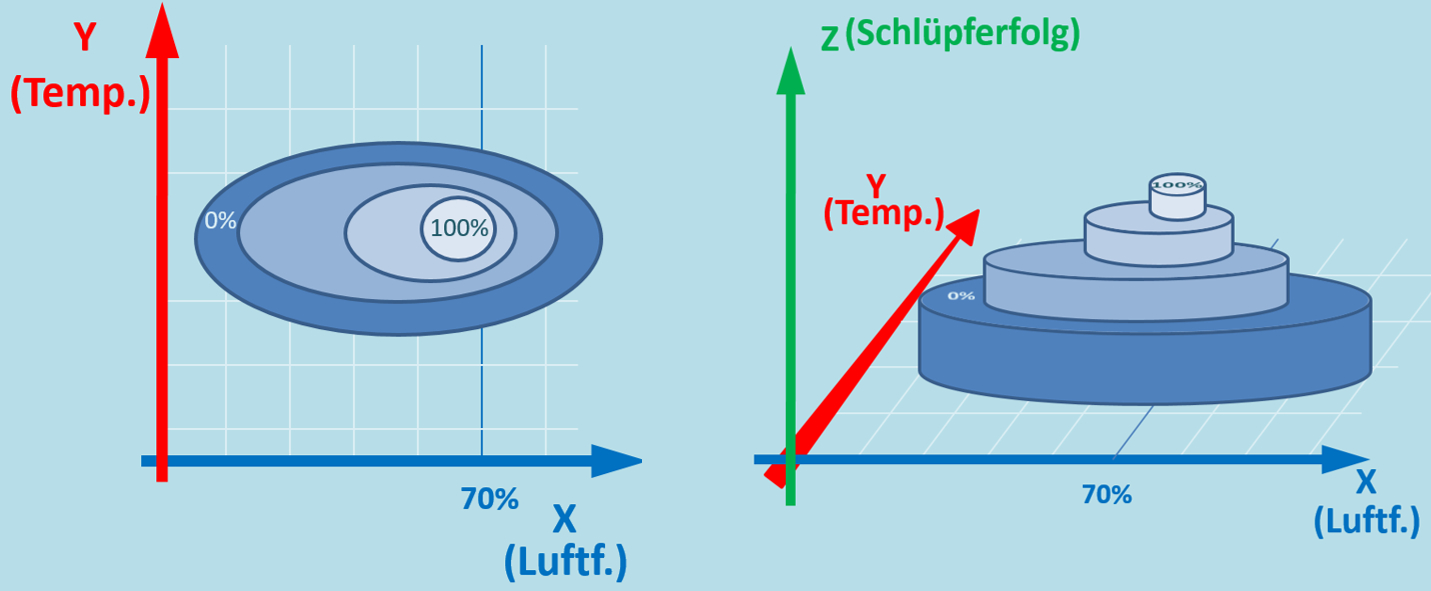
Das Ganze geht natürlich auch mit dem anderen Parameter: Leitet aus dem dreidimenionalen Diagramm ein zweidimensionales Diagramm ab, das den Schlüpferfolg in Abhängigkeit von der Temperatur zeigt. Bei einer gleichbleibenden Luftfeuchtigkeit von 70%. Diesmal ohne Text-Hilfen, nur das entsprechende Diagramm:
Hausaufgabe
Nach den neuen "Home-Schooling-Regeln" sollen wir Lehrer euch ein ausführlicheres Feedback geben. Daher möchte ich gerne, dass ihr mir die Lösung zu der folgenden Hausaufgabe schriftlich schickt. Das ganze wird über den Schulmanager laufen, ich kontaktiere euch im Laufe des Tages über den Schulmanager.
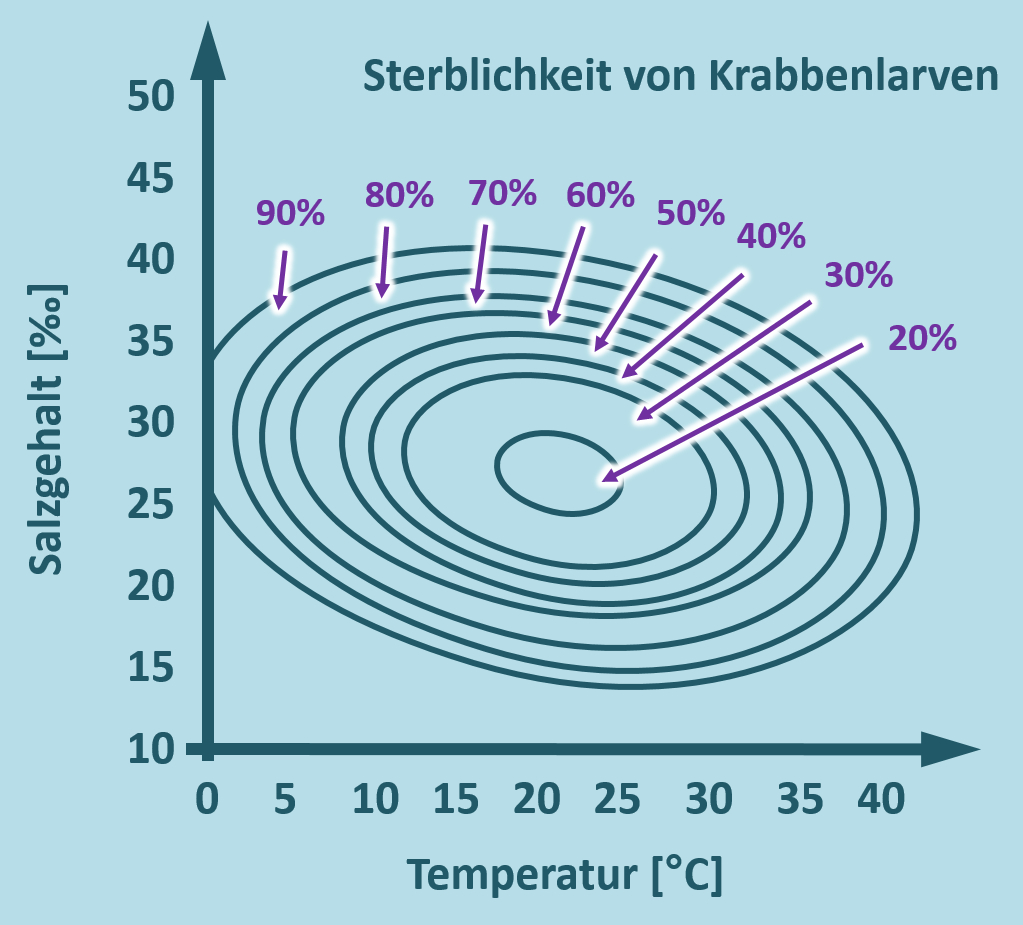
- Beschreibt die folgende Grafik!
- Eine Interpretation ist nicht nötig, da ihr die Gründe für den Verlauf nicht kennt.
- Bedenkt aber bitte, dass auch in dieser Grafik DREI Parameter stecken!
Arbeitsauftrag Chemie5 (verpflichtend)
- Die folgende verpflichtende Unterrichtseinheit hat eine Bearbeitungszeit von ca. 45 Minuten.
- Ihr benötigt für die Bearbeitung: Das Schulbuch, das PSE, einen Zettel, Stift und Ruhe.
- Bitte bearbeitet die gestellten Aufgaben tatsächlich erst selbst, bevor ihr auf die Lösung klickt!
Wiederholung: Aggregatszustände
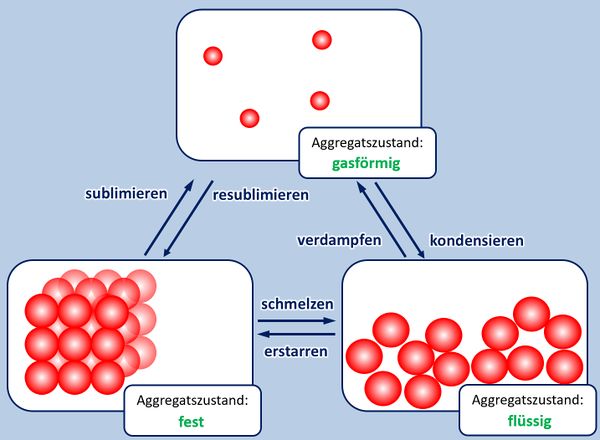
Zu Beginn der 9. Jahrgangsstufe in Chemie wurden die Aggregatszustände von Stoffen besprochen. Ebenso die Fachbegriffe für die Vorgänge wenn ein Stoff von einem in einen anderen Aggregatszustand wechselt. Zur Auffrischung dieser Inhalte noch einmal die entsprechende Abbildung:
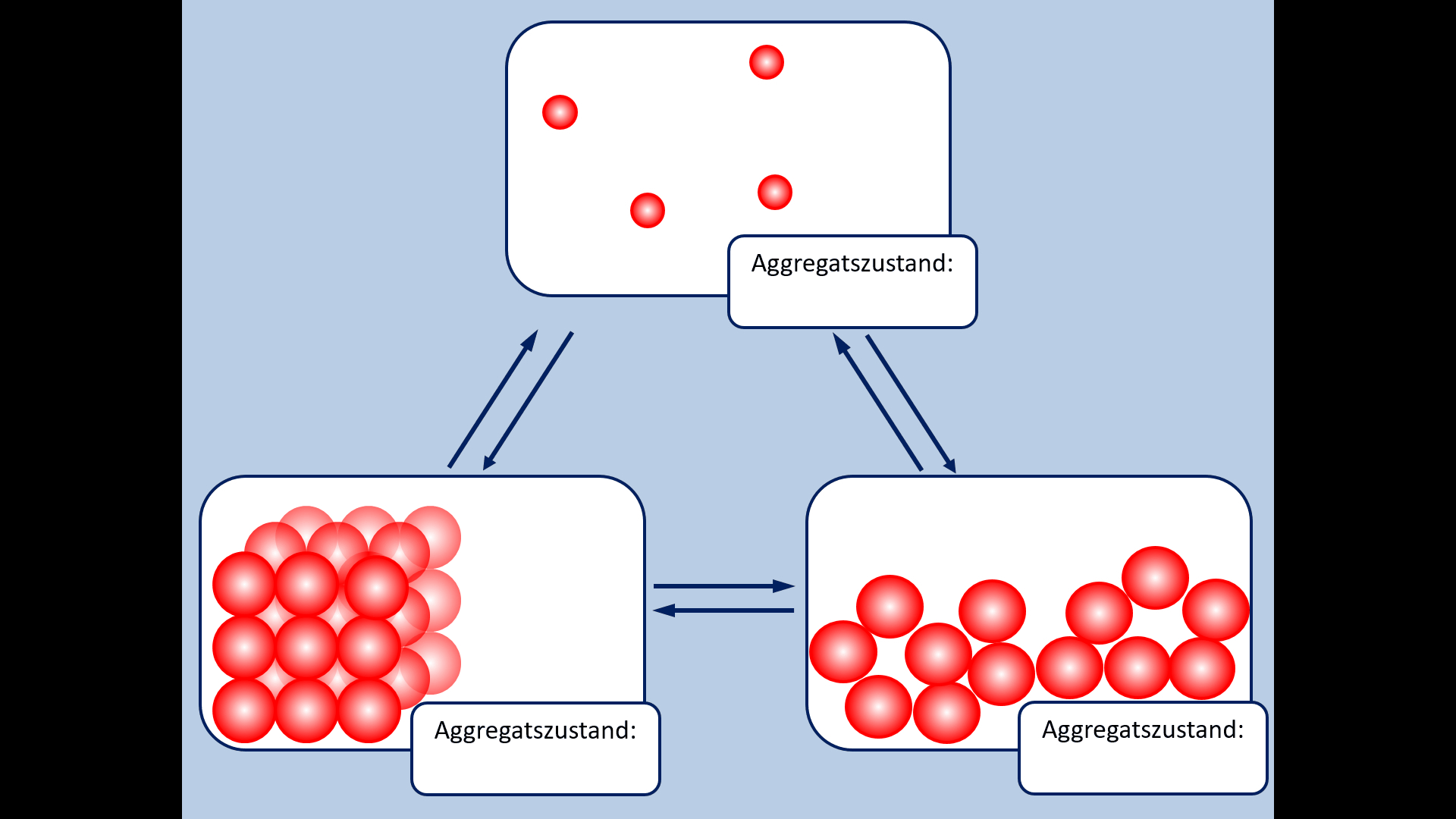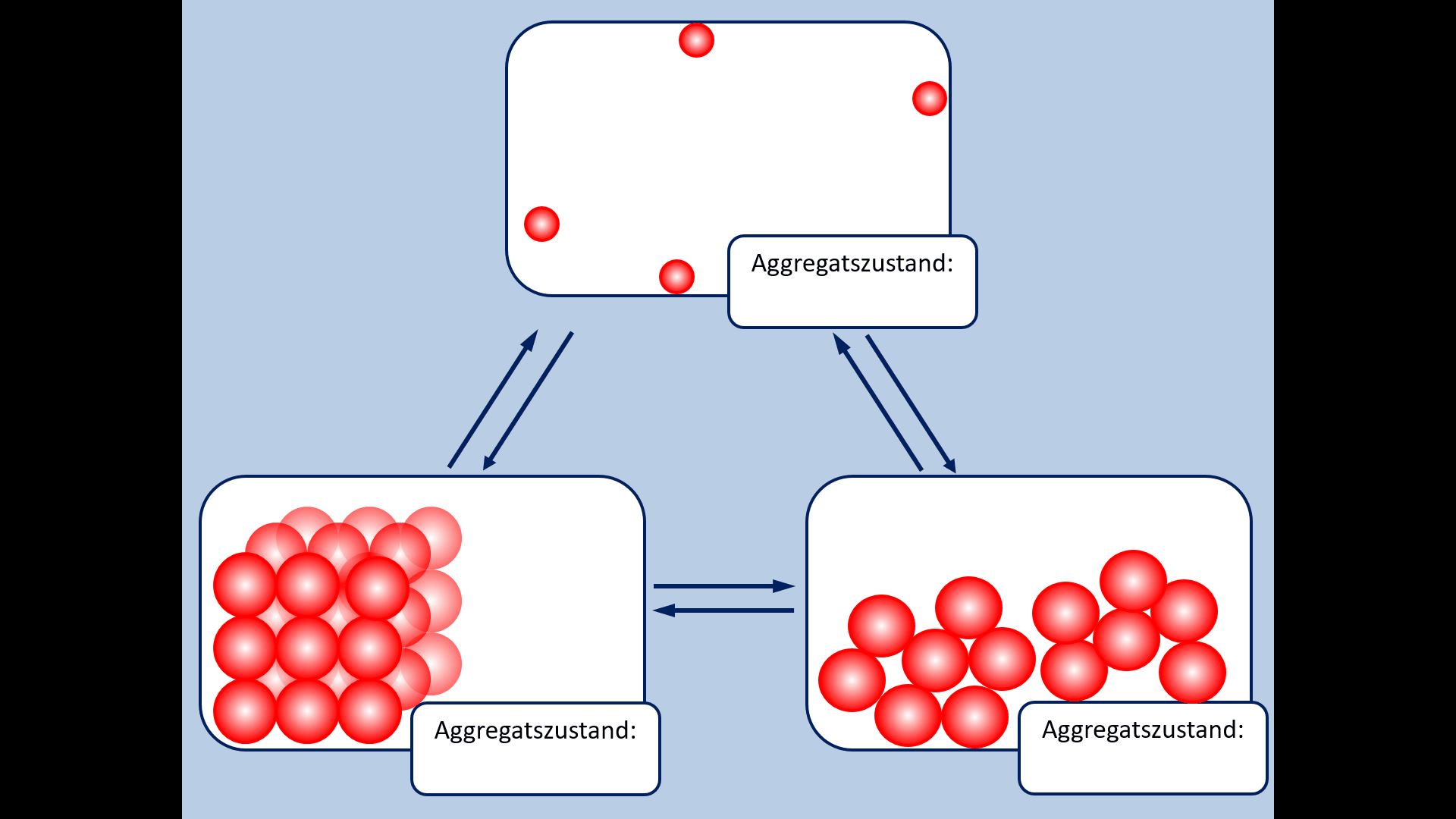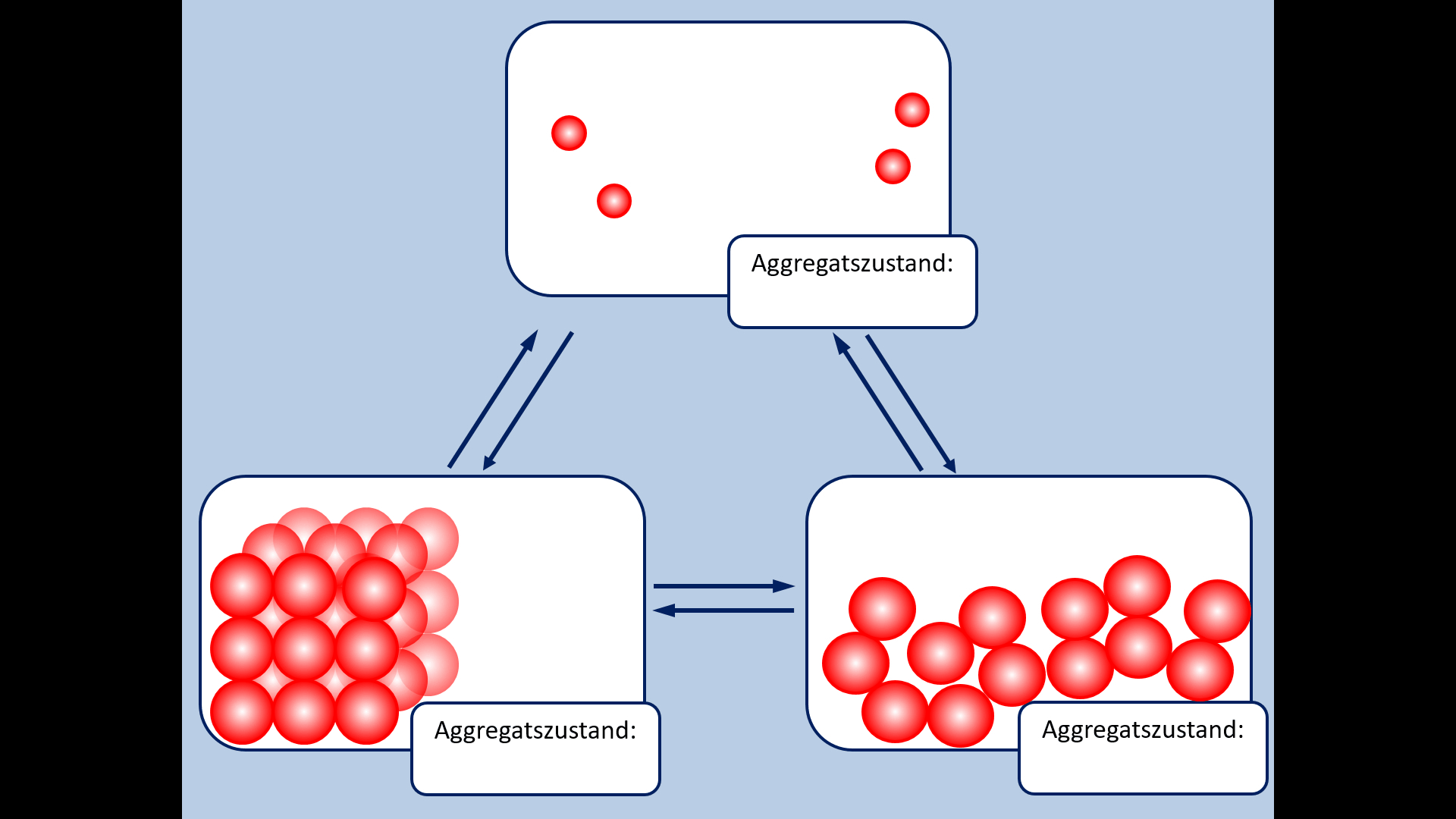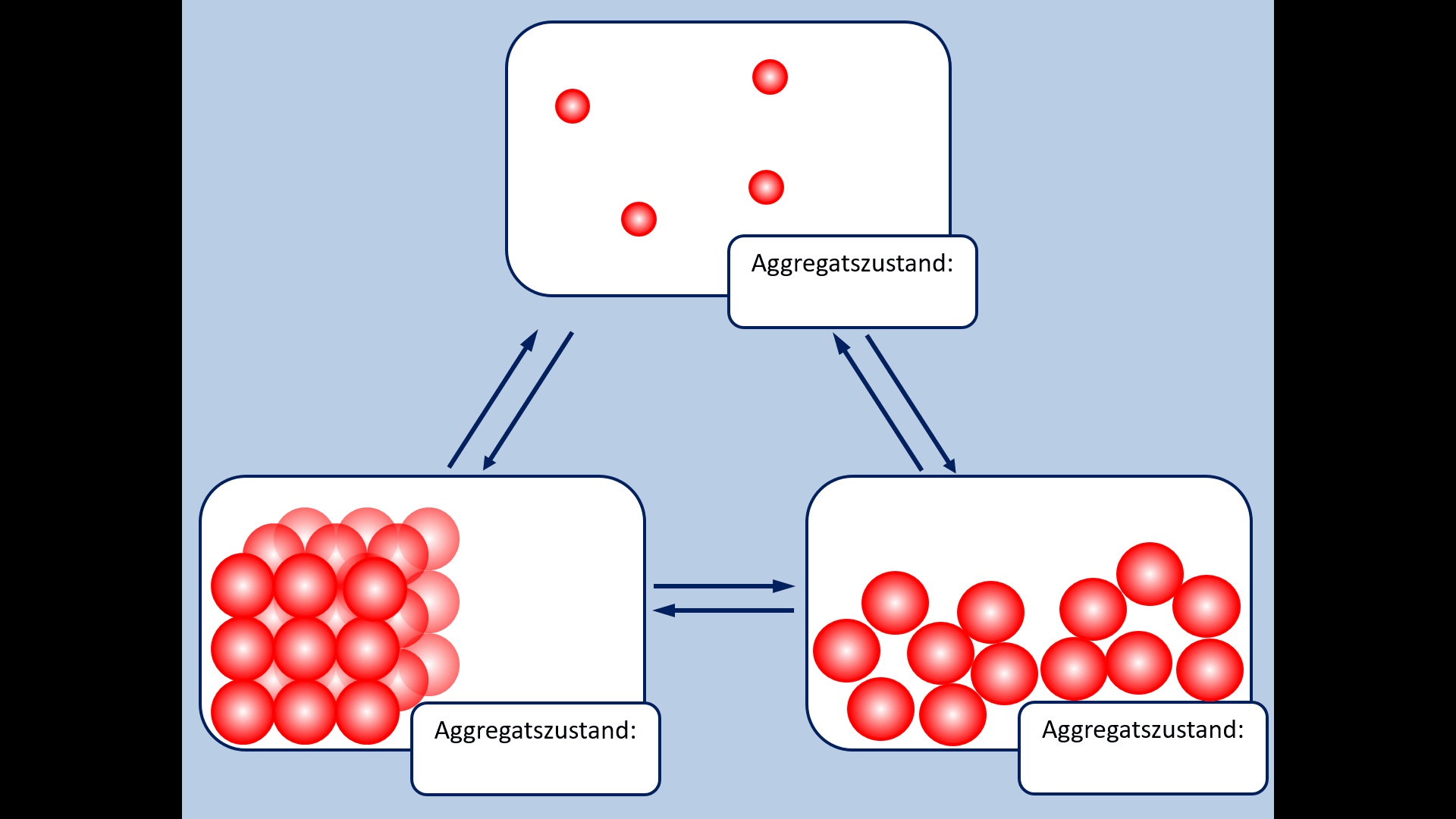
- Ergänzt die fehlenden Fachbegriffe!
Anziehungskräfte
Bei Raumtemperatur (und "normalem" Druck) liegen verschiedene Stoffe in verschiedenen Aggregatszuständen vor, z.B. ist Sauerstoff gasförmig, Wasser flüssig und Wachs fest. Um auch Wasser und Wachs bei Raumtemperatur in den gasförmigen Zustand zu überführen, muss man Energie zuführen, am einfachsten in Form von Wärme (es ginge auch z.B. durch "Mikrowellen").
Bei 100° schafft man es zwar Wasser zu verdampfen, also die Wasserteilchen voneinander zu trennen, mit Wachs klappt das bei dieser Temperatur aber noch nicht.
Stelle eine begründete Vermutung auf, woran das liegen könnte! (Schreibe einen kurzen, vernünftigen Satz.)
Die Kräfte, die die Wasserteilchen zusammenhalten und verhindern, dass sie sich bei Raumtemperatur voneinander lösen sind nicht so stark wie die Kräfte, die die Wachsteilchen zusammenhalten.
Kräfte bei Salzen
Inzwischen wisst ihr bereits einiges über den Aufbau von bestimmten Stoffen, z.B. Salzen. Ihr wisst, dass die festen Salzkristalle aus einer großen Menge unterschiedlich geladener Ionen zusammengesetzt sind, die sich alle gegenseitig anziehen. Es gibt also einen logischen Zusammenhang zwischen dem Bau und dem Aggregatszustand dieser Stoffe: Alle am Aufbau beteiligten Teilchen sind geladen, ziehen sich gegenseitig an und das entspricht starken Anziehungskräften. Es ist daher sehr viel Energie nötig, um diese Kräfte zu überwinden und Salze zu schmelzen oder zu verdampfen (z.B. liegt der Sdp. von Kochsalz (NaCl) bei 1461°C).
- Zur Wiederholung: Zeichnet den Ausschnitt aus einem Calciumoxid-Kristall (CaO)!
Calcium besitzt 2 VE und wird diese in Verbindungen abgeben (Ca -> Ca2+ + 2e-. Sauerstoff besitzt 6 VE, wird in Verbindungen also 2 aufnehmen (O + 2e- -> O2-. Damit aus diesen Ionen eine neutrales Salz entsteht, muss jeweils ein O-Atom mit einem Ca-Atom reagieren. Die chemische Formel für das Salz lautet daher CaO. Ein Ausschnitt aus dem Kristallgitter könnte so aussehen:
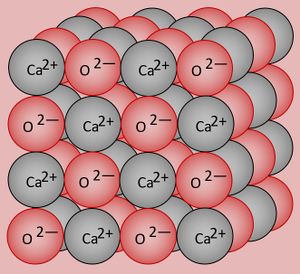
Warum Sauerstoff bei Raumtemperatur gasförmig vorliegt, solltet ihr inzwischen auch gut nachvollziehen können: Über das Sauerstoffmolekül habt ihr gelernt, dass sich zwei Sauerstoffatome über eine Doppelbindung zwei Elektronenpaare teilen und zusammen mit ihren freien Elektronenpaaren jeweils 8 VE zugerechnet bekommen. Damit liegt Edelgaskonfiguration vor. Es gibt zum jetzigen Zeitpunkt für euch keinen Grund anzunehmen, dass zu benachbarten Sauerstoffmolekülen irgendwelche Anziehungskräfte ausgebildet werden. Die Moleküle sind also voneinander getrennt und damit gasförmig:
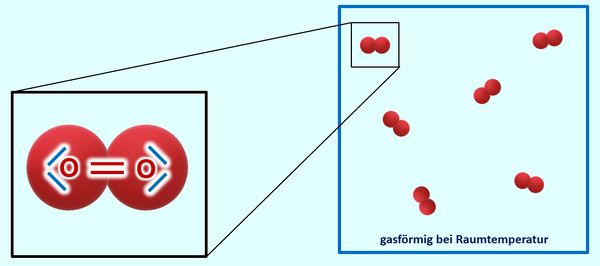
Das Problem:
Ihr habt auch den Stoff Wasser als Molekül kennengelernt. Auch hier könnt ihr erklären, warum ein Sauerstoff-Atom mit genau zwei Wasserstoffatomen eine Bindung eingeht. Mehr aber auch nicht. Auch hier sollte es keinen Grund geben, warum sich diese Moleküle untereinander anziehen sollten. Offensichtlich tun sie es aber doch. Denn bei Raumtemperatur ist Wasser flüssig, die Moleküle hängen also irgendwie aneinander. Erst bei 100°C "lassen sie sich offenbar los":
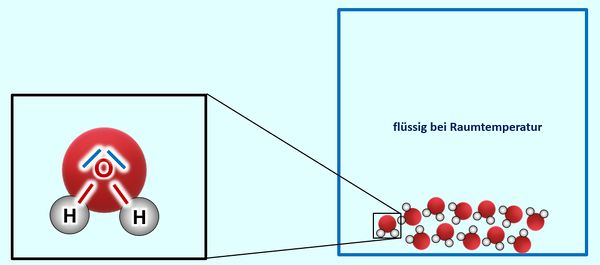
Die Lösung:
Ich muss euch enttäuschen... oder zumindest "vertrösten". Die genaue Begründung, warum sich Wassermoleküle auch gegenseitig anziehen, werdet ihr erst in der nächsten Jahrgangsstufe kennenlernen.
Das einzige, was ihr aus dieser Unterrichtsstunde mitnehmen sollt, lautet:
Auch zwischen Molekülen existieren Anziehungskräfte. Man nennt sie... (Spannung, Trommelwirbel):
Zwischenmolekulare Kräfte Wahnsinn, oder?
- Lest jetzt auf der Seite 109 den letzten Absatz "Moleküle bilden Molekülgitter"
- Legt jetzt das Buch beiseite.
- Betrachtet die folgende Abbildung und erklärt, was die (dunkelroten) durchgezogenen Linien bedeuten und was die gestrichelten Linien bedeuten!
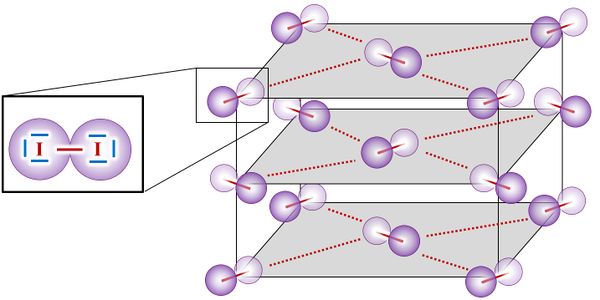
Die durchgezogenen Linien symbolisieren die Atombindungen, die zwei Iod-Atome zu einem Iod-Molekül verbinden. Die gestrichelten Linien symbolisieren die zwischenmolekularen Anziehungskräfte zwischen den Iod-Molekülen. Diese müssen überwunden werden, wenn man Iod in den gasförmigen Zustand überführen möchte (Iod sublimiert).
optional (freiwillig)
Durftet ihr als Kinder "Wachstropfen" machen? Falls nicht, hier eine kurze Anleitung:
Nehmt ein Schälchen mit Wasser und stellt ein Plätzchen-Ausstech-Förmchen hinein. Das Förmchen sollte zur Hälfte ins Wasser eintauchen. Zündet eine Kerze an und lasst das Wachs ins Förmchen tropfen. (Der Zusammenhang mit dieser Unterrichtseinheit ist: Durch die Flamme überführt ihr die Moleküle des Wachses zunächst in den flüssigen Zustand, ein Teil verdampft sogar und verbrennt. Das flüssige Wachs tropft ins Förmchen und erstarrt im kalten Wasser recht schnell.
Ihr erhaltet dann eine Fachsfigur in der Form der Ausstech-Figur:
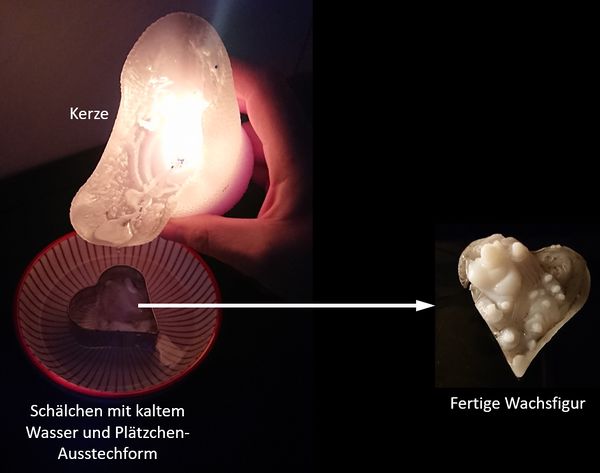
- Ihr könnt natürlich farbige (auch mehrere verschiedene) Kerzen nehmen.
- Ihr müsst kein Herz nehmen! Es geht alles, von mir aus auch ein Totenkopf (wenn ihr so etwas als Plätzchen-Ausstech-Förmchen habt.
- Fertigt eine solche Figur an und schenkt sie einem Familienmitglied oder eurer besten Freundin / bestem Freund.
Hausaufgabe
Keine Hausaufgabe, da das die letzte Stunde vor den Ferien war. Erholt euch gut, trotz Ausgangsbeschränkungen und dem Fall, dass ihr eventuell unter Quarantäne steht.
Testseiten
Eiweiß-Test-Seite
H5P-Test-Seite
Q11-Struktur-Test-Seite
verlinkte Seiten
Zu den Arbeitsaufträgen in Bio (Corona)
Zu den Arbeitsaufträgen Chemie (Corona)
Zur Schulentwicklungs-Testseite
Zur Studien- und Berufsorientierung
Zur Studien- und Berufsorientierung der Mittelstufe
Biologie-Rätsel des Monats
Biologie
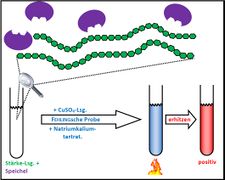
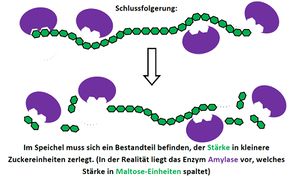
Visualisierung der Unterrichtsversuche zum Thema "Verdauungsprozesse im Mund".
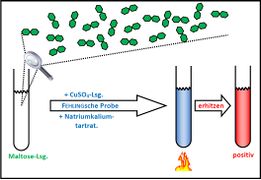
Fehling-Probe mit Maltose
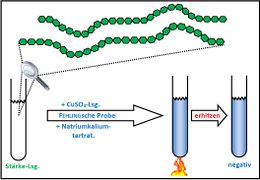
Fehling-Probe mit Stärke und Speichel
Chemie
Das Anfertigen eines Versuchsprotokolls stellt eine wichtige Grundfertigkeit dar. Auch im Hinblick auf das spätere Erstellen einer Seminararbeit. In den naturwissenschaftlichen Fächern ist die typische Gliederung einer Arbeit nämlich einem Versuchsprotokoll ganz ähnlich. Hier zwei gelungene Beispiele:
Trennung eines Gemisches aus Sand und Salz