8a 2021 22/Chemie/Thema 3 SALZE: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung |
Keine Bearbeitungszusammenfassung |
||
| Zeile 67: | Zeile 67: | ||
{{Box|Abschreiben|Übernehme die Überschrift, das kursiv gedruckte und die Tabelle ins Heft und versuche dir die Ionen schon einmal so gut es geht einzuprägen|Üben | {{Box|Abschreiben|Übernehme die Überschrift, das kursiv gedruckte und die Tabelle ins Heft und versuche dir die Ionen schon einmal so gut es geht einzuprägen. | ||
Überprüfe dein Wissen anschließend mit folgender Übung|Üben | |||
}} | }} | ||
| Zeile 74: | Zeile 76: | ||
{{Box|Merke|ACHTUNG: Wir hatten uns gemerkt, dass die Ionenladung der Wertigkeit entspricht. Das gilt auch für die Molekül-Ionen. So besitzt bspw. das Hydroxid-Ion OH- die Wertigkeit | {{Box|Merke|ACHTUNG: Wir hatten uns gemerkt, dass die Ionenladung der Wertigkeit entspricht. Das gilt auch für die Molekül-Ionen. So besitzt bspw. das Hydroxid-Ion OH- die Wertigkeit 1 und es entsteht aus Mg2+ und OH- das Salz Mg(OH)2. Man arbeitet hier wenn nötig mit Klammern|Merksatz | ||
}} | }}{{Box|Üben|Hole dir vorne am Pult die Übung des Kuverts 4 und bearbeite sie|Unterrichtsidee }} | ||
Version vom 2. Juni 2022, 10:25 Uhr
Salze in der Chemie
Salze bestehen aus Ionen
Diese Ionen lassen sich im Kern-Hülle-Modell einfach darstellen. Löse die folgenden Aufgaben, um das Kern-Hülle-Modell zu verstehen.
Salze bilden Ionengitter
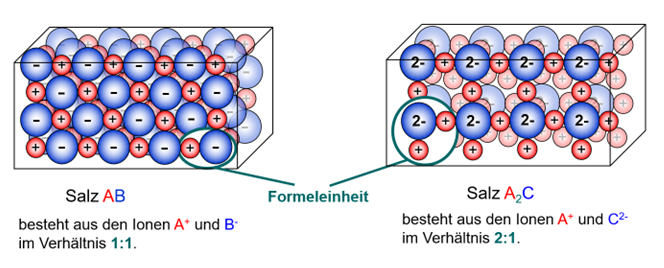
Bildet sich ein Salz neu, so setzt es sich stets aus einem bestimmten Verhältnis von Kationen und Anionen zusammen.
Da die Anziehungskraft die von einem Ion ausgeht in alle Richtungen wirkt, setzen sich mehrere dieser "gebauten Einheiten" umeinander. Es entsteht ein sog. Ionengitter. Dabei sitzen die Ionen an festen Plätzen an denen sie durch die Anziehungskräfte ihrer entgegengesetzten Ladungen gehalten werden.
Auch im Ionengitter selbst, spiegelt sich dabei das bestimmte Verhältnis von Kationen zu Anionen. Die von dir zusammengesetzte Einheit ist quasi der Grundbaustein des Salzes. Millionen bzw. Milliarden dieser Grundbausteine lagern sich aneinander und bilden schließlich den Salzkristall
Diesen Grundbaustein selbst bezeichnet man auch als Formeleinheit.
Bearbeite anschließend folgende Übungen:
Benennung der Ionen
Die Benennung der Ionen hast du bereits bei den Benennungen der Salze mitgelernt
Die Metallkationen besitzen den deutschen Namen z.B. Natriumion, Kaliumion,
die Nichtmetallantionen dagegegen den lateinischen Nachnamen z.B. Sulfid-Ion, Oxid-Ion usw.
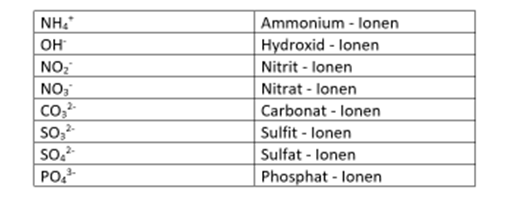
Allerdings gibt es ein paar besondere Ionen, die sog. Molekülionen, die man auswendig lernen muss. Salze wie bspw. Gips, Kalk oder Soda bestehen aus ihnen.