8a 2021 22/Chemie/Thema 3 SALZE: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
Keine Bearbeitungszusammenfassung |
||
| Zeile 13: | Zeile 13: | ||
===Salze bilden Ionengitter=== | ===Salze bilden Ionengitter=== | ||
Bildet sich ein Salz neu, so setzt es sich stets aus einem bestimmten Verhältnis von Kationen und Anionen zusammen. | ''Bildet sich ein Salz neu, so setzt es sich stets aus einem bestimmten Verhältnis von Kationen und Anionen zusammen.'' | ||
<br /> | <br /> | ||
{{Box|Warum ist das so?|Nehme dir ein Kuvert vom Pult und setze mit den vorhanden Kationen und Anionen 7 mögliche Salze zusammen. | {{Box|Warum ist das so?|Nehme dir ein Kuvert vom Pult, schneide die Teilchen GROB aus und setze mit den vorhanden Kationen und Anionen 7 mögliche Salze zusammen. | ||
ACHTUNG: Verwende hierfür kein PSE. | |||
Nach welchem Kriterium gehst du vor? | |||
Lasse deine Teilchen durch die Lehrkraft kontrollieren! | |||
Übernehme die Überschrift und das kursiv gedruckte und skizziere deine Teilchen ins Heft. Erstelle die jeweiligen | |||
Formeln daneben, die deine Salze beschreiben.|Unterrichtsidee }} | |||
[[Datei:Formeleinheit.png| | |||
''Da die Anziehungskraft die von einem Ion ausgeht in alle Richtungen wirkt, setzen sich mehrere deiner "gebauten Einheiten" umeinander. Es entsteht ein sog. Ionengitter. Dabei sitzen die Ionen an festen Plätzen an denen sie durch die Anziehungskräfte ihrer entgegengesetzten Ladungen gehalten werden.'' | |||
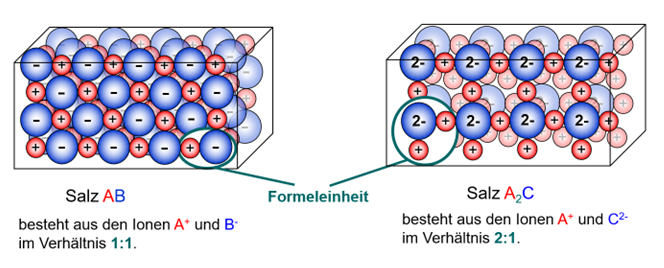
Auch im Ionengitter selbst, spiegelt sich dabei das bestimmte Verhältnis von Kationen zu Anionen. Die von dir zusammengesetzte Einheit ist quasi der Grundbaustein des Salzes. Millionen bzw. Milliarden dieser Grundbausteine lagern sich aneinander und bilden schließlich den Salzkristall | |||
Diesen Grundbaustein selbst bezeichnet man auch als Formeleinheit. | |||
<br /> | |||
[[Datei:Formeleinheit.png|Ionengitter|alternativtext=|links|gerahmt]] | |||
Version vom 2. Juni 2022, 08:36 Uhr
Salze in der Chemie
Salze bestehen aus Ionen
Diese Ionen lassen sich im Kern-Hülle-Modell einfach darstellen. Löse die folgenden Aufgaben, um das Kern-Hülle-Modell zu verstehen.
Salze bilden Ionengitter
Bildet sich ein Salz neu, so setzt es sich stets aus einem bestimmten Verhältnis von Kationen und Anionen zusammen.
Da die Anziehungskraft die von einem Ion ausgeht in alle Richtungen wirkt, setzen sich mehrere deiner "gebauten Einheiten" umeinander. Es entsteht ein sog. Ionengitter. Dabei sitzen die Ionen an festen Plätzen an denen sie durch die Anziehungskräfte ihrer entgegengesetzten Ladungen gehalten werden.
Auch im Ionengitter selbst, spiegelt sich dabei das bestimmte Verhältnis von Kationen zu Anionen. Die von dir zusammengesetzte Einheit ist quasi der Grundbaustein des Salzes. Millionen bzw. Milliarden dieser Grundbausteine lagern sich aneinander und bilden schließlich den Salzkristall
Diesen Grundbaustein selbst bezeichnet man auch als Formeleinheit.