8a 2022 23
Inhaltsverzeichnis
Chemie
- 2. Schulaufgabe: Montag, 19.06.23
aktuelle Aufgaben zum Üben
Allgemein müsst ihr mit folgenden Größen umgehen können:
- Masse eines Stoffes:
, Einheit:
(Gramm)
- Die tatsächlich Anzahl von Teilchen eines Stoffes:
, keine Einheit
- Das Volumen eines (gasförmigen) Stoffes:
, Einheit:
(Liter)
- Stoffmenge eines Stoffes:
, Einheit:
- molare Masse eines Stoffes:
, Einheit
, kann für Atome aus dem PSE abgeleitet werden
- Die Avogadrokonstante
- molares Volumen eines (gasförmigen) Stoffes bei Standardbedingungen (273°C und 1013hPa):
, Einheit
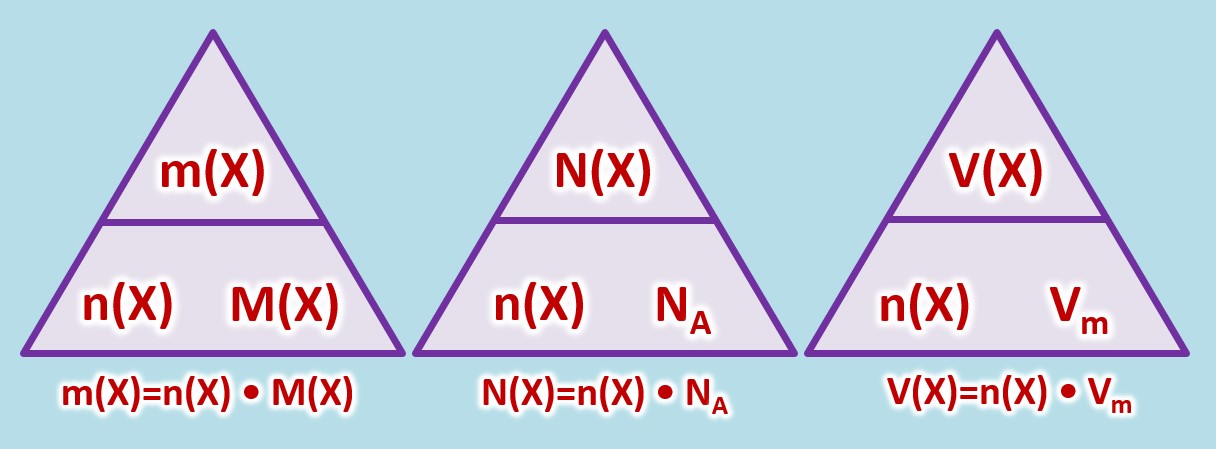
Es gelten die folgenden Zusammenhänge:
Online-Unterricht am 09.01.2023
- Arbeitet die folgenden Blöcke der Reihe nach ab.
- Nutzt das ausgeteilte Arbeitsblatt, um eure Lösungsvorschläge zu dokumentieren.
- Vergleicht eure Lösungen mit der angegebenen Musterlösung selbständig!
Stelle jeweils die Gleichungen für die folgenden chemischen Reaktionen auf:
Reaktion 1: Bei der positiven Knallgasprobe reagiert das aufgefangene Gas Wasserstoff mit dem Sauerstoff aus der Luft im Zuge einer kleinen Explosion zu gasförmigem Wasser.
Nicht schummeln: Wirklich erst auf Lösung klicken, wenn ihr selbst eine chemische Gleichung auf dem Arbeitsblatt stehen habt!
2 H2 + O2 --> 2 H2O
Reaktion 2: Entzündet man ein Magnesiumband, so reagiert es ebenfalls mit dem in der Luft enthaltenen Sauerstoff zu der Verbindung Magnesiumoxid (MgO). Bei der Reaktion entsteht ein sehr helles Licht, in das man nicht längere Zeit hinein schauen sollte.
2 Mg + O2 --> 2 MgO
Reaktion 3: Eine pulverförmige Mischung aus Eisen und Schwefel wird als lange Spur auf eine feuerfeste Platte gestreut. Es genügt nun, diese Spur am einen Ende zu entzünden, um eine Reaktion zu starten, bei der die Verbindung Eisensulfid (FeS2) entsteht. Das Gemisch glüht nach und nach vom einen Ende bis zum anderen komplett durch.
Fe + 2 S --> FeS2
Reaktion 4: Im Hofmannschen Dreischenkelapparat wird die Verbindung Wasser in die beiden Produkte Wasserstoff und Sauerstoff gespalten, solange die Spannungsquelle angeschaltet ist.
2 H2O --> 2 H2 + O2
Reaktion 5: Quecksilberoxid (HgO) ist eine sehr giftige Verbindung. Wenn man sie auf über 500°C erhitzt und diese Temperatur permanent aufrecht erhält, zerfällt sie. Dabei entsteht reines Quecksilber und Sauerstoff.
2 HgO --> 2 Hg + O2
Reaktion 6: Die Verbindung Wasserstoffperoxid (H2O2) zerfällt unter bestimmten Bedingungen schon bei Raumtemperatur zu Wasser und Sauerstoff.
2 H2O2 --> 2 H2O + O2
- Betrachtet nun die chemischen Reaktionsgleichungen der Reaktionen 1-3 und 4-6.
- Die Reaktionen 1-3 haben eine Gemeinsamkeit und die Reaktionen 4-6 haben eine Gemeinsamkeit.
- Formuliert jeweils einen allgemeinen Satz, der die Gemeinsamkeit bei den Reaktionen 1-3 bzw. 4-6 beschreibt.
- Sucht euch dann eine/n Partnerin in der Klasse, der ebenfalls gerade diesen Aufgabenblock bearbeitet. Lest ihr/ihm eure beiden Sätze vor. Hört euch ihre/seine beiden Sätze an. Entscheidet euch für die beste Variante und bessert eure eigenen Sätze eventuell aus.
- Erst jetzt (nachdem ihr euch mit jemandem in der Klasse besprochen habt) dürft ihr euch hier die Musterlösungsvorschläge anschauen.
- Falls eure Lösung zu stark von der Musterlösung abweicht, müsst ihr sie erneut ausbessern
Letzte Warnung: Ihr müsst eure Lösung erst mit jemandem besprochen und evtl. verbessert haben, bevor ihr auf Lösung klickt!
Gemeinsamkeiten bei den Reaktionen 1-3:
Hier entsteht aus zwei Edukten immer ein Produkt.
Gemeinsamkeiten bei den Reaktionen 4-6:
Hier entstehen aus einem Edukt immer zwei Produkte.
- Lest den folgenden Text zu unterschiedlichen Reaktionstypen.
- Füllt auf eurem Arbeitsblatt die noch leeren Lücken auf!
Infotext
Man kann chemische Reaktionen danach einteilen, wie viele Edukte und Produkte daran beteiligt sind. Entsteht bei einer chemischen Reaktion nur ein einziges Produkt aus mehreren Edukten, spricht man von einer Synthese. Umgekehrt spricht man von einer Analyse, wenn aus einem einzigen Edukt mehrere Produkte entstehen. Von einer Umsetzung spricht man, wenn mehrere Edukte und mehrere Produkte auftauchen.
Grundwissen
Folgende Begriffe und Methoden solltest Du bereits erklären können:
- homogen/heterogen
- Legierung, Lösung, Gasgemisch
- Feststoffgemisch (Gemenge), Suspension, Emulsion, Nebel, Rauch, Schaum
- Filtrieren, Destillieren, Chromatographieren
- Zustände: fest (s), flüssig (l), gasförmig (g)
- Zustandsänderungen: schmelzen, erstarren, sieden, kondensieren, sublimieren, resublimieren
Das Interpretieren von Grafiken (auch Tabellen oder Karikaturen) ist eine oft verlangte Fähigkeit von Oberstufen-Schülern. Ich empfehle folgendes Vorgehen:
- Man beginnt mit einer Beschreibung
- Was zeigt die Grafik? (y-Achse und x-Achse in Beziehung setzen, z.B. mit der Formulierung: "Die Grafik zeigt das was auf der y-Achse steht in Abhängigkeit von dem was auf der x-Achse steht.)
- Welche Zusammenhänge sind zu sehen? Man verzichtet zunächst auf Erklärungen/Begründungen, bleibt zunächst noch bei einer reinen Beschreibung (Schöne Formulierungen: "Je ...größer/kleiner/höher/niedriger/usw. desto ..."
- Erst zum Schluss versucht man die Zusammenhänge zu erklären. Je nach behandeltem Stoff im Unterricht kann diese Erklärung recht umfangreiches Wissen verlangen. Gelegentlich sind hier auch Hypothesen über eine mögliche Begründung verlangt, die noch nicht besprochen wurden.
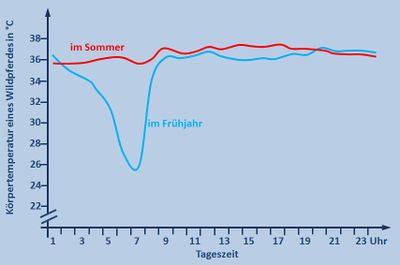
Abb. selbst erstellt, Originalgrafik: Kuntz, Regina; Der versteckte Winterschlaf der Wildpferde; Spektrum der Wissenschaft; August 2008; S. 46 - 53, 2008
Versucht zunächst selbst diese Grafiken zu interpretieren. - Lasst euch dann die Lösung anzeigen.
- Die Grafik zeigt die Körpertemperatur eines Wildpferdes in Abhängigkeit von der Uhrzeit einmal im Sommer und einmal im Winter.
- Im Sommer bleibt die Körpertemperatur den ganzen Tag konstant bei 36°C. Im Frühjahr sinkt die Körpertemperatur nachts und in den frühen Morgenstunden um 10°C auf 26°C ab. Ab 08:00 Uhr steigt sie wieder auf 36°C und bleibt dann konstant.
- Im Unterricht könnte man dazu folgendes besprochen haben: Die Sommerkurve ist völlig normal. Pferde zählen zu den gleichwarmen Tieren und halten ihre Körpertemperatur konstant. Überraschend ist das starke Absinken der Körpertemperatur in der Nacht in kalten Frühjahrsnächten. Wahrscheinlich hat das Pferd aber einen Vorteil von dieser Absenkung, denn es muss weniger Wärme erzeugen, um den Körper über die Umgebung aufzuheizen. Dadurch spart es z.B. Fettreserven und Nahrung.
- Aus wie vielen Protonen, Neutronen und Elektronen ist ein Fluor-Atom aufgebaut?
- Verwendet euer PSE! - Natürlich könntet ihr die Lösung auch googeln, aber in der Schulaufgabe oder in einem Test steht euch nur das PSE zur Verfügung, nicht Google!
Nicht schummeln: Wirklich erst auf Lösung klicken, wenn ihr eine Lösung aufgeschrieben habt!
- Protonen: 9 (erkennbar an der "Kernladungszahl" oder auch "Ordnungszahl", steht in der Regel unten links beim Elementsymbol
- Neutronen: 10 (erkennbar an der "Massenzahl", die in der Regel oben links beim Elementsymbol steht, abzüglich der "Kernladungszahl")
- Elektronen: 9 (bei ungeladenen Atomen muss die Anzahl der Elektronen genau so groß sein, wie die Anzahl der Protonen
- Ein Diamant besteht aus reinem Kohlenstoff. Üblicherweiße wird das Gewicht eines Diamanten in Karat angegeben. Es soll ein Diamant mit exakt einem Karat betrachtet werden. Das entspricht einer Masse von 0,2 Gramm. Berechne die Stoffmenge der Kohlenstoffatome in diesem Diamanten!
Hier ist die Stoffmenge gesucht, gegeben ist die Masse von Kohlenstoff. Die Molare Masse für Atome kann man direkt aus dem PSE ablesen, der Zahlenwert entspricht der "Massenzahl" (in der Regel oben links).
gesucht:
gegeben: ,
Formel:
Einsetzen der Werte in die Formel:
- Aus wie vielen Protonen, Neutronen und Elektronen ist ein Magnesium-Atom aufgebaut?
- Verwendet euer PSE! - Natürlich könntet ihr die Lösung auch googeln, aber in der Schulaufgabe oder in einem Test steht euch nur das PSE zur Verfügung, nicht Google!
Nicht schummeln: Wirklich erst auf Lösung klicken, wenn ihr eine Lösung aufgeschrieben habt!
- Protonen: 12 (erkennbar an der "Kernladungszahl" oder auch "Ordnungszahl", steht in der Regel unten links beim Elementsymbol
- Neutronen: 12 oder 13 (erkennbar an der "Massenzahl", die in der Regel oben links beim Elementsymbol steht, abzüglich der "Kernladungszahl")
- Elektronen: 12 (bei ungeladenen Atomen muss die Anzahl der Elektronen genau so groß sein, wie die Anzahl der Protonen
- Berechne die Masse einer Portion Wasser, deren Stoffmenge n(H2O) = 1,0mol beträgt! (Man könnte auch einfacher fragen: Wie viel Gramm wiegt 1 Mol Wasser?)
Hier ist die Massegesucht, gegeben ist die Stoffmenge von Wasser. Die Molare Masse für Moleküle wie H2O kann durch Addition der am Aufbau beteiligten Atome direkt aus dem PSE abgeleitet werden.
gesucht:
gegeben: ,
Formel:
Einsetzen der Werte in die Formel:
- Aus wie vielen Protonen, Neutronen und Elektronen ist ein Schwefel-Atom aufgebaut?
- Verwendet euer PSE! - Natürlich könntet ihr die Lösung auch googeln, aber in der Schulaufgabe oder in einem Test steht euch nur das PSE zur Verfügung, nicht Google!
Nicht schummeln: Wirklich erst auf Lösung klicken, wenn ihr eine Lösung aufgeschrieben habt!
- Protonen: 16 (erkennbar an der "Kernladungszahl" oder auch "Ordnungszahl", steht in der Regel unten links beim Elementsymbol
- Neutronen: 16 (erkennbar an der "Massenzahl", die in der Regel oben links beim Elementsymbol steht, abzüglich der "Kernladungszahl")
- Elektronen: 16 (bei ungeladenen Atomen muss die Anzahl der Elektronen genau so groß sein, wie die Anzahl der Protonen
- Stelle die chemische Gleichung auf: Magnesium reagiert mit Sauerstoff zu Magnesiumoxid. Das ist eine Verbindung mit der chemischen Formel MgO
2 Mg + O2 --> 2 MgO
- Wenn man die Reaktion in einem abgeschlossenen Gefäß durchführt, in das man vorher exakt 1 Mol Sauerstoffmoleküle (O2) eingesperrt wurden, welche Stoffmenge an Magnesiumatomen muss man dazu geben, damit die Reaktion vollständig abläuft (also alle Sauerstoffmoleküle verbraucht werden)?
Das hat eigentlich nicht viel mit "chemischem Rechnen" zu tun: Gesucht wird hier die Stoffmenge n(Mg), Einheit "mol". Aus der chemischen Gleichung geht hervor, dass vom Verhältnis her immer zwei Magnesiumteilchen mit einem Sauerstoffmolekül reagieren. Da "Mol" nichts anderes ist, als die Bezeichnung für eine bestimmte Anzahl an Teilchen, bedeutet die Gleichung aber auch gleichzeitig: Zwei Mol Magnesium reagieren mit einem Mol Sauerstoffmoleküle. Jetzt sollte man aber auf die Lösung kommen.
Es müssen 2 Mol Magnesium dazu gegeben werden, damit alle Sauerstoff-Moleküle reagieren. - Zusatzfrage: Wie viel Gramm sind das? Oder anders: Welcher Masse an Magnesium entspricht das?
gesucht:
gegeben: ,
Formel:
Einsetzen der Werte in die Formel:
- Aus wie vielen Protonen, Neutronen und Elektronen ist ein Kalium-Atom aufgebaut?
- Welche Ionen bildet Kalium, wenn es mit Nichtmetallen zu einem Salz reagiert?
- Verwendet euer PSE! - Natürlich könntet ihr die Lösung auch googeln, aber in der Schulaufgabe oder in einem Test steht euch nur das PSE zur Verfügung, nicht Google!
Nicht schummeln: Wirklich erst auf Lösung klicken, wenn ihr eine Lösung aufgeschrieben habt!
- Protonen: 19 (erkennbar an der "Kernladungszahl" oder auch "Ordnungszahl", steht in der Regel unten links beim Elementsymbol
- Neutronen: 20 (erkennbar an der "Massenzahl", die in der Regel oben links beim Elementsymbol steht, abzüglich der "Kernladungszahl")
- Elektronen: 19 (bei ungeladenen Atomen muss die Anzahl der Elektronen genau so groß sein, wie die Anzahl der Protonen
- Kalium bildet in Salzen einfach positiv geladene Kationen, K+
- Stelle die chemische Gleichung auf: Kalium reagiert mit Sauerstoff zu Kaliumoxid.
- Man muss erkennen, dass Kaliumoxid ein Salz ist, das aus positiv geladenen Kationen und negativ geladenen Anionen besteht.
- Die Kaliumionen sind (wie in der Aufgabe oben bereits erwähnt) einfach positiv geladen: K+
- Sauerstoff steht in der 6. Hauptgruppe und bildet demzufolge immer zweifach negativ geladene Anionen O2-
- Wenn aus diesen beiden Ionen ein Salz gebildet werden soll, das insgesamt ungeladen ist, dann braucht man zwei K+-Ionen pro einem O2--Ion. Daraus folgt die Summenformel für Kaliumoxid: K2O
- Die chemische Gleichung lautet dann:
4 K + O2 --> 2 K2O
- Wenn man die Reaktion in einem abgeschlossenen Gefäß durchführt, in das man vorher exakt 2 Mol Sauerstoffmoleküle (O2) eingesperrt wurden, welche Stoffmenge an Kaliumatomen muss man dazu geben, damit die Reaktion vollständig abläuft (also alle Sauerstoffmoleküle verbraucht werden)?
Das hat eigentlich nicht viel mit "chemischem Rechnen" zu tun: Gesucht wird hier die Stoffmenge n(K), Einheit "mol". Aus der chemischen Gleichung geht hervor, dass vom Verhältnis her immer vier Kaliumteilchen mit einem Sauerstoffmolekül reagieren. Da "Mol" nichts anderes ist, als die Bezeichnung für eine bestimmte Anzahl an Teilchen, bedeutet die Gleichung aber auch gleichzeitig: Vier Mol Kalium reagieren mit einem Mol Sauerstoffmoleküle. Jetzt sollte man aber auf die Lösung kommen.
Es müssen 8 Mol Kalium dazu gegeben werden, damit alle Sauerstoff-Moleküle reagieren. - Zusatzfrage: Wie viel Gramm sind das? Oder anders: Welcher Masse an Kalium entspricht das?
gesucht:
gegeben: ,
Formel:
Einsetzen der Werte in die Formel:
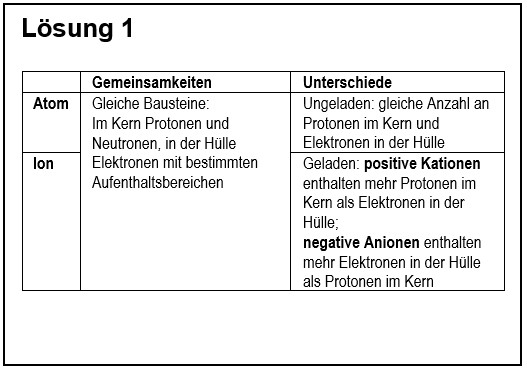
1. Vergleiche in übersichtlicher Form ein Atom mit einem Ion!
2. Beschreibe mit Hilfe einer chemischen Gleichung die Bildung von Cäsiumchlorid aus den Elementen1 Stelle vorher die Gleichungen zur Bildung der Ionen aus den Elementen auf!
3. Wähle aus den folgenden Eigenschaften diejenigen aus, die sich mit dem Ionengitter von Salzen erklären lassen: Verformbarkeit - große Bindungskräfte - Löslichkeit - elektrische Leitfähigkeit - Sprödigkeit - niedrige Siedetemperatur - Reaktionsträgheit.
4. Beziehe zu folgender Aussage begründet Stellung: Beim Schmelzen von Kaliumbromid müssen Ionen entstanden sein, weil die Schmelze elektrisch leitfähig ist.
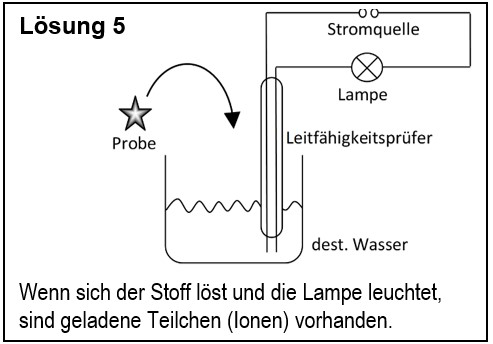
5. Entwirf einen Versuch, mit dem man zeigen kann, dass ein unbekannter Feststoff aus Ionen besteht.
6. Formuliere (mit Ionengleichungen) die Bildung von folgenden Salzen: Mg3N2, CaO, KI, BaCl2 und Aluminiumfluorid
7. Sortiere folgende Teilchen nach abnehmender Teilchengröße: Li+, K, S2-, Na+
8. Ermittle das Zahlenverhältnis der Ionen in folgenden Salzen: Kaliumsulfid, Aluminiumoxid, Natriumbromid, Calciumoxid.
Versuchsprotokolle
Freitag, 30.09.
- Im Unterricht: Filzstift-Chromatographie
- Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken
Montag, 10.10.
- Chemie-Übung: Trennung eines Sand-Salz-Gemisches
- Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken
Montag, 07.11.
- Chemie-Übung: Wasserstoff oder Sauerstoff?
- Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken
Montag, 27.02. und 06.03
- Chemie-Übung: Flammenfärbung
- 1. Übung: Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken
- 2. Übung: Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken
20.03. - 08.05.: Fällungsreaktionen
- Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken neue Version hochgeladen am 14.04., Fehler ausgebessert
- Erklärung der Fällungsreaktion auf Teilchenebene als .pdf-Datei: Hier klicken
- Unterscheidung von Silberchlorid-, Silberbromid und Silberiodid-Niederschlag als .pdf-Datei: Hier klicken
- Fällung und Unterscheidung von Carbonat- und Sulfat-Ionen als .pdf-Datei: Hier klicken
15.05-22.05.: Ionenlotto
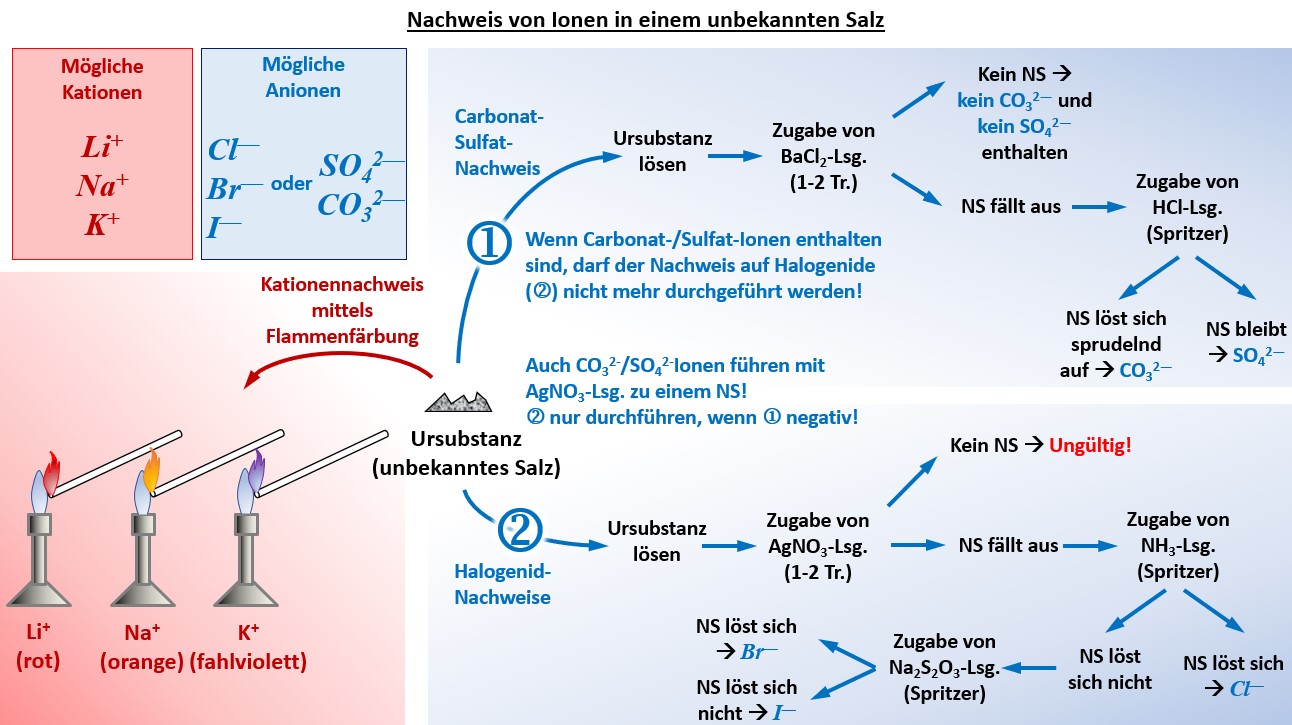
- Im Unterricht gestellte Aufgabe: "Identifiziere in der unbekannten Salzprobe die vorhanden Kationen und Anionen! Die Salzprobe enthält eines der folgenden Kationen: K+, Na+, Li+ und eines der folgenden Anionen: Cl-, Br-, I-, CO32-, SO42-. Fertige ein sauberes Protokoll an, in dem vor allem die Durchführung und das Ergebnis dargestellt wird!"
- Zwei zu dieser Aufgabe passende Muster-Protokoll als .pdf-Datei: Hier klicken
- Übersicht über die praktisch durchzuführenden Schritte:
Montag, 03.07.
- Eigenschaften von Alkanen (einfache Kohlenwasserstoffe)
- Versuchsprotokoll zum Herunterladen als .pdf-Datei: Hier klicken
Lernstoff für angekündigte Leistungsnachweise
Schulaufgabe am 19.06.
Neben den Hefteinträgen und dem oben genannten Grundwissen, eignen sich folgende Seiten im Buch (Galvani - Chemie 8) zur Vorbereitung auf die Schulaufgabe:
- S. 146 - 147: Aufbau von Salzen
- S. 150 - 151: Verhältnisformeln
- S. 152 - 153: Periodensystem der Atome und Ionen
- S. 154 - 155: Eigenschaften von Salzen
- S. 162 - 163 : Ionennachweise
- S. 164: Flammenfärbung
- S. 174 - 176: Metalle und ihre Eigenschaften
- S. 120 - 121: Atommasse
- S. 122 - 124: Stoffmenge, molare Masse und molares Volumen
Schulaufgabe am 16.12.
Neben den Hefteinträgen und dem oben genannten Grundwissen, eignen sich folgende Seiten im Buch (Galvani - Chemie 8) zur Vorbereitung auf die Schulaufgabe:
- S. 10 - 11: Das ist Chemie...
- S. 22 - 24: Aggregatzustände
- S. 26 - 28: Eigenschaften von Stoffen
- S. 44 - 45: Reinstoffe und Stoffgemische
- S. 46 - 48: Homogene und heterogene Stoffgemische
- S. 56 - 58: Trennmethoden
- S. 60 - 62: Luft - Zusammensetzung, Verflüssigung
- S. 64 - 65: Gasnachweise
- S. 92 - 93: (+ S. 94): Atommodelle (Gesetz von der Erhaltung der Masse, Gesetz von den konstanten Proportionen)
- S. 101 + 103: Aufstellen von chemischen Reaktionsgleichungen