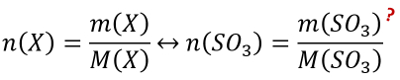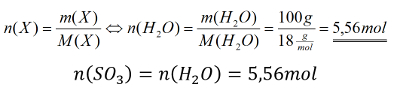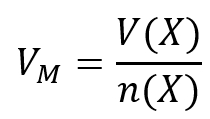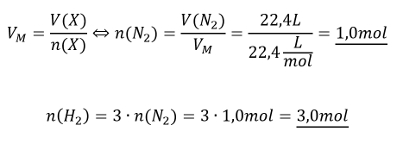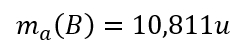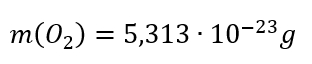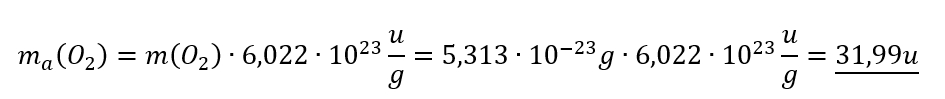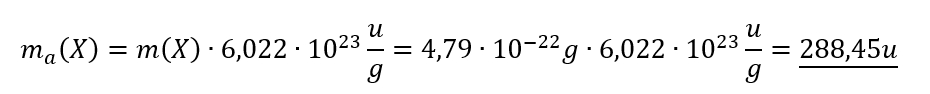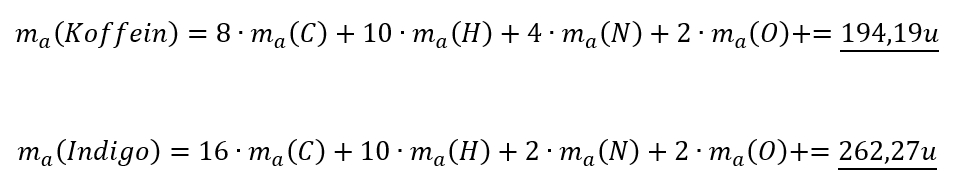Benutzer:Thomas Lux/Test Oberstufe
Inhaltsverzeichnis
- 1 Arbeitsaufträge für Fr., 22.02.
- 2 Distanzunterricht, Montag 15.02.
- 2.1 Distanzunterricht Montag, 08.02.
- 2.2 Distanzunterricht Dienstag, 26.01.
- 2.3 Distanzunterricht Dienstag, 26.01.
- 2.4 Distanzunterricht Donnerstag 20.01. Chemie
- 2.5 Distanzunterricht Mittwoch, 19.01.
- 2.6 Distanzunterricht Montag, 18.01.
- 2.7 Distanzunterricht Montag, 18.01.
- 2.8 Distanzunterricht Montag, 18.01.
- 2.9 Distanzunterricht Donnerstag, 14.01. Chemie
- 2.10 Distanzunterricht Freitag, 15.01. Chemie
- 2.11 Distanzunterricht Donnerstag, 14.01. Chemie
- 2.12 Distanzunterricht Donnerstag, 14.01. Bio
Arbeitsaufträge für Fr., 22.02.
Zu bearbeiten: Am besten heute.
Zur Bearbeitung benötig ihr das Schulbuch, einen Zettel, einen Stift und eine Internetverbindung um Videos zu schauen. Und Ruhe!
Die Bearbeitungszeit sollte ca. 60 Minuten betragen.
Die optionalen Inhalte sind nicht in die Bearbeitungszeit mit eingerechnet.
In den nächsten Wochen werden wir uns intensiv mit der Frage beschäftigen, wie es sein kann, dass ein Stück Erbgut überhaupt für ein bestimmtes Merkmal verantwortlich sein kein. Bildlich könnte man sich das ganze so vorstellen: Was passiert alles an der Stelle, an der im folgenden Bild der Pfeil mit dem Fragezeichen steht.
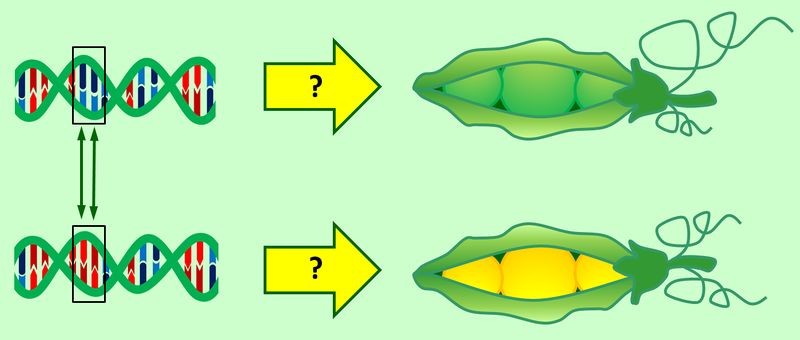
Das Ganze ist nicht neu. Fast alles wurde bereits in der 9. Jahrgangsstufe besprochen (bzw. "sollte besprochen worden sein"). Vielleicht habt ihr die Stichworte Proteinbiosynthese, Transkription oder Translation noch in Erinnerung. Bevor wir diese molekularen Mechanismen wieder auffrischen zunächst noch eine Wiederholung der anderen Art: Im oberen Bild ist wie selbstverständlich abgebildet, dass die DNS verantwortlich für ein Merkmal (Farbe der Samen) verantwortlich ist. Woher weiß man das? Am Anfang der Thematik "Genetik" haben wir einen Versuch analysiert, der zeigen konnte, dass der Zellkern die Informationen über die Merkmale einer Zelle enthält.
- Sucht diesen Versuch in eurem Skript (es war ein Arbeitsblatt)!
- Lest euch die entsprechende Einheit gut durch!
- Legt dann das Skript beiseite!
- Skizziert den Versuch nun (mit Worten, nicht mit "Skizzen")! Am besten macht ihr das tatsächlich schriftlich. Ihr könnt es auch jemandem (von mir aus auch einem Gegenstand in eurem Zimmer) erzählen. Aber bitte bildet ganze, sinnvolle Sätze! Zum Skizzieren eines Versuchs gehört: Der Versuchsaufbau, das Ergebnis, die Interpretation des Ergebnisses soweit möglich.
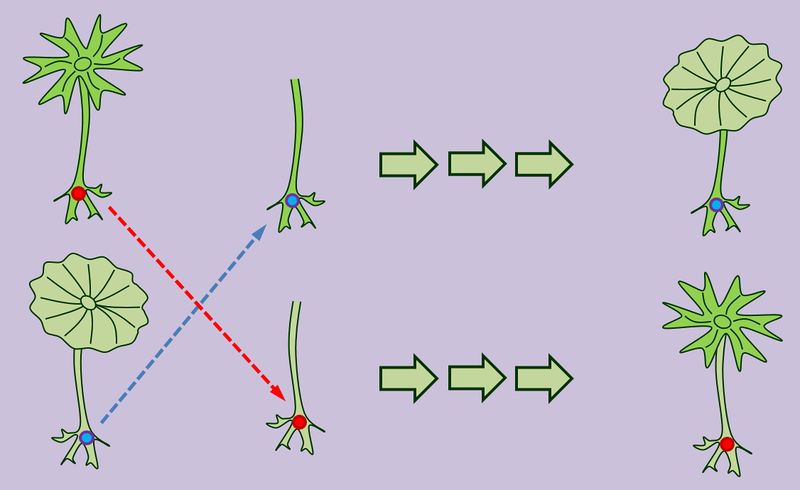
- Versuchsaufbau: Man verwendet verschiedene Arten von Acetabularia. Das sind einzellige Grünalgen, die sich vor allem in der Form ihres Hutes unterscheiden. Eine typische Eigenschaft dieser Algen ist das Nachwachsen des Hutes, wenn man ihn abschneidet. die Hüte zweier verschiedener Acetabularia-Arten wurden entfernt und die Zellkerne, die im Rhizoid sitzen vertauscht.
- Ergebnis: Es wächst (nach einigen Zwischenformen) die Hut-Form, die zum transplantierten Zellkern passt.
- Schlussfolgerung: Der Zellkern enthält die Informationen über die Merkmale der Zelle.
Damit könnte man sich eigentlich zufrieden geben. Fachlich hätte man dann aber etwas übersehen. Warum belegen die Versuch mit Acetabularia NICHT, dass die DNS die Informationen über die Merkmale einer Zelle enthalten?
Bei Atecabularia wird der Zellkern ausgetauscht. Im Zellkern befindet sich nicht nur DNS. Die Informationen über die Merkmale könnten daher auch an ein anderes Medium gekoppelt sein, dass im Zellkern vorkommt, z.B. Proteine oder RNA.
Einen tatsächlichen Beleg dafür, dass die DNS der Träger der Erbinformation sein muss lieferten die Versuche von Oswald Avery 1944. Dessen Versuche waren eine Weiterentwicklung von Versuchen, die Frederik Griffith 1928 durchführte. Betrachten wir zunächst diese.
- Beschreibt mit Worten (wie oben: Am besten schriftlich oder jemandem laut in ganzen Sätzen erklären) die folgenden Abbildungen Schritt für Schritt und versucht so weit es geht die dargestellten Ergebnisse auch zu interpretieren (also eine Begründung dafür zu finden)!
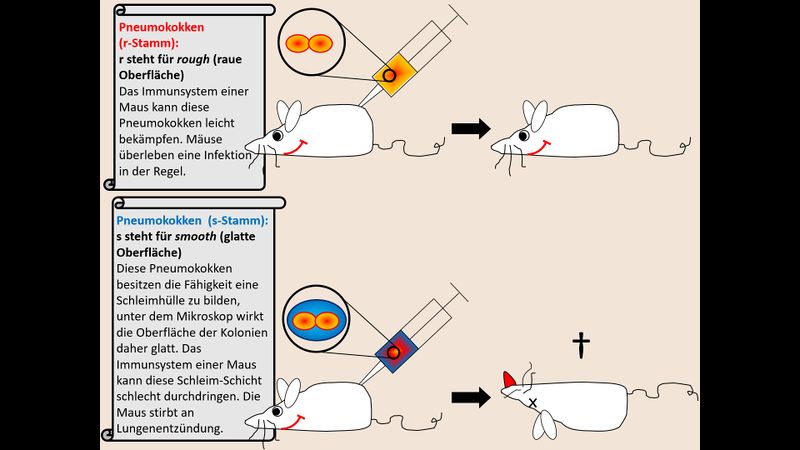
Mäuse werden mit verschiedenen Streptokokken infiziert. Man unterscheidet Streptokokken vom r-Stamm und vom s-Stamm. Diese unterscheiden sich in ihrem Aussehen unter dem Mikroskop (daher der Name), molekularbiologisch besitzen die Bakterien des s-Stamms eine Schleimhülle um ihre Zellen.
Eine Infektion mit r-Stamm-Pneumokokken ist für die Mäuse unproblematisch, bei der Infektion mit s-Stamm-Pneumokokken sterben sie
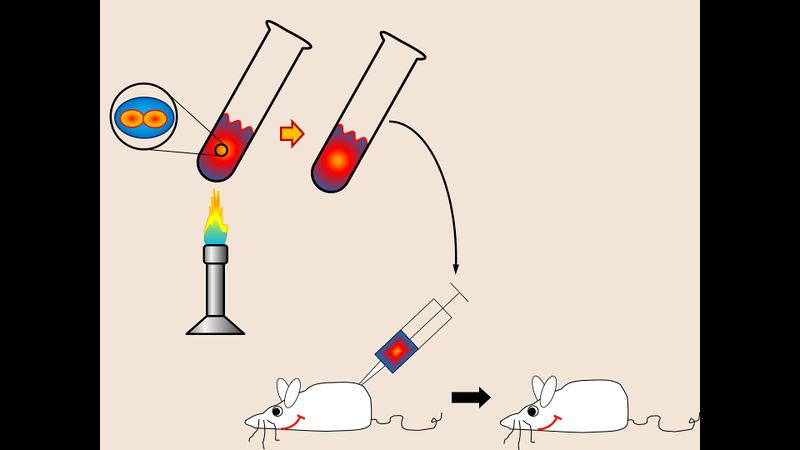
Erhitzt man die s-Stamm-Pneumokokken, verlieren Sie ihre tödlich Wirkung. Das ist verständlich, da durch das starke Erhitzen die Bakterien abgetötet werden und nicht mehr lebensfähig bzw. vermehrungsfähig sind.
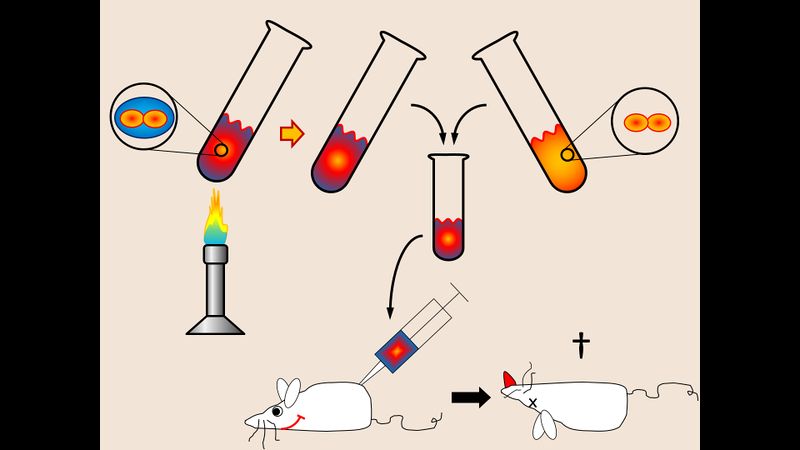
Bringt man abgetötete s-Stamm-Pneumokokken mit lebenden r-Stamm-Pneumokokken in Kontakt, so führt die Infektion einer Maus mit dieser Kombination zu ihrem Tod.
Griffith deutete die Ergebnisse seines Versuchs nicht ganz korrekt. Wie würdet ihr dieses Versuchsergebnis erklären?
R-Stamm-Pneumokokken sind nicht tödlich, weil das Immunsystem der Maus über die Oberfläche der Pneumokokken-Zellen eine leichte Angriffsmöglichkeit hat (s. Blutgruppen, Antikörper, Verklumpung). s-Stamm-Pneumokokken "verstecken" ihre Oberfläche in der Schleimschicht und sind so für das Immunsystem der Maus quasi nicht "sichtbar".
Prinzipiell sind nun zwei Szenarien denkbar: Die abgestorbenen s-Stamm-Pneumokokken werden durch die r-Stamm-Pneumokokken wieder zum Leben erweckt... Das ist jedoch nicht möglich, Pneumokokken-Zombies gibt es nicht. Die zweite Möglichkeit: Der Informationsträger, der bei den s-Stamm-Pneumokokken dafür verantwortlich ist, dass sich eine Schleimhülle bildet ist noch da! - Die s-Stamm-Pneumokokken haben sich ja nicht in Luft aufgelöst, sie sind nur tot. Irgendwie muss der Träger der Information "Mach-Schleim" noch vorhanden sein und in die Erbinformation der r-Stamm-Pneumokokken übergegangen sein.
Tatsächlich ist genau das passiert: Die Pneumokokken können DNS aus dem sie umgebenden Medium aufnehmen und in ihre eigene DNS einbauen. Der Vorgang nennt sich Transformation.
Avery verfeinerte den Versuch nun so, dass das eingangs beschriebene Dilemma (was genau im Zellkern ist denn jetzt Träger der Erbinformation: DNS, Proteine, RNS?) umgangen werden konnte. Beschreibt die Versuchsreihe und das Ergebnis!
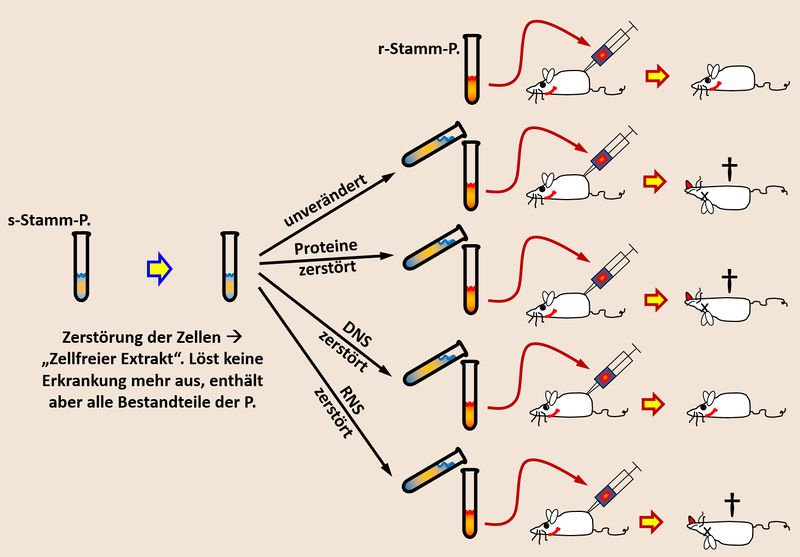
- Versuchaufbau: Avery stellte einen zellfreien Extrakt von s-Stamm-Pneumokokken her. Dieser löst zwar keine Erkrankung mehr aus, enthält aber noch alle Bestandteile. Diesen zellfreien Extrakt mischte er mit lebenden r-Stamm-Pneumokokken, wobei er jedoch in verschiedenen Ansätzen verschiedene Bestandteil (auf chemischem Wege) zerstörte: Einmal die DNS, einmal die Proteine und einmal die RNS.
- Ergebnis: Die Mäuse überleben eine Infektion mit dem Gemisch aus r-Stamm-Pneumokokken und s-Stamm-Bestandteilen, wenn die DNS zerstört wurde.
- Schlussfolgerung: Die DNS muss die Information über den Bau der Schleimkapsel enthalten haben und hat sich damit als Träger der Erbinformation erwiesen.
Ich habe kein wahnsinnig schönes Video gefunden, das mich persönlich anspricht, aber wer lieber jemandem "Zuhören" will und nicht bloß immer "Lesen", der kann sich das folgende Video zu den Versuchen von Griffith und Avery anschauen:
O.k., Zeit sich die DNS etwas genauer anzuschauen. Schaut das folgende Video:
Beantwortet nun folgende Fragen:
- Erwin Chargaff experimentierte zu Zeiten von Griffith und Avery ebenfalls mit DNS. Hauptsächlich zerlegte er die DNS von verschiedenen Lebewesen in ihre Bestandteile und bestimmte die enthaltene Menge. In eurem Buch auf der S. 61 oben rechts ist eine Abbildung, die im Prinzip einen Teil seiner Ergebnisse zeigte. Interpretiert diese Abbildung!
- Die Grafik zeigt das Verhältnis der vier in der DNS vorkommenden Basen bei verschiedenen Lebewesen.
- Bei unterschiedlichen Lebewesen ist das Verhältnis der Basen unterschiedlich
- Stets gilt jedoch: Die Basen A und T kommen immer im gleichen Verhältnis vor ebenso wie die Basen G und C
- Die Begründung für diesen Effekt ist die Komplementarität der beiden DNS-Einzelstränge: Die Basen Adenin und Thymin können über Wasserstoffbrücken eine stabile Bindung eingehen, die Basen Guanin und Cytosin ebenso. Für jede Adenin-Base auf dem einen Strang muss auf dem anderen eine Thymin-Base enthalten sein. Daher ist die Anzahl dieser beiden Teilchen immer gleich. Diese Begründung gilt auch für die Basen Guanin und Cytosin.
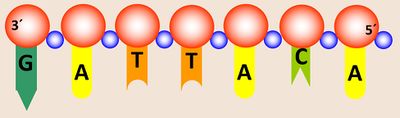
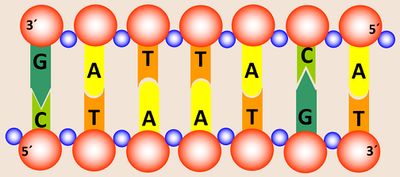
- Ein DNS-Einzelstrang soll folgende Sequenz enthalten: 3´-GATTACA-5´. Wie lautet die entsprechend komplementäre Sequenz des gegenüberliegenden Stranges?
Hefteintrag ist online.
Distanzunterricht, Montag 15.02.
Zu bearbeiten: Am besten heute.
Zur Bearbeitung benötig ihr das Schulbuch, einen Zettel, Stift, eine Internetverbindung, um Videos zu schauen. Und Ruhe!
Die Bearbeitungszeit sollte unter 90 Minuten liegen.
Die optionalen Inhalte sind nicht in die Bearbeitungszeit mit einberechnet.
Die meisten von den bisher im Unterricht aufgetretenen Erbkrankheiten haben ihre Ursache in einem defekten Gen, also einem kleinen Abschnitt DNA in einem Chromosom. In dieser Einheit soll es um eine Gruppe von Erbkrankheiten gehen, bei denen eine andere Ursache eine Rolle spielt. Betrachtet dazu das folgende Karyogramm eines Menschen:
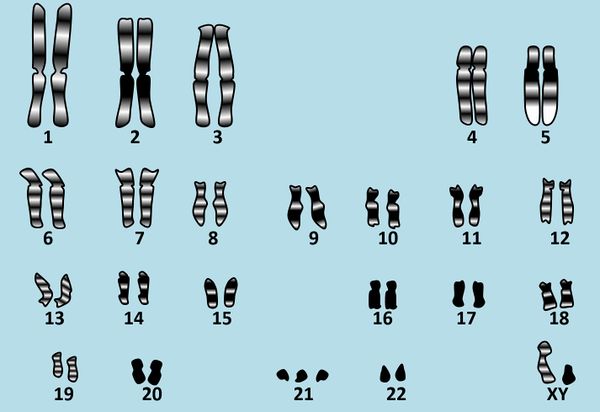
- Beschreibt dieses Karyogramm!
Es handelt sich um das Karyogramm eines Mannes, da bei den Gonosomen ein X- und ein Y-Chromosom vorliegen. Zusätzlich ist das 21. Chromosom dreimal vorhanden.
Bevor wir uns mit den Konsequenz dieser Abweichung beschäftigen zunächst ein Blick auf die Ursachen: Wie kommt es dazu, dass hier eine Trisomie 21 vorliegt (tri = drei, soma = das Körperchen; gemeint ist also: das dreifache Vorliegen des 21. Körperchens/Chromosoms).
Das folgende Video ist auf englisch. Das macht aber nichts. Wenn ihr gut in Englisch seid, könnt ihr versuchen den gesprochenen Text zu verstehen. Wenn nicht, konzentriert euch auf die Animationen und die geschriebenen Fachbegriffe. Und ignoriert bitte die Kommentare...
Schaut bitte lediglich bis zum Zeitindex 3:41 min! Der restliche Teil des Videos kann später freiwillig angeschaut werden:
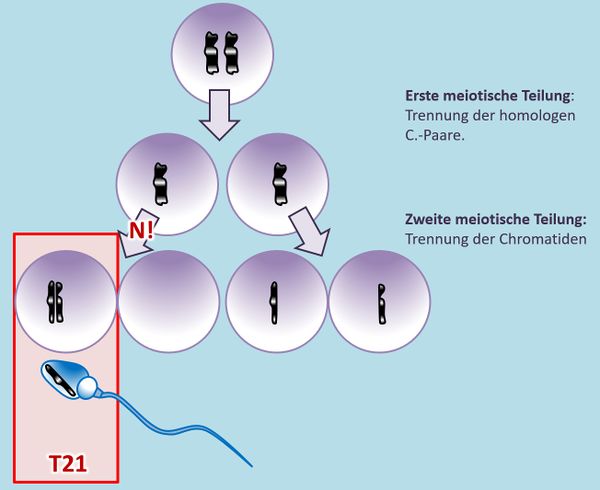
Zusammenfassung: Ursachen für eine Trisomie 21 sind also Nondisjunction-Ereignisse, in der Regel gekennzeichnet durch das Symbol N!.
- Beschreibe mit Worten, was das bedeutet!
Nondisjunction bedeutet "Nicht-Trennung". Es handelt sich um einen Vorgang, der in der Meiose, also bei der Bildung von Geschlechtszellen, auftreten kann. Bei einem N! in der ersten meiotischen Teilung werden die homologen Chromosomen nicht voneinander getrennt, bei einem N! in der zweiten meiotischen Teilung werden die Chromatiden nicht voneinander getrennt. In beiden Fällen kommt es zu Geschlechtszellen (Eizellen, Spermien), die von einem Chromosom ein Chromatid zu viel oder zu wenig haben.
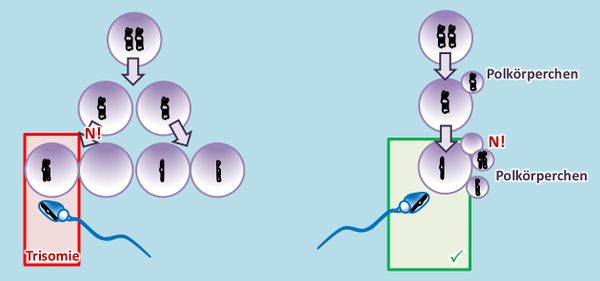
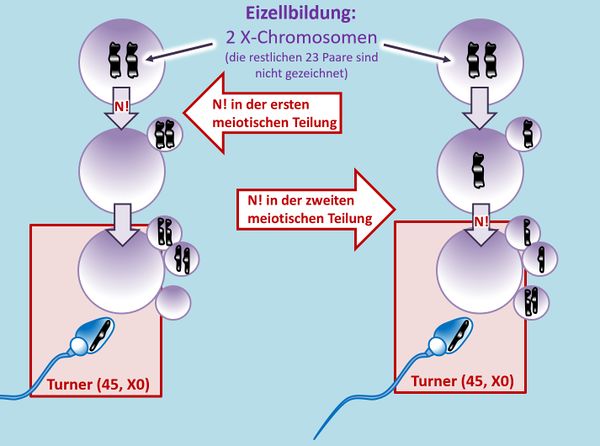
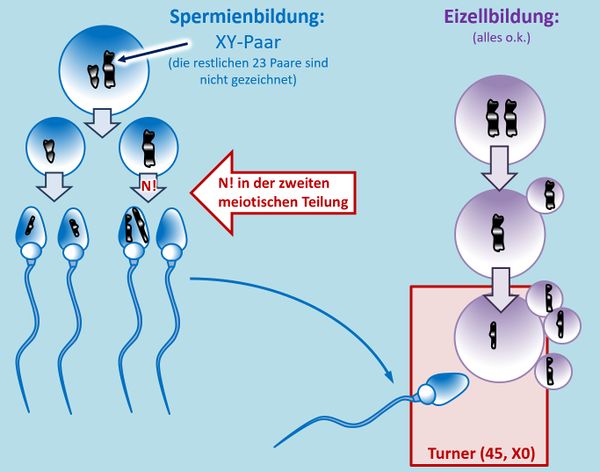
Ihr sollt dieses Phänomen selbst noch einmal zeichnen. Betrachtet eine hypothetische Urkeimzelle mit nur einem Chromosomenpaar. Zeichne die Schritte, die durch ein N! in der zweiten meiotischen Teilung zu einer Eizelle führen, die nach der Befruchtung mit einem "normalen" Spermium in einer Trisomie mündet.
Im Film wurde auch bereits auf die Monosomien eingegangen. Im oben gezeichneten Beispiel würde eine Monosomie entstehen, wenn die zweite Eizelle von links durch ein "normales" Spermium befruchtet werden würde. Monosomien (also Zustände, bei denen von einem Chromosom nur eine Kopie in der Zelle vorliegt) sind immer tödlich. Eine befruchtete Eizelle mit einer derartigen Ausstattung an Chromosomen entwickelt sich nicht oder kaum zu einem Fötus bzw. Embryo heran. Eine Ausnahme existiert, auf die wird später eingegangen: Menschen mit 44 normalen Autosomen aber nur einem X-Chromosom. Man könnte von einer "Monosomie 23" sprechen (tut man aber nicht).
In eurem Buch auf der Seite 92 sind die Auswirkungen einer Trisomie 21, auch bekannt unter dem Namen Down-Syndrom, aufgeführt. Lest diese Seite!
Schließt jetzt das Buch und beantwortet folgende Fragen:
- Woher hat das Down-Syndrom seinen Namen?
- Was ist ein Polkörperchen und was hat das mit Trisomien zu tun? (Was ein Polkörperchen ist, steht nicht hier im Text, wurde aber früher bereits besprochen.)
- Was für ein Faktor beeinflusst die Häufigkeit des Auftretens von N! ?
- Der Name stammt von dem Arzt, der die Symptome als erstes dokumentiert hat: John Langdon Down.
- Bei der Bildung von Eizellen in der Meiose entwickelt sich immer nur eine Tochterzelle zur Eizelle weiter, die restlichen bleiben als deutlich kleineres Polkörperchen an der großen Eizelle kleben. Im Film bzw. auch in der oberen Abbildung ist dieser Prozess nicht dargestellt. Dort sieht es so aus, als würden aus einer Urkeimzelle vier gleichwertige Zellen entstehen. Das ist aber Absicht. Es ging in diesen Darstellungen einfach darum, die prinzipiellen Möglichkeiten aufzuzeigen. Zum Zusammenhang mit Trisomien: Wenn ein N! stattfindet, kann es sein, dass die fehlerhafte Zelle sich zufällig zu einem Polkörperchen entwickelt. Dann hat das keine Auswirkungen auf das Kind.
- Je älter eine Frau, umso größer ist die Wahrscheinlichkeit für ein N!.
Früher war es üblich bei der Besprechung des Down-Syndroms alle möglichen Symptome aufzuzählen. Dadurch entstand der Eindruck, Menschen mit Trisomie 21 sind immer hochgradig behindert. Das trifft jedoch nicht zu. In vielen Fällen sind nur wenige der möglichen Symptome, teilweise auch nur sehr schwach ausgeprägt. Vor allem wenn die Trisomie 21 früh entdeckt wird, z.B. durch pränatale Diagnostik, können frühkindliche Fördermaßnahmen dazu führen, dass sich Kinder mit Trisomie 21 nahezu normal entwickeln.
- Wiederholung: Beschreibe eine pränatale Diagnose-Möglichkeit, um Trisomie 21 festzustellen!
z.B. Amniozentese (Fruchtwasseruntersuchung): Entnahme von Fruchtwasser durch die Bauchdecke der schwangeren Frau. Das Fruchtwasser enthält immer auch kindliche, abgestoßene (oder andere) Zellen. Aus diesen kann ein Karyogramm angefertigt werden. Eine Trisomie wäre dann erkennbar
Es gibt eine ganze Reihe von Dokumenten (Filme etc.), die zeigen, dass Menschen mit Down-Syndrom eben nicht "weniger intelligente Behinderte" sein müssen. Die folgende Seite gehört zur regelmäßig erscheinenden Zeitschrift "Ohrenkuss", die ausschließlich von Menschen mit Down-Syndrom produziert wird. Wer will, kann darin stöbern:
- Link zur Seite des Magazins "Ohrenkuss": Hier klicken
N! kommen tatsächlich sehr häufig vor. In den meisten Fällen entwickeln sich aus befruchteten Eizellen, die Trisomien enthalten aber keine Embryonen oder Föten. Warum ein zusätzliches Chromosom in den meisten Fällen letal (tödlich) ist, kann an dieser Stelle nicht geklärt werden, auch weil noch nicht alle Prozesse vollständig verstanden sind. Letztlich liegt es wohl an einem Ungleichgewicht von Enzymen, die entstehen.
Wenn ihr Schwierigkeiten mit dieser Art von Themen habt (Behinderungen, Tod, Ausgrenzung), empfehle ich euch diesen Punkt wirklich zu überspringen oder jemanden dazu zu holen. Im Unterricht kann man hier bestimmte Ängste, Vorurteile etc. abfangen, im Moment müsst ihr aber alleine klarkommen.
Verschafft euch auf den folgenden WIKIPEDIA-Seiten einen Überblick über die Symptome, Lebenserwartung und Behandlungsmöglichkeiten bei:
- Trisomie 18 (Edwards-Syndrom) Hier klicken
- Trisomie 13 (Pätau-Syndrom) Hier klicken
Die bisher besprochenen numerischen Chromosomenabberationen (zahlenmäßige Abweichung von der Chromosomen-Anzahl) betrafen ausschließlich die Autosomen. Es können aber auch die Gonosomen betroffen sein. Man unterscheidet folgende Typen:

Lest im Buch die S. 99 und bearbeitet die Aufgaben 1 - 4!
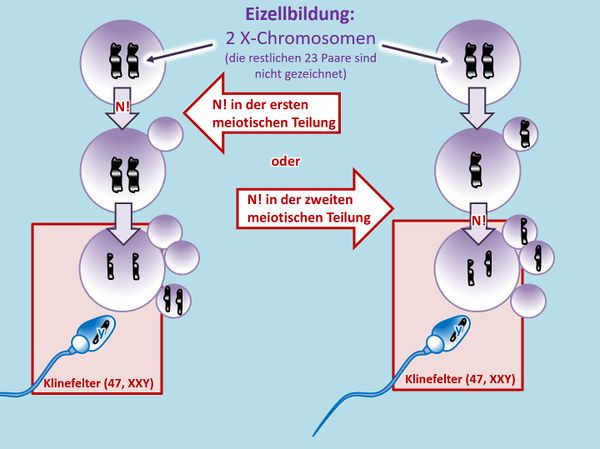
Nachdem in der Aufgabe die Rede davon ist, dass die beiden X-Chromosomen genetisch völlig identisch sind, kommt hier eigentlich nur die rechte Variante in Frage! Bei der linken Variante wären die beiden X-Chromosomen genetisch unterschiedlich. (Das eine Chromatid in der Eizelle stammt von dem Chromosom, welches die Frau von ihrem Vater hat; das andere Chromatid stammt von dem Chromosom, welches die Frau von ihrer Mutter hat.)
Vermutlich habt ihr keine Lösung gefunden und trotzdem auf den Anzeigen-Butten geklickt...
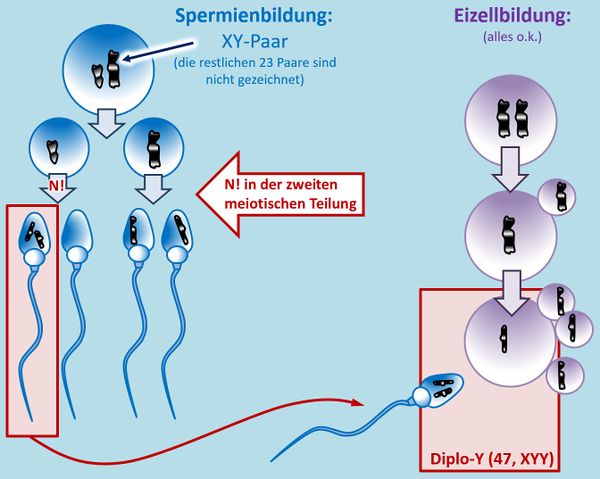
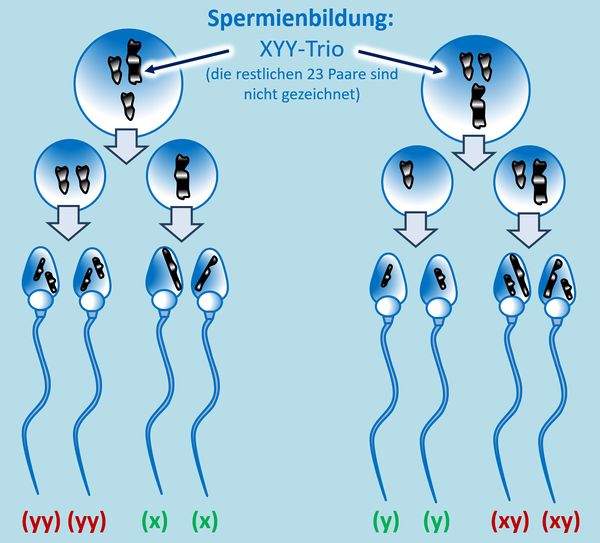
Hm. Aber gut, was solltet ihr auch sonst machen? O.k., hier ein Tipp: Bei einer ungeraden Anzahl an Chromosomen in der Zelle taucht in der 1. meiotischen Teilung ein Problem auf: Normalerweise ordnen sich hier die homologen Paare nebeneinander an, so dass jeweils ein ganzes Chromosom vom Spindelfaserapparat zum einen oder anderen Zellpol gezogen wird. Bei einer ungeraden Anzahl bleibt aber ein Chromosom übrig. Dieses wird wahlweise entweder zum einen oder anderen Zellpol gezogen. In diesem speziellen Fall muss man auch noch folgende Fälle unterscheiden: Bei einem normalen Mann ordnen sich in der 1. meiotischen Teilung das X- und das Y-Chromosom nebeneinander an und werden dann getrennt. Liegen allerdings wie hier zwei Y-Chromosome (und ein X-Chromosom) vor, könnte es auch sein, dass sich in der 1. meiotischen Teilung die beiden Y-Chromosome in der Äquatorialebene nebeneinander anordnen und das X-Chromosom keinen Partner hat.
Probiert es jetzt erneut!
Distanzunterricht Montag, 08.02.
Zu bearbeiten: Am besten heute. Ihr könnt gerne zusammen an dieser Einheit arbeiten, indem ihr euch über ein Kommunikations-Tool eurer Wahl Kontakt aufnehmt.
Zur Bearbeitung benötig ihr das Schulbuch, einen Zettel und einen Stift.
Die Bearbeitungszeit wird 90 Minuten sicher nicht überschreiten.
Die optionalen Inhalte sind jedoch nicht in die Bearbeitungszeit mit eingerechnet.
Wie in der letzten Unterrichts-Stunde angedeutet hat das Analysieren von Stammbäumen eine ganz praktische Bedeutung: Man kann damit z.B. die Wahrscheinlichkeit ableiten, mit der ein Kind geboren wird, das Träger einer Erbkrankheit ist.
- Lest zunächst auf S. 109 in der linken Spalte die Absätze 1, 2 und 4
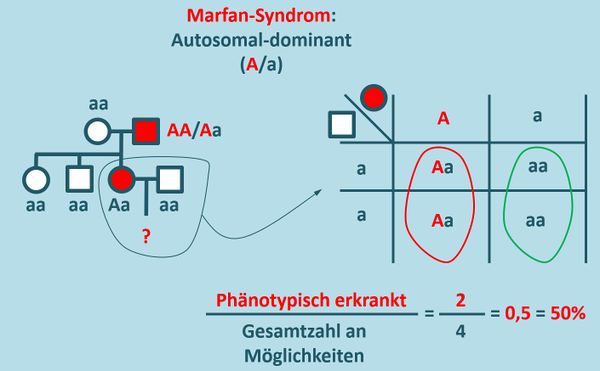
- Zeichnet unter Angabe aller möglichen Genotypen einen Stammbaum für eine Familie, in der ein autosomal-dominant vererbtes Merkmal (z.B. das Marfan-Syndrom) vorkommen soll: Ein gesunder Mann heiratet eine Frau, die das Marfan-Syndrom zeigt. Die beiden Geschwister der Frau (ein Bruder, eine Schwester) sind phänotypisch unauffällig, ebenso wie die Mutter. Der Vater litt allerdings auch am Marfan-Syndrom.
- Berechnen Sie die Wahrscheinlichkeit dafür, dass ein Kind des eingangs genannten Paares das Marfan-Syndrom aufweisen wird.
- Es gibt einen berühmten Fall von einer Frau, die das Marfan-Syndrom zeigt. Wer will, kann Lizzie Velásquez recherchieren.
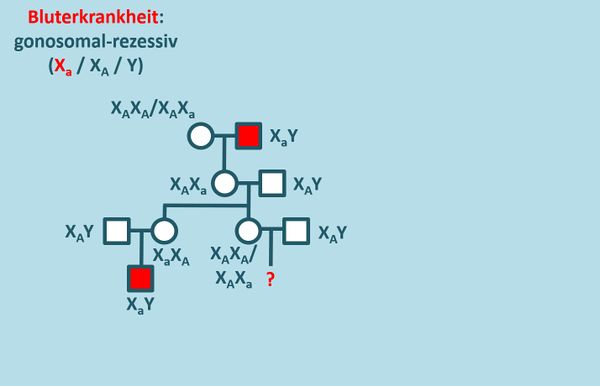
Die Aufgabe 1 auf der S. 110 beschäftigt sich mit einer Familie, in der die Bluterkrankheit vorkommt. Diese wird gonosomal-rezessiv vererbt. Löst die Aufgabe mit folgender Änderung: ... Ermitteln Sie über einen Stammbaum der Familie das Risiko, mit dem ein Kind dieser Frau ebenfalls bluterkrank sein wird.
- Zeichnet zunächst den Stammbaum unter Angabe aller möglichen Genotypen!
- Berechnet jetzt die Wahrscheinlichkeit für ein Kind, das an der Bluterkrankheit leidet
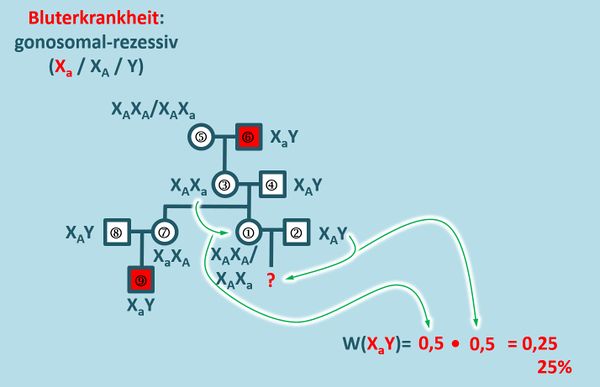
Die Gesamtwahrscheinlichkeit ergibt sich aus der Multiplikation der Einzelwahrscheinlichkeiten. Fälle, die zu 100% eintreten, brauchen nicht berücksichtigt werden (weil sie in der Multiplikation als Faktor 1 auftreten würden und das Ergebnis nicht verändern).
- Betrachten wir zunächst die Mutter 1:
Sie könnte die den Genotyp XAXa oder XAXA besitzen. Dies hängt von ihrer Mutter (3) ab. Von ihrem Vater (4) erhält sie in jedem Fall XA. Xa kann der Vater nicht besitzen, sonst wäre er krank.
Das die Mutter (3) tatsächlich Konduktorin ist (Genotyp XAXa) ist aufgrund ihrer Eltern (5) und (6) sicher.
Mit welcher Wahrscheinlichkeit trägt die Frau (1) nun den Genotyp XAXa?
Es gibt prinzipiell zwei Möglichkeiten: Entweder sie erhält von ihrer Mutter (3) XA oder Xa. In einem von zwei Fällen also. Das entspricht einer Wahrscheinlichkeit von 50% (oder 0,5).
- Betrachten wir nun den Vater (2):
Nachdem er gesund ist, muss er den Genotyp XAY besitzen. Wenn er das Chromosom XA an sein Kind weitergibt, wird es eine Tochter, die gesund ist. Gibt er das Y-Chromosom weiter, wird es ein Junge. Ob dieser krank ist oder nicht, hängt vom X-Chromosom der Mutter ab.
Mit welcher Wahrscheinlichkeit gibt der Mann (2) nun ein Y-Chromosom weiter?
Es gibt prinzipiell zwei Möglichkeiten: Entweder XA oder Y. In einem von zwei Fällen also. Das entspricht einer Wahrscheinlichkeit von 50% (oder 0,5).
- Beide Wahrscheinlichkeiten miteinander multipliziert ergibt eine Wahrscheinlichkeit von 25%, mit der ein krankes Kind (ein Junge) auf die Welt kommt.
Das letzte Beispiel zeigt auch, dass es bei rezessiv vererbten Merkmalen einen entscheidenden Unterschied macht, ob eine phänotypisch gesunde Person heterozygot ist, also den Genotyp Aa bzw. XAXa besitzt oder homozygot ist, also den Genotyp AA bzw. XAXA besitzt. Lange Zeit gab es keine Möglichkeit (außer in bestimmten Fällen über Stammbaum-Betrachtungen) zu testen, ob eine Person heterozygot ist. Inzwischen gibt es für einige Krankheiten gentechnische Nachweis-Methoden.
Ein schon etwas älterer "Heterozygoten-Test" nutzt eher die Prozesse im Stoffwechsel von Menschen aus.
- Lest auf S. 108 den Text über Phenylketonurie (PKU) (1. Absatz link + 2. und 3. Absatz rechts) und auf der S. 109 den Abs. 5 (rechte Spalte)
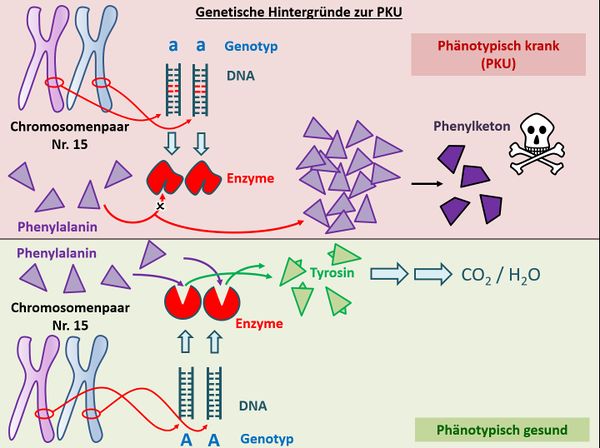
- Betrachtet anschließend das folgende Bild und beschreibt es mit eurem soeben erworbenen Fachwissen. Sprecht dabei laut! Am besten ihr holt euch jemanden dazu, der gerade Zeit hat, z.B. eure Eltern, die sich bestimmt wahnsinnig freuen werden! Wenn ihr das nicht möchtet, dann erzählt es wenigstens einem Gegenstand auf eurem Schreibtisch, laut!
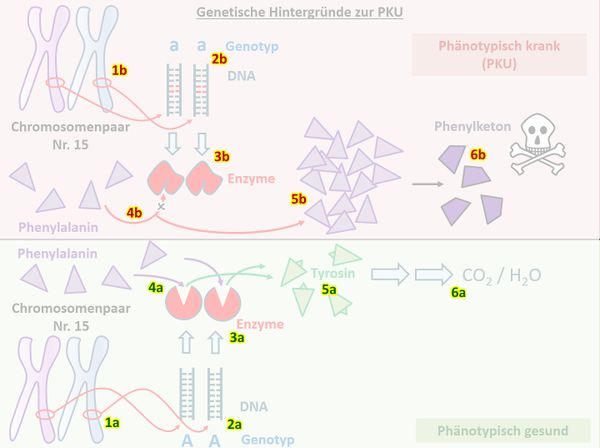
Z.B.: Menschen besitzen von jedem Chromosom ein homologes Paar. Auf diesen Chromosomen gibt es Orte, die z.B. für die sichtbare Ausprägung eines Merkmals mitverantwortlich sind. Diese Orte nennt man auch Gene (1a/1b). Die Gene bestehen aus DNA, die aber nicht immer gleich ist. Häufig gibt es verschiedene Varianten von DNA-Abschnitten, die in einem Gen sitzen (2a/2b). Diese Varianten heißen Allele. Im Normalfall sorgt ein Allel auf dem Chromosom Nr. 15 (das konnten ihr nicht wissen) für die Bildung des Enzyms Phenylalaninhydroxylase (3a), welches in der Lage ist, mit der Nahrung aufgenommenes Phenylalanin in Tyrosin umzuwandeln (4a). Dieses wird von anderen Enzymen, die hier nicht relevant sind, in CO2 und H2O zerlegt (5a, 6a).
Bei Menschen mit Phenylketonurie befindet sich auf dem entsprechenden Gen ein Allel, welches nicht zur Bildung des korrekten Enzyms führt (2b/3b). Mit der Nahrung aufgenommenes Phenylalanin kann nicht weiterverarbeitet werden (4b) und reichert sich im Körper an (5b). In einer Nebenreaktion entsteht Phenylketon (6b) was sich äußerst toxisch auf die Entwicklung von Nervenzellen auswirkt.
Wird die Krankheit nicht erkannt, entwickeln Kinder mit PKU schwerste Behinderungen. Diese Fehlentwicklung lässt sich einfach vermeiden, indem man eine strenge Diät einhält, bei der kein Phenylalanin in der Nahrung vorkommt.
- Recherchiert Lebensmittel, die viel bzw. kaum Phenylalanin enthalten!
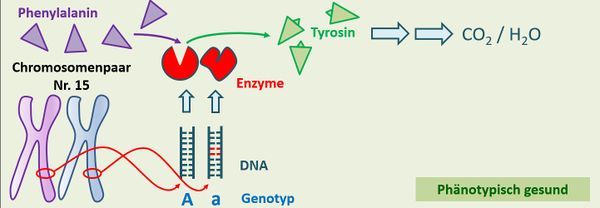
- Im Buchtext wurde bereits der Genotyp Aa angesprochen. Zeichnet diesen Fall nach dem gleichen Schema wie auf der Folie oben!
Der Heterozygoten-Test auf Phenylketonurie wird bei nahezu allen Neugeborenen durchgeführt und kann nach folgendem Muster erfolgen (heutzutage macht man das allerdings anders): Man spritzt einer Person Phenylalanin und misst im Anschluss regelmäßig den Tyrosin-Gehalt im Blut.
- Zeichne ein Diagramm, das die Tyrosin-Konzentration im Blut nach der Gabe von Phenylalanin in Abhängigkeit von der Zeit zeigt. Einmal für den Fall, dass die betroffene Person den Genotyp AA besitzt und mit einer zweiten Kurve den Genotyp aa.
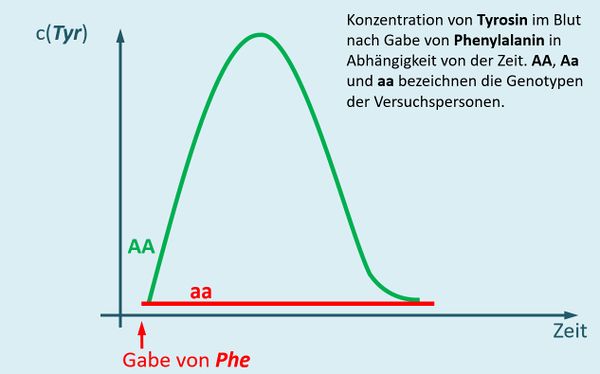
Bei Personen mit dem Genotyp AA werden zwei funktionstüchtige Enzyme gebildet, die Phenylalanin zu Tyrosin umwandeln. Das bedeutet, dass nach der Gabe von Phenylalanin der Tyrosin-Gehalt stark ansteigen muss. Tyrosin wird jedoch weiterverarbeitet, insofern fällt nach einiger Zeit der Tyrosin-Spiegel wieder.
Bei Personen mit dem Genotyp aa werden zwei funktionslose Enzyme gebildet. Phenylalanin wird nicht weiterverarbeitet, es taucht kein zusätzliches Tyrosin im Blut auf.
- Zeichne in das Diagramm nun den Verlauf ein, der sich ergeben sollte, wenn die betrachtete Person heterozygot (Genotyp Aa) ist.
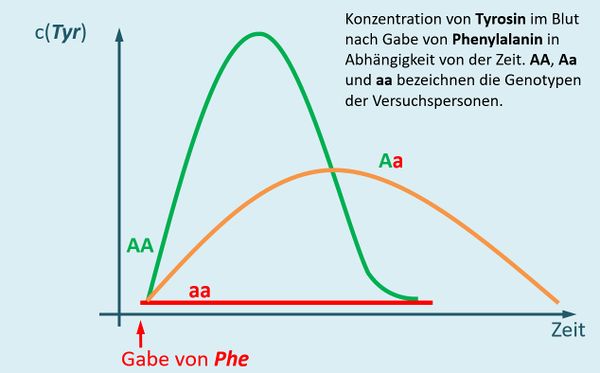
Personen mit dem Genotyp Aa bilden teilweise intakte, teilweise defekte Enzyme. Die intakten können Phenylalanin abbauen. Aber eben nicht so schnell im Vergleich zur Situation bei Menschen mit dem Genotyp AA, die doppelt so viele intakte Enzyme herstellen. Die Kurve steigt daher nicht so schnell, hält aber länger an.
Ende der ersten Stunde. Kurze Pause :) - Die zweite Hälfte wird kürzer.
- Eine detailliertere Übersicht über Pränatale Diagnostik bietet z.B. diese Seite: Familienplanung.de
Zu Beginn der Vererbungslehre haben wir einfach Fälle betrachtet. Zum Beispiel bei Erbsen: Die Farbe der Samen wurde von einem Gen bestimmt. Je nachdem welche Allelkombination vorlag, waren die Früchte gelb oder grün. Ähnlich war es bei den Farben der Blüten oder der Oberflächenbeschaffenheit der Samen (rund oder runzelig). Dieser Zusammenhang gilt jedoch nicht streng. Folgende Effekte treten auf:
- Polyphänie: Ein Gen sorgt nicht nur für die Ausprägung eines Merkmals am Körper, sondern es werden gleich ganz viele Merkmale beeinflusst. Bsp.: Das Marfan-Syndrom. Ein einziges defekten Allel sorgt hier für eine ganze Reihe von Veränderungen: Herzfehler, Augenfehler, Verlängerung der Gliedmaßen etc.
- Polygenie: Ein Merkmal wird von vielen Genen beeinflusst. Bsp.: Die Hautfarbe. Es gibt nicht ein Gen, welches die Hautfarbe bestimmt, sondern viele. Damit kann man sehr gut erklären, warum Menschen nicht einfach weiß, schwarz oder braun sind, sondern sehr viele Zwischenstufen denkbar sind.
- Modifikation: Ein Merkmal wird nicht (nur) von den Genen bestimmt, sondern ein Umweltfaktor sorgt für die Veränderung des Merkmals. Bsp.: Auch hier könnte man die Hautfarbe anführen. Jeder weiß, dass die Haut dunkler wird, wenn man sie der Sonne aussetzt. Der Umweltfaktor "Sonne" sorgt hier also für eine Veränderung des Merkmals "Hautfarbe".
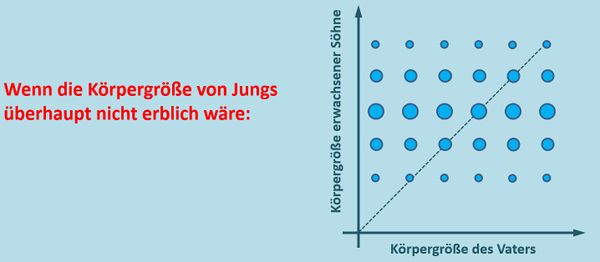
- Lest S. 100 und bearbeitet die Aufgabe 2 und Aufgabe 4!
- Aufgabe 2: Wenn die Körpergröße keinerlei genetischen Anteil hätte, dann dürften sich die Verteilungsmuster bei Männern verschiedener Größen nicht unterscheiden. Egal wie groß ein Mann ist, es müsste immer das selbe Verteilungsmuster bezüglich der Körpergröße seiner Söhne herauskommen. Die Abbildung zeigt nur eine Möglichkeit. Andere wären denkbar:
- Aufgabe 4: Im Schnitt sind die Söhne immer etwas größer als ihre Väter: Es befinden sich mehr und größere Punkte über der Mittelgeraden (heißt das Ding so? - Also die rote Linie in der Abbildung im Buch?). Wenn sich dieser Trend fortsetzt, werden Männer (im Schnitt) immer größere Söhne zeugen und langfristig werden Männer damit selbst immer größer.
- Zur Vererbung der Hautfarbe: Recherchiert die Zwillinge Leo und Ryan.
Beendet jetzt die Arbeit in Biologie und macht erst etwas anderes, geht... spielen?! Lest zu einem späteren Zeitpunkt die S. 100, 108-109 und bearbeitet die unten stehenden Aufgaben. Der Hefteintrag wurde bereits hochgeladen.
Wie schon erwähnt, werden heutzutage oft genetische Tests herangezogen werden, um Aussagen über mögliche Veranlagungen zu machen. Die Tests sind in den letzten Jahren immer billiger und genauer geworden.
- Lest auf der S. 109 den Abs. 3 über Chorea Huntington!
- Fasst die (eher ethischen) Probleme solcher Tests in diesem speziellen Fall zusammen!
z.B.: Mit einem positiven Test auf Chorea-Huntington könnte ein Konflikt entstehen: Eine Person, die sich ein Kind wünscht muss dann mit der Tatsache leben, dass eine 50%ige Wahrscheinlichkeit besteht, dass das Kind ebenfalls an dieser schweren, unheilbaren Krankheit erkranken wird.
Rosafarbene Hortensien (das sind Pflanzen. Wenn ihr die nicht kennt: Hier klicken) können mit einem einfachen Trick "umgefärbt" werden.
- Recherchiert eine Methode, rosafarbene Hortensien blau zu färben!
- Was hat das mit der letzten Unterrichtseinheit zu tun?
Die Blaufärbung wird (bei bestimmten Sorten) sowohl durch den pH-Wert des Bodens, als auch durch Aluminiumsalze im Boden verursacht. Das betrachtete Merkmal (Blütenfarbe) wird hier also nicht (nur) von Genen bestimmt sondern von einem Umweltfaktor. Insofern handelt es sich hier eine Modifikation.
Distanzunterricht Dienstag, 26.01.
Verbessert gegenseitig eure Hausaufgabe:
- Findet einen Partner, mit dem ihr zusammenarbeiten wollt. Wenn ihr keinen findet, könnt ihr eure Hausaufgabe auch alleine verbessern.
- Besorgt euch einen Rotstift!
- Macht ein Foto von eurer Hausaufgabe (Aufgabe 10 und Aufgabe 12 auf dem AB) und schickt sie an eure Korrekturpartnerin bzw. eurem Korrekturpartner!
- Druckt dann die Lösungen, die ihr jetzt erhalten habt aus (wenn ihr euch selbst korrigiert ist das natürlich nicht nötig)
- Solltet ihr keinen Drucker haben, könnt ihr das Foto auch in z.B. Powerpoint einfügen und dann mit dem Mauszeiger etwas hineinmalen.
- Geht zunächst auf dieser Seite Schritt für Schritt die Musterlösung durch und vergleicht mit der Lösung, die vor euch liegt. Verbessert mit roter Farbe die Fehler!
- Schickt eurem Korrekturpartner die Arbeit zurück (z.B. wieder ein Foto davon)
- Wenn ihr euch nicht selbst korrigiert habt, dürft ihr jetzt in grün die Korrektur korrigieren - sofern die Korrektur falsch ist oder ihr euch ungerecht behandelt fühlt.
- Ihr erhaltet um 13:50 Uhr einen Arbeitsauftrag über den Schulmanager. Als Antwort auf diesen Arbeitsauftrag schickt ihr mir eure (doppelt) korrigierte Lösung zurück!
Aufgabe 10: Berechne die Stoffmenge an Schwefeltrioxid, die man benötigt, um mit 100g Wasser vollständig zur Schwefelsäure zu reagieren.
Tipp 1: Es geht hier um die Stoffmenge und eine Masse ist gegeben. Finde die Gleichung, in der diese beiden Parameter vorkommen und die nützlich sein könnte!
Tipp 2: Direkt lässt sich die Stoffmenge von Schwefeltrioxid mit dieser Gleichung nicht berechnen. Das geht nur, wenn alle anderen Größen der Gleichung bekannt wären, aber die Masse von Schwefeltrioxid ist unbekannt. Über die chemische Gleichung kann man die Stoffmenge von Schwefeltrioxid jedoch mit der Stoffmenge des Wassers in Beziehung setzen: Wie verhält sich die Stoffmenge (also die Anzahl der Teilchen) von Schwefeltrioxid zu der Stoffmenge (also der Anzahl der Teilchen) von Wasser?
Tipp 3: Die Stoffmenge des Schwefeltrioxids lässt sich also durch die Stoffmenge des Wassers ausdrücken. Und die kann berechnet werden! Denn von Wasser hat man die Masse gegeben. Berechne zunächst die Stoffmenge des Wassers und schließe dann die Aufgabe ab!
Aufgabe 12: Im Labor soll Ammoniak aus den Elementen hergestellte werden (also aus H2 und N2). Es gibt noch exakt 22,4L Stickstoff. Welche Stoffmenge an Wasserstoff benötigt man, um den gesamten Stickstoff zu Ammoniak umzusetzen.
Tipp 1: Es geht hier um die Stoffmenge. Darüber hinaus ist ein Volumen gegeben. Finde die Gleichung, in der diese beiden Parameter vorkommen und die nützlich sein könnte!
Tipp 2: Direkt lässt sich die Stoffmenge von Wasserstoff mit dieser Gleichung nicht berechnen, es fehlt das Volumen, V(H2). Aber wie immer kann über die chemische Gleichung die Stoffmengen der beteiligten Stoffe in Beziehung zueinander setzen. Stelle die chemische Gleichung auf und drücke dann die Stoffmenge des benötigten Wasserstoffs in der Stoffmenge des Stickstoffs aus!
Tipp 3: Jetzt kann die Stoffmenge des Stickstoffs ausgerechnet werden und daraus die Stoffmenge des benötigten Wasserstoffs!
Distanzunterricht Dienstag, 26.01.
Die folgende Einheit soll auf das chemische Reaktionsverhalten von Alkoholen hinführen. Dazu ist eine Wiederholung von Unterrichtsstoff aus dem letzten Schuljahr nötig: Die Redoxreaktionen. Das folgende Video wiederholt alles, was für die folgenden Stunden wichtig ist. Es ist sehr ausführlich und schreitet langsam voran. Wahrscheinlich werden sich einige von euch langweilen. Aber auch diejenigen unter euch, die letztes Jahr unter Umständen große Probleme beim Aufstellen von Redoxgleichungen hatten: Das Video erklärt wirklich jeden einzelnen Schritt, den man machen muss. Das Video dauert fast 30min. Danach sollt ihr selbst weitere Aufgaben lösen. Dazu benötigt ihr ein Arbeitsblatt, welches ihr am besten schon vor dem Anschauen des Videos ausdruckt oder in einem separaten Fenster öffnet
- Hier gibt es das Arbeitsblatt: pdf-Datei
Nachdem ihr das Video geschaut habt, geht zur nächsten Aufgabe auf dem Arbeitsblatt über:
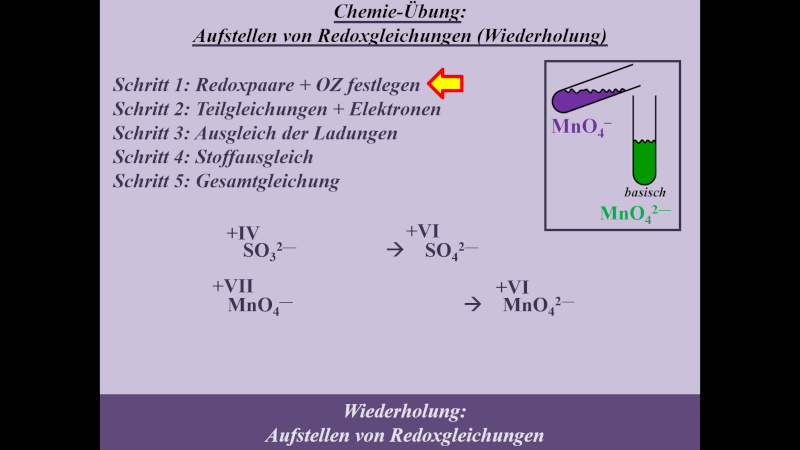
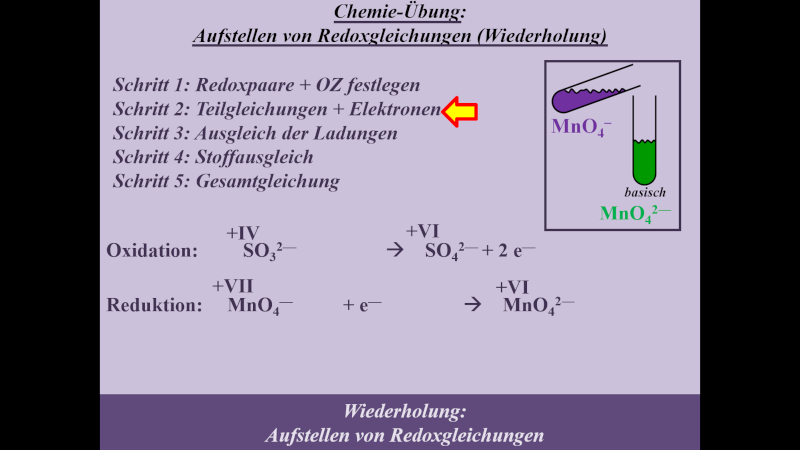
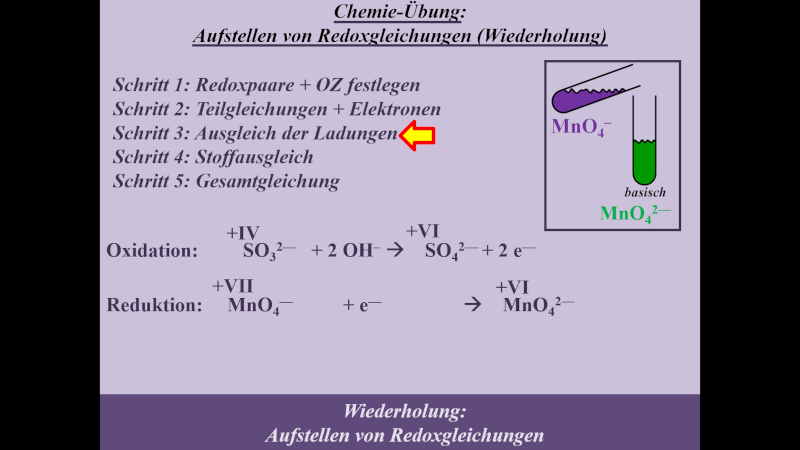
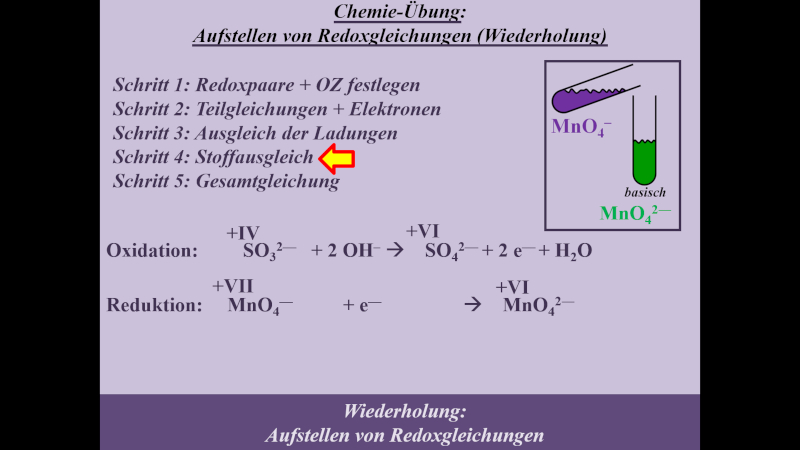
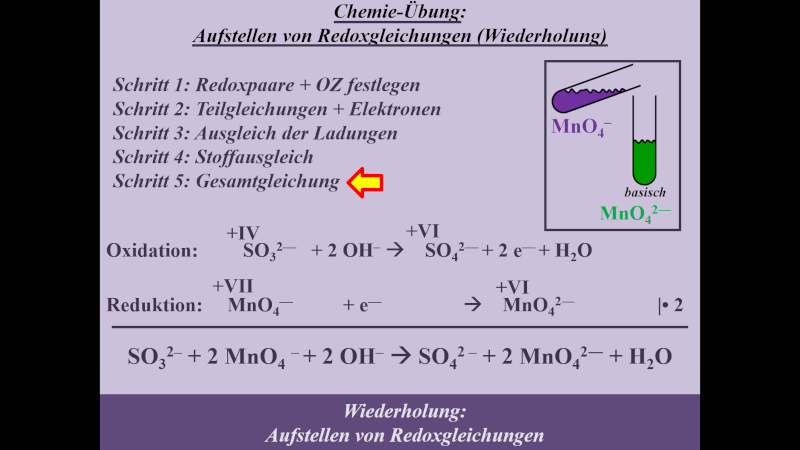
Die Reaktion von Permanganat (MnO4-) in basischer Sulfit-Lsg. zum grünen Manganat MnO42-. Im Video war häufiger zwar die Rede von gründen Mn6+-Ionen, es ist jedoch fachwissenschaftlich besser von MnO42- zu sprechen. Am Verfahren ändert sich dadurch nicht, nur das Ergebnis sieht anders aus.
Ich empfehle übrigens, dass ihr diese Aufgaben am besten mit einem Partner besprecht! - Ruft euch über ein Medium eurer Wahl zu einer kleinen Gruppen (2 - 4 Personen) zusammen und löst die folgende Aufgabe zusammen! Die letzte Aufgabe könnt ihr dann zur Überprüfung eurer Fähigkeiten alleine rechnen.
- Schritt 1: Redoxpaare und Oxidationszahlen festlegen
- Schritt 2: geflossene Elektronen festlegen
- Schritt 3: Ladungsausgleich
- Schritt 4: Stoffausgleich mit H2O
- Schritt 5: Gesamtgleichung aufstellen
In der nächsten Aufgabe geht es um die Bildung von braunem MnO2 in basischer Sulfit-Lsg. Wenn das Medium weder sauer noch basisch ist, dürft ihr euch entscheiden, mit welchen Ionen ihr den Stoffausgleich durchführt: entweder mit OH-- oder mit H3O+-Ionen.
Stellt zunächst die Redoxgleichung auf, indem ihr die H3O+-Ionen zum Ausgleichen verwendet!
Letzte Aufgabe: Betrachtet noch einmal die Bildung von braunem MnO2 in basischer Sulfit-Lsg. Verwendet diesmal aber zum Ausgleichen die OH--Ionen!<br
Distanzunterricht Donnerstag 20.01. Chemie
Mit der folgenden Einheit möchte ich in ein neues Stoffgebiet einsteigen. Schaut das folgende Video (17min.). Dort wird zunächst ein Versuch vorgestellt und die Beobachtung dann erklärt. Am Ende wird euch eine Aufgabe gestellt. Diese Aufgabe erledigt ihr bitte sofort im Anschluss an das Video. Dazu braucht ihr entweder ein Periodensystem oder ihr recherchiert die nötigen Infos direkt im Netz. Eure Lösung schickt ihr bitte in Form eines Fotos als Antwort auf den Arbeitsauftrag, den ich euch morgen um 08:10 Uhr über den Schulmanager anzeigen lasse.
Am Freitag machen wird eine Videokonferenz über MS Teams, um eure Ergebnisse sowohl in Bio als auch Chemie zu besprechen. Viel Erfolg!
Distanzunterricht Mittwoch, 19.01.
Ihr habt gestern sehr gut mitgearbeitet, daher heute eine etwas weniger anspruchsvolle Stunde. Mit dem folgenden Link gelangt ihr auf eine Seite von BR alpha (Ein TV-Sender, der zum Bayerischen Rundfunk gehört):
Trinkalkohol
Diese Seite besitzt sieben Unterkapitel, die ihr dort auf der rechten Seite der Homepage anklicken könnt:
1. Alkoholische Gärung in der Brauerei
2. Die alkoholische Gärung im Labor
3. Was macht Ethanol zu einem Alkohol
usw.
Zu jedem Kapitel gibt es einen kurzen Film (insgesamt ca. 35 Minuten) und darunter ein Quiz. Ich vertraue darauf, dass ich ihr euch heute alleine mit dieser Seite 45 Minuten beschäftigen könnt. Wer noch eine etwas anspruchsvollere Aufgabe braucht, bearbeitet bitte die folgende Aufgabe (Kontrolle in der nächsten Stunde am Di, 26.01.): pdf-Datei
Distanzunterricht Montag, 18.01.
Hallo 10d!
In der letzten Woche kam es vor allem in der 1. Stunde zu Problemen bei manchen Videokonferenzen. Höchstwahrscheinlich ist der Server überlastet, an dem Problem wird gearbeitet. Solange verzichte ich auf die Videokonferenz in der 1. Stunde, ich kann mit euch ja auch in der zweiten Stunde sprechen. Der Zeitplan für heute sieht also so aus:
- Um 07:50 Uhr solltet ihr einen Arbeitsauftrag über den Schulmanager erhalten haben, auf den ihr bis spätestens 08:15 Uhr antwortet. Das dient zunächst als Anwesenheitskontrolle. Erhalte ich keine Rückmeldung von euch, melde ich euch im Sekretariat als fehlend (was vermutlich dazu führt, dass eure Eltern informiert werden).
- Ihr arbeitet bis 09:00 Uhr alleine an diesem Arbeitsauftrag
- Dann starte ich eine BBB-Konferenz und wir besprechen, was ihr hier geschafft habt.
Für diesen Arbeitsauftrag benötigt ihr euer Buch und einen Zettel mit Stift.
In der letzten Stunde habt ihr die Stoffklasse der Alkohole kennengelernt. Überlegt noch einmal, welches Strukturmerkmal bei allen Stoffen dieser Klasse gleich ist!
Alkohole besitzen eine Hydroxygruppe: -OH
Diese funktionelle Gruppe im Molekül hat Auswirkungen auf die physikalischen Eigenschaften. Vergleicht die beiden Stoffe Propan-1-ol und Butan hinsichtlich ihrer Siedepunkte und begründet die Unterschiede so genau wie möglich! - Ihr müsst die Lösung zu dieser Aufgabe nicht ausführlich hinschreiben, aber notiert Stichpunkte, die ihr in einer Schulaufgaben-Situation genauer ausführen würdet. Eine solche Aufgabe könnte in einer schriftlichen Arbeit - je nachdem in welchem Zusammenhang sie gestellt wird - 10 BE oder mehr wert sein.
- Propan-1-ol hat den deutlich höheren Sdp.
- Um einen Stoff zum Sieden zu bringen, müssen die Teilchen (hier: Moleküle) eines Stoffes voneinander getrennt werden
- Je höher die Siedetemp. desto mehr Energie muss man anscheinend aufwenden, um die Moleküle voneinander zu trennen. Umso größer müssen offensichtlich die Zwischenmolekularen Anziehungskräfte sein.
- Beim Butan wirken als Zwischenmolekularen Kräfte nur die schwachen Van-der-Waals-Kräfte: Aufgrund von Fluktuationen in der Elektronenhülle kommt es zu spontanen Dipolen (mit geringen Partialladungen), die im Nachbarmolekül induzierte Dipole erzeugen. Die Stärke der Van-der-Waals-Kräfte hängt von der Größe bzw. der Masse des Moleküls ab.
- Beim Propan-1-ol wirken zwei weitere (starke bis sehr starke) Zwischenmolekulare Anziehungskräfte. Zum einen stellt die Hydroxy-Gruppe aufgrund der großen Elektronegativitätsdifferenz zwischen den C- und O- bzw. den H- und O-Atomen einen permanenten Dipol mit relativ starken Partialladungen dar. Hier ziehen sich die Moleküle stark an.
- Zum anderen ist das Molekül in der Lage Wasserstoffbrückenbindungen auszubilden: Sehr starke Anziehungskräfte zwischen Wasserstoffatomen, die an ein stark elektronegatives Element gebunden sind (hier der Fall: Das H-Atom der Hydroxygruppe) und den freien Elektronenpaaren von stark elektronegativen Element der 2. Periode (hier der Fall: Das O-Atom der Hydroxy-Gruppe)
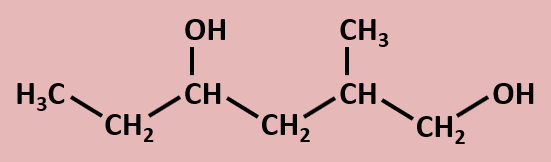
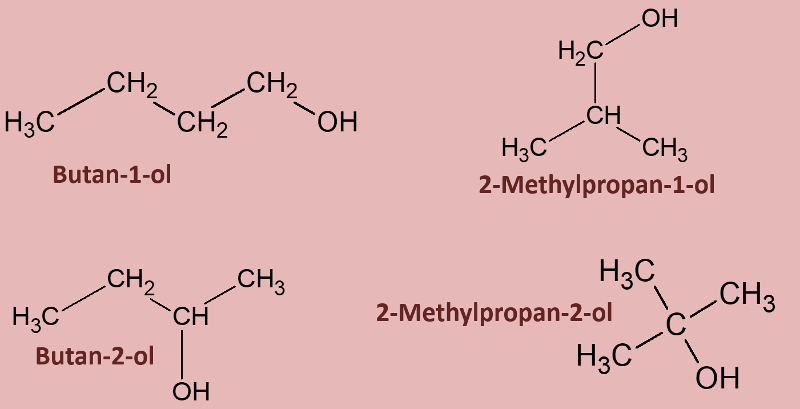
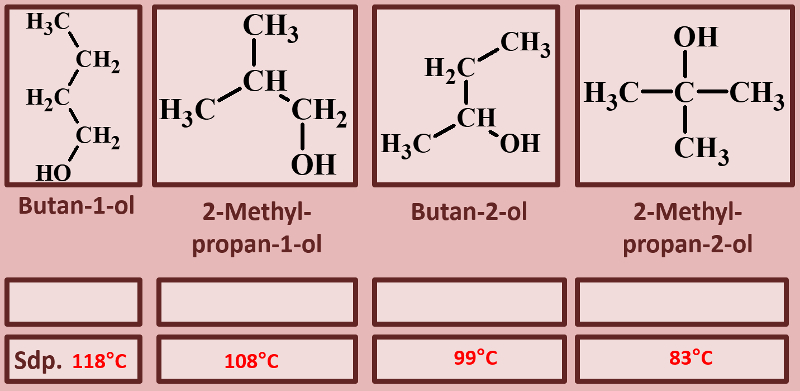
Betrachtet die folgenden Alkohole und deren Siedepunkte. Benennt zunächst die Alkohole! Stellt dann eine Hypothese auf, welche die unterschiedlichen Siedepunkte erklären könnte! Die Masse aller vier Alkohole ist gleich, außerdem sind es Konstitutionsisomere (gleiche Bausteine nur anders zusammengesetzt), daher ist es (bei eurem aktuellen Wissensstand) evtl. verwunderlich, warum sich die Siedepunkte überhaupt unterscheiden.
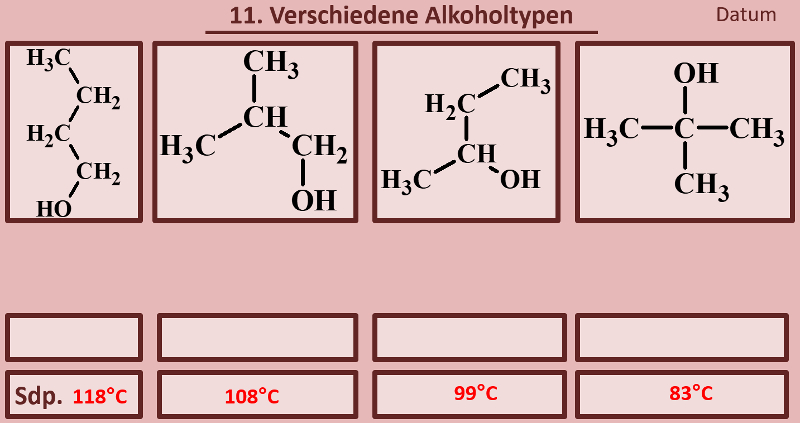
Warum Butan-1-ol den höchsten Siedepunkt im Vergleich zu den anderen hat solltet ihr bereits erklären können, wenn nicht, lest jetzt im Buch auf der Seite 36 den Abschnitt "Unterscheide beruhen auf Gemeinsamkeiten".
Butan-1-ol ist ein langgestrecktes Molekül. Dadurch entstehen große Kontaktflächen zwischen den Molekülen und das vergrößert die Van-der-Waals-Kräfte. Die anderen Alkohole sind verzweigt und damit "kugeliger", die Oberfläche wird also kleiner und die Van-der-Waals-Kräfte schwächer. Das führt zu geringeren Anziehungskräften zwischen den Molekülen und damit zu geringeren Siedepunkten.
Damit die Stelle des Moleküls, an denen ein permanenter Dipol vorliegt (also die OH-Gruppe) gut mit anderen OH-Gruppen wechselwirken kann, sollte sie möglichst "frei in der Gegend herum baumeln" oder "von allen Seiten zugänglich sein". Vergleicht unter diesem Gesichtspunkt die Situation bei den vier Molekülen!
Bei den verzweigten Alkoholen wird die OH-Gruppe teilweise von angrenzenden Methylgruppen abgeschirmt. Andere Moleküle können sich ihr also nicht so gut nähern. Daher funktioniert auch die Anziehung nicht so gut und die Siedepunkte fallen.
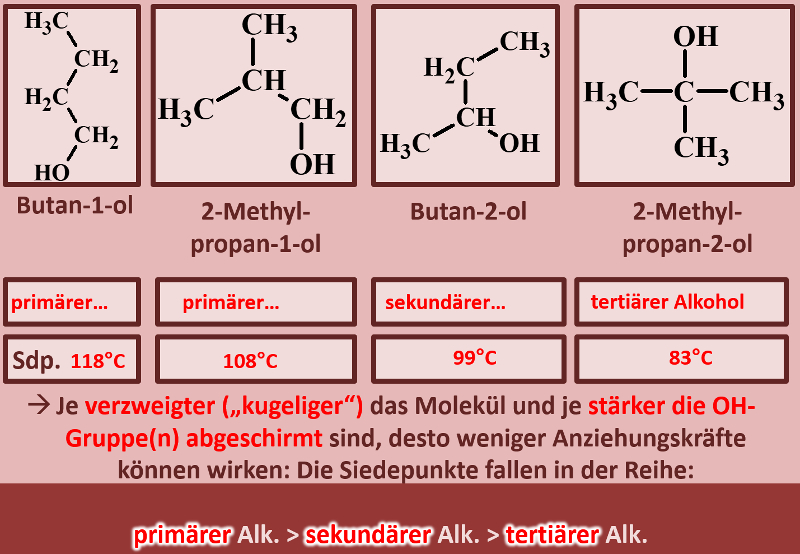
Noch ein Punkt: Je nachdem mit wie vielen C-Atomen das C-Atom, an dem die OH-Gruppe hängt, verbunden ist, spricht man von primären, sekundären oder tertiären Alkoholen. Ordne diese Begriffe den vier abgebildeten Molekülen zu und formuliere eine Aussage, in der ein Zusammenhang dieser Begriffe mit dem Siedepunkt hergestellt wird!
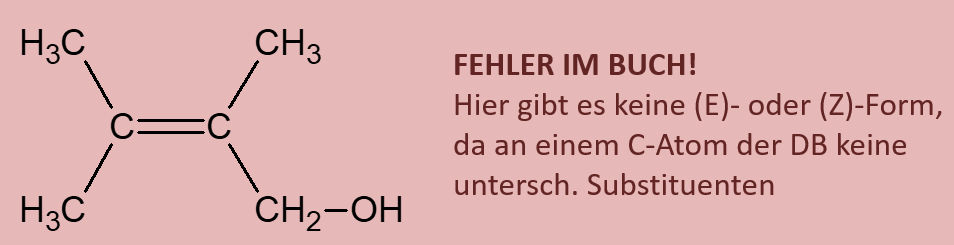
Ihr habt beim Einüben der Benennung von Alkoholen bereits gesehen, dass es Moleküle gibt, die mehr als eine Hydroxy-Gruppe enthalten. Was jedoch so gut wie nie vorkommt, sind Moleküle, bei denen zwei Hydroxygruppen an einem C-Atom hängen. Das folgende Bild stellt beispielhaft dar, was mit solchen Molekülen spontan passieren würde. Beschreibe das Bild mit eigenen Worten! (Und zwar wirklich, nicht nur in Gedanken. Sprich es laut aus!)
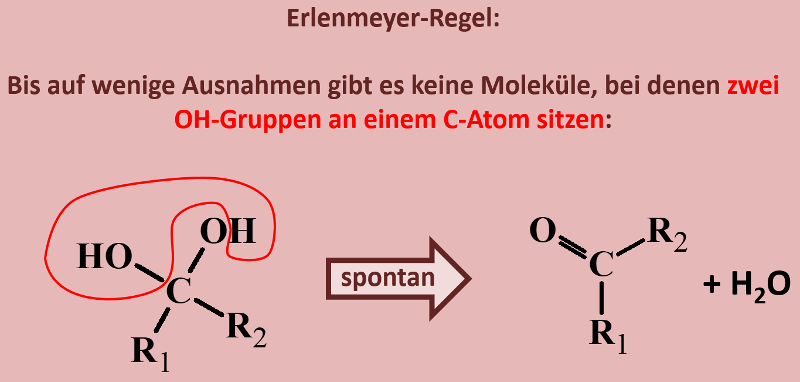
Hast Du wirklich einen schönen, deutschen Satz auf dem Papier stehen?
Unter Abspaltung von Wasser reagiert das Molekül zu einer Verbindung, die anstelle von zwei Hydroxy-Gruppen nun eine Doppelbindung zu einem O-Atom aufweist.
Dieses Phänomen ist unter dem Namen Erlenmeyer-Regel bekannt. Ihr kennt den Namen sicher von dem Glasgefäß "Erlenmeyerkolben".

Aufgrund der polaren Hydroxygruppe eignen sich Alkohole für viele Dinge, für die Alkane nicht brauchbar sind. Lest im Buch die S. 78 - 79 und notiert euch zu jeder fett gedruckten Überschrift einen Satz, der die dort beschriebenen Inhalte zusammenfasst. Solltet ihr das vor 09:00 Uhr geschafft haben, habt ihr kurz Pause. Um 09:00 Uhr wählt euch bitte in die Videokonferenz ein über den Link, den ich euch im Schulmanager geschickt habe.
- Der zu dieser Einheit passende Hefteintrag kann hier heruntergeladen werden: pdf-Datei. Bitte abschreiben oder ausdrucken und ins Heft kleben.
- Lest bis morgen im Buch zur Wiederholung die S. 80, 82 und neu: S. 84
Distanzunterricht Montag, 18.01.
Hallo 9a!
In der heutigen Einheit sollt ihr eine weitere Einteilungsmöglichkeit von chemischen Reaktionen kennenlernen und im Anschluss die neuen Begriff anhand einiger Beispiele einüben. Am Freitag würde ich gerne eine Videokonferenz mit euch durchführen, um die letzten drei Einheiten mit euch live zu besprechen.
Im folgenden Video (3:28min) werden drei Grundtypen chemischer Reaktionen theoretisch vorgestellt. Prägt euch die Begriffe ein, im Anschluss sollt ihr sie anwenden!
Aufgaben: Stellt für die folgenden Reaktionen die chemische Gleichung auf. Gebt an, ob es sich um eine Synthese, Analyse oder Umsetzung handelt und entscheidet, ob es eine exotherme oder endotherme Reaktion ist!
- Eisenpulver und Schwefelpulver wird vermischt. Man taucht einen glühenden Nagel kurz in das Gemisch und es beginnt eine starke Reaktion. Nach und nach glüht das gesamte Gemisch auf. Am Ende liegt der Stoff Pyrit (FeS2) vor.
- Chemische Gleichung: Fe + 2 S --> FeS2
- Grundtyp: Synthese. Begründung: Aus mehreren Edukten wird ein Produkt
- Energiebeteiligung: Exotherm. Begründung: Man muss nur am Anfang kurz den glühenden Eisennagel ins Gemisch tauchen. Danach läuft die Reaktion von alleine ab und setzt die ganze Zeit Energie frei.
- Quecksilberoxid (HgO) wird in einem Reagenzglas mit dem Bunsenbrenner stark erhitzt. Solange sich das RG in der BB-Flamme befindet, strömt Sauerstoff aus dem RG und es bilden sich am Rand kleine Quecksilbertröpfchen
- Chemische Gleichung: 2 HgO --> 2 Hg + O2
- Grundtyp: Analyse. Begründung: Aus einem Edukt werden mehrere Produkte
- Energiebeteiligung: Endotherm. Begründung: Nur solange man Energie zuführt, also sich das RG in der BB-Flamme befindet, läuft die Reaktion ab. Man muss also permanent Energie zuführen.
- In einem RG befinden sich Wasser und ein Stück Magnesium-Band. Am oberen Ende ist das RG mit einem Stopfen verschlossen, in dem ein dünnes Glasrohr steckt. Das Wasser im RG wird vorsichtig erhitzt, so dass es verdampft und alle anderen Gase aus dem RG verbrennt. Es liegt also ein Stück Magensiumband in gasförmigem Wasser vor. Entzünden man das Magnesiumband dann an einer Stelle, reagiert es mit dem Wasser. Sobald die Reaktion gestartet ist, reagiert das gesamte Magnesiumband nach und nach auf der gesamten Länge unter Freisetzung großer Mengen von Licht und Wärme. Nach der Reaktion bleibt der der Stoff Magnesiumoxid (MgO) im RG übrig und während der Reaktion kann man zeigen, dass aus dem dünnen Glasrohr im Stopfen Wasserstoff entweicht.
- Chemische Gleichung: Mg + H2O --> MgO + H2
- Grundtyp: Umsetzung. Begründung: Aus mehreren Edukten werden mehrere Produkte
- Energiebeteiligung: Exotherm. Begründung: Man muss die Reaktion nur einmal kurz starten. Danach läuft die Reaktion von alleine ab und setzt die ganze Zeit Energie frei.
Nachdem nicht klar ist, wann jemals wieder normaler Unterricht stattfindet, hier ein paar Videos, in denen ihr die chemischen Reaktionen dieser Einheit sehen könnt:
Ein relativ ausführliches Video zur Synthese von Eisensulfid (Pyrit):
Die Thermolyse von Quecksilberoxid:
Die Umsetzung von Magnesium in Wasserdampf (mit lustiger Musik... YEAH!):
Hausaufgabe (könnt ihr auch sofort erledigen):
- Ladet den Hefteintrag herunter. Schreibt ihn bitte entweder ab oder druckt ihn aus und klebt ihn in euer Heft: pdf-Datei
- Lest im Buch, S. 34
- Sucht das Arbeitsblatt heraus, auf dem wir das Aufstellen chemischer Gleichungen geübt haben. Falls ihr es nicht findet, kann es hier noch einmal heruntergeladen werden: pdf-Datei. Entscheidet, ob es sich bei den Reaktionen 1, 3, 5 und 7 auf der Vorderseite (links) und den Reaktionen 3, 8 und 10 auf der Rückseite (rechts) um eine Synthese, Analyse oder Umsetzung handelt. Falls die Beschreibung es zulässt, könnt ihr auch angeben, ob es eine exo- oder endotherme Reaktion ist und wenn ihr die chemische Gleichung noch nicht aufgestellt habt, dann holt das bitte nach!
Wir hören uns am Freitag, Link zur Konferenz kommt über den Schulmanager!
Distanzunterricht Montag, 18.01.
In den vorangegangenen Einheiten habt ihr einen historischen Einblick in die Probleme erhalten, die sich beim Arbeiten mit der Masse von Stoffportionen ergeben. Für die weiteren Einheiten sind diese historischen Aspekte erst einmal weniger interessant. Wir wollen in den nächsten Einheiten eher dahin kommen, dass in der Lage seid, z.B. folgende Aufgaben zu lösen:
"Ein Auto verbraucht pro hundert gefahrene Kilometer im Durchschnitt 5,0L Benzin. Wie viel Gramm Kohlenstoffdioxid wird auf diesem Weg ausgestoßen."
Bis dahin müssen jedoch noch einige Dinge geklärt werden und wir fangen heute erst einmal mit kleinen Schritten an. Ihr benötigt für diese Einheit einen Stift, Zettel und euer Buch!
Ihr solltet in der letzten Einheit bemerkt haben, dass die "frühen Chemiker" sehr daran interessiert waren, die Masse von einzelnen Atomen zu bestimmen. Diese Atommasse spielt eine wichtige Rolle bei der Berechnung von Mengeneinheiten, um chemische Reaktionen vollständig durchführen zu können. Nachdem es keine Waage gab, mit der man so kleine Massen bestimmen konnte, behalf man sich mit einer willkürlichen Größe: Die atomare Masseneinheit u wurde eingeführt. Man wusste zwar nicht, wie viel Gramm ein Teilchen wog, welches 1u schwer war, aber man konnte bestimmen wie viel u z.B. ein Sauerstoffatom und wie viel u ein Wasserstoffatom wog. So konnte man die Atome von unterschiedlichen Elementen vergleichen.
Mit Hilfe von Massenspektrometern gelang es irgendwann, für die atomare Masseneinheit u einen Wert in Gramm zu bestimmen, es gilt:
1u = 1,66 x 10-24g
Damit lassen sich nun schon ein paar einfache Aufgaben rechnen. Um zu unterscheiden, ob man von der Masse eines Teilchens in g oder der atomaren Masseneinheit in u spricht, gibt es die zwei Variablen m(X) für die "normale" Masse und ma(X) für die atomare Masseneinheit. X steht dabei für die Teilchen, das man betrachtet. Die folgenden Ausdrücke bedeuten dann folgendes:
m(O-Atom) = 2,658 x 10-23g.
Die Masse eines Sauerstoffatoms beträgt zwei Komma sechs fünf acht mal zehn hoch minus dreiundzwanzig Gramm.
ma(C-Atom) = 12,0u
Die Masse eines Kohlenstoffatoms beträgt zwölf Komma Null u.
Test:
Schreibe als mathematische Gleichung: Misst man die Masse eines Bor-Atoms in atomaren Masseneinheiten, so erhält man 10,811u.
Schreibe als mathematische Gleichung: Die Masse eines Sauerstoff-Moleküls (!) beträgt 5,313 x 10-23 Gramm
Mit Hilfe des oben beschriebenen Zusammenhangs zwischen der Masse in g und der atomaren Masseneinheit in u lassen sich die beiden Größen auch leicht ineinander umwandeln:
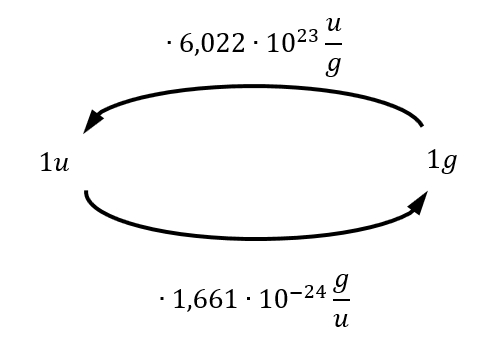
Berechne die Masse eines Sauerstoffmoleküls in u! (Die Masse in Gramm ist oben bereits angegeben)
Nachdem ein unbekannter Stoff X im Massenspektrometer untersucht wurde, konnte die Masse eines Teilchens dieses Stoffes auf 4,79 x 10-22g bestimmt werden. Rechne diesen Wert in atomare Masseneinheiten um!
Man sollte meinen, nachdem man jetzt die atomare Masseneinheit auch in Gramm bestimmen kann, ist die Angabe in u doch nicht mehr nötig. Es war doch nur eine Hilfsgröße, solange man das Gewicht von Atomen noch nicht direkt bestimmen konnte. Die Einheit hat sich aber gehalten, denn sie ist (unter anderem) in folgendem Punkt ganz praktisch: Sie lässt sich einfacher schreiben! Nehmt an, ihr habt ein Molekül "XYZ", für das gilt: ma(XYZ) = 212,3u und m(XYZ) = 3,5 x 10-24g.
Versucht beide Angaben in einem Word-Dokument zu schreiben! Das geht mit der atomaren Masseneinheit sehr leicht, mit der "normalen" Masse tut man sich deutlich schwerer. Dieses "Zehn hoch irgendwas" ist einfach umständlich.
Wenn ihr eure Hausaufgabe gemacht habt und das Buch auf den Seiten 34 - 35 gelesen habt, dann wisst ihr schon, dass man die Masse von Molekülen oder die Formelmasse von Salzen, gemessen in der atomaren Masseneinheit u, ganz einfach bestimmen kann, indem man die Masseneinheiten der einzelnen Atome, die am Aufbau des Moleküls oder der Formelmasse beteiligt sind, zusammenzählt. Bsp.: Möchte man die Masse eines Schwefelsäure-Moleküls (H2SO4) wissen (in u), dann addiert man einfach die Masseneinheiten der am Aufbau beteiligten Atome, also: 2 x ma(H) + ma(S) + 4 x ma(O).
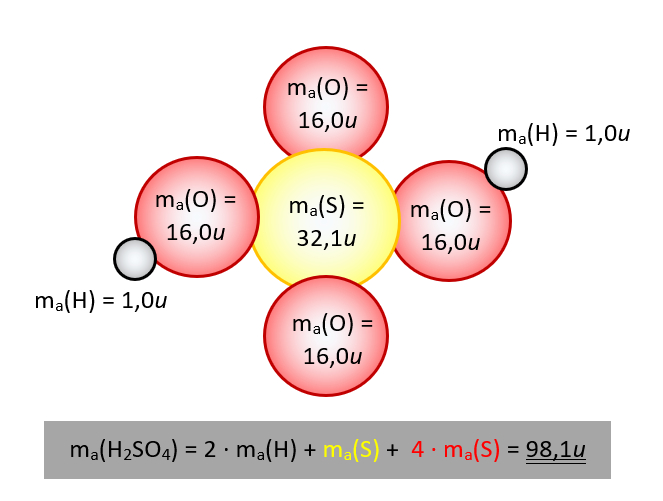
Das leuchtet vermutlich den meisten ein, aber die große Frage ist doch: Woher weiß man die Werte für die einzelnen Atome? - Sie stehen im Periodensystem! Nehmt das Periodensystem im Buch auf der letzten Seite zur Hand. Ihr erkennt im oberen weißen Feld "Erklärungen", dass die Zahl links oberhalb des Elementsymbols die Atommasse in u angibt.
Berechnet nun mit Hilfe des PSEs die Molekülmassen (in u) von:
- Adrenalin (ein Hormon, welches euer Körper in stressigen Situationen ausschüttet), chem. Formel: C9H13NO3
- Koffein (ein Stoff in Kaffee oder Cola, der anregend wirkt), chem. Formel: C8H10N4O2
- Indigo (ein Stoff zum Färben von Jeans), chem. Formel: C16H10N2O2
Adrenalin C9H13NO3:
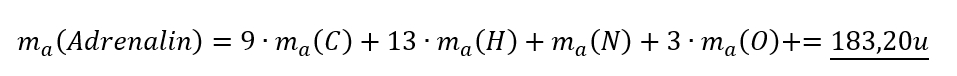
Solltet ihr das nicht richtig haben, dann überprüft genau, wo der Fehler lag und rechnet die anderen beiden Stoffe noch einmal nach!
Mit dem nun verfügbaren Atomgewicht könnte man theoretisch schon arbeiten. Betrachten wir noch einmal das Beispiel aus der letzten Einheit. Es ging um die chemische Reaktion: Eisen reagiert mit Schwefel zu Pyrit:
Fe + 2 S --> FeS2
Diese chemische Gleichung sagt aus, dass man doppelt so viele Schwefel-Atome wie Eisenatome braucht, damit alles miteinander reagiert und nichts übrig bleibt. Angenommen ihr habt einen Teelöffel voll Eisenpulver und wollte exakt die Menge Schwefel dazugeben, die nötig ist, um alles vollständig in Pyrit umzuwandeln. Dann könnte man jetzt die Portion Eisen wiegen, mit Hilfe der Atommasse von Eisen ausrechnen, wie viele Atome das sind. Diese Anzahl verdoppeln und dann ausrechnen, welche Masse diese Anzahl an Schwefelatomen hat. Diese Menge könnte man dann abwiegen. Das folgende Bild veranschaulicht den Rechenweg:
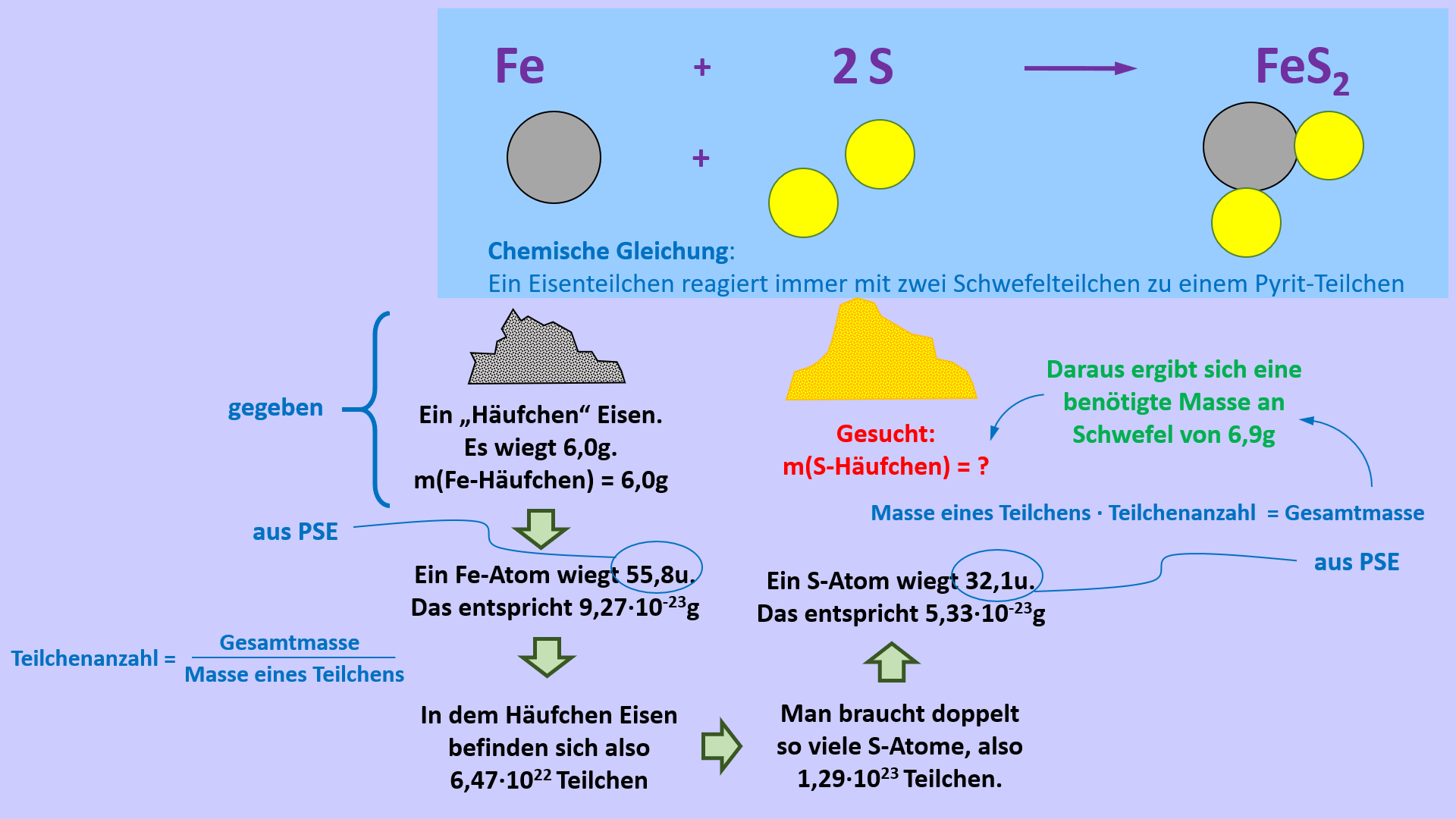
Das wirkt noch etwas umständlich...
Bei dieser Berechnung tauchen nämlich wieder sehr große, unhandliche Zahlen auf: Die Anzahl der Teilchen. Diese wird in der Chemie mit einem N(X) gekennzeichnet. Also z.B. kann man den Satz: "In meinem Zimmer liegen 3208 Legosteine auf dem Boden mathematisch so formulieren:
N(Legosteine) = 3208
Weil Atome so klein sind, befinden sich in den 6,0g Eisen einfach unglaublich viele Atome: Die Anzahl beträgt N(Fe) = 6,47 x 1022. Eine Zahl mit dreiundzwanzig Stellen (!), in Worten also ungefähr 600 Trilliarden Atome...
Daher hat man sich etwas einfacheres ausgedacht: Man betrachtet einfach eine sehr große Menge an Teilchen und gibt dieser Anzahl einen bestimmten Namen. Das ist nicht so ungewöhnlich, wie es vielleicht im ersten Moment klingt. Ihr kennt z.B. sicher den Ausdruck "ein Dutzend" für die Anzahl 12. (Wo jetzt genau der Sinn darin liegt zu sagen, "Ich hole beim Bauern ein Dutzend Eier" anstatt "Ich hole beim Bauern zwölf Eier", kann ich euch auch nicht genau sagen. Aber das Phänomen gibt es eben. Fragt mal eure Oma ob sie den Begriff "Schock" noch kennt, für eine Anzahl an z.B. Eiern).
In der Chemie hat man nun den Begriff "Mol" eingeführt. Das ist die Bezeichnung für eine bestimmte Anzahl an Teilchen, nämlich 6,022 x 1023. Man nennt diesen Wert auch Avogadro-Konstante NA = 6,022 x 1023 1/mol
Freiwilliger Test:
- Besorgt euch eine Stoppuhr oder ruft die Funktion auf eurem Handy auf!
- Stoppt die Zeit, die ihr benötigt, um zehn mal "Sechs Komma null zwei zwei mal zehn hoch dreiundzwanzig" zu sagen!
- Stoppt die Zeit, die ihr benötigt, um zehn mal "Ein Mol" zu sagen!
Ergebnis? - Seht ihr, die Einheit "Mol" ist eben praktisch.
Warum jetzt ausgerechnet 6,022 x 1023? - Das ist genialer Schachzug der Chemiker gewesen. Diese Zahl wurde deshalb gewählt, weil dann die im PSE angegebene atomare Masseneinheit genau übereinstimmt mit der Masse in g, die ein Mol dieser Teilchen wiegt.
Nochmal langsam, zum mitschreiben: Die Zahl, die oben links bei den Elementsymbolen im PSE steht, gibt also nicht nur die Masse eines Atoms dieses Elements in u an, sondern gleichzeitig entspricht dieser Wert der Masse in g von einem Mol dieser Atome. - Wahnsinn! Diese Chemiker..., das sind vielleicht Teufelskerle!
Und jetzt wieder ernst: Diese Größe, also die Masse, die ein Mol eines Stoffes in g wiegt, nennt man Molare Masse M(X). Ein Beispiel: "Die molare Masse von Wasser, also diejenige Masse in Gramm, die ein Mol Wassermoleküle wiegen, beträgt 18g/mol." oder in Form einer mathematischen Gleichung: M(H2O) = 18g/mol.
Die Variable, um eine Anzahl in Mol zu messen, nennt man "Stoffmenge", sie wird mit einem kleinen n(X) gekennzeichnet, die Einheit Mol wird abgekürzt mit mol. Wenn man also sagen möchte: "Ich habe heute 2 Mol Erdbeeren gepflückt, dann kann man das so formulieren:
n(Erdbeeren) = 2mol (Dieser Wert ist völlig unrealistisch. So viele Erdbeeren gibt es auf der ganzen Welt nicht)
Test:
Wie spricht man die folgende Gleichung aus: n(Sterne im Universum) = 0,1mol (Dieser Wert stimmt ungefähr)? Wie viele Sterne sind das?
- Die Anzahl der Sterne im Universum beträgt Null Komma Ein Mol.
- Das sind 6,022 x 1022 oder auch 0,602 x 1023
Schreibe als mathematische Gleichung: In der Sahara gibt es ungefähr Null Komma eins Mol Sandkörner.
Einfache Aufgaben
- Es liegen 14,007g Stickstoffatome vor. Wie viel Mol sind das?
- Wie viel Gramm wiegen 2 Mol Kohlenstoffatome?
- Im Jahr 2018 wurden grob geschätzt 4 x 1011 Äpfel auf der ganzen Welt geerntet. Wie viel Mol sind das?
- Der Wert der angegebenen Masse in g entspricht genau dem Wert, der im PSE links über dem Element steht, also ist das genau die Masse eines Mols Stickstoffatome
- Die Zahl links oberhalb des Kohlenstoffs im PSE lautet 12,000. Das ist die Masse in g, die ein Mol wiegen würde. Zwei Mol müssen dann das doppelte wiegen, also 24,0g.
- Als Hilfe: Das ist eine ähnliche Frage, wie man wissen will: "Wie viele Dutzend sind 7 Eier?". Man muss die tatsächliche Anzahl durch diejenige Anzahl teilen, die in einem Dutzende stecken, also 7 geteilt durch 12. Bei dem Beispiel mit den Äpfeln: 4 x 1011 geteilt durch 6,022 x 1023. Ergibt 6,67 x 10-13mol.
Die einfachen Berechnungen in den oberen Kästen waren mehr so... "freestyle". Viele von euch werden die Aufgaben relativ problemlos lösen können. Manche brauchen aber vielleicht etwas mehr Struktur. Diesen Personen empfehle ich das Buch (S. 35 - 38), die Hefteinträge (s. u.) und ganz knapp zusammengefasst die folgende Übersicht, die die bisher besprochenen Größen und ein paar Gleichungen zum Umrechnen enthält:
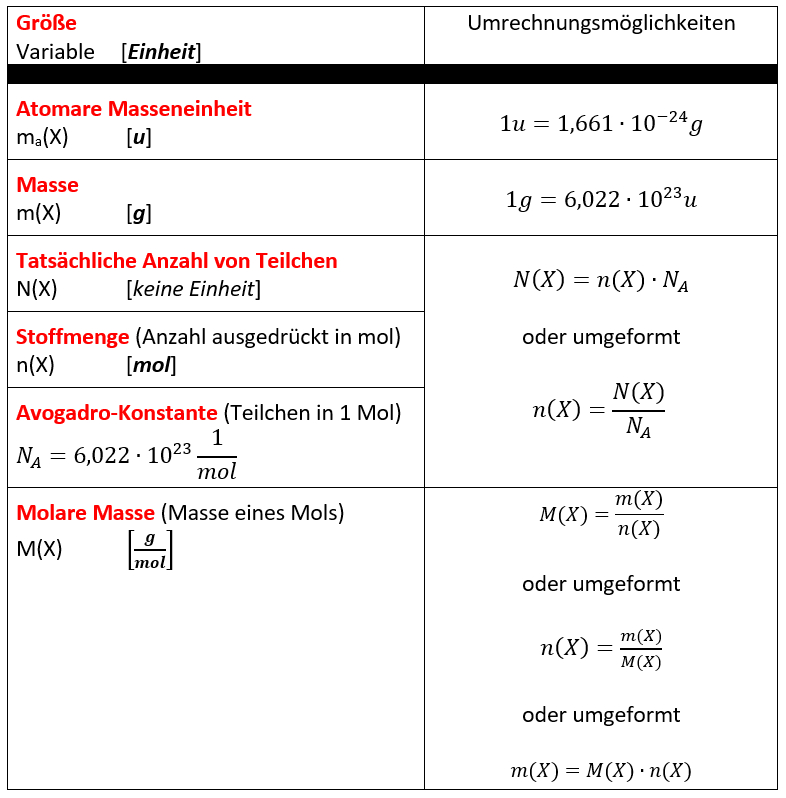
Hausaufgabe:
Auch wenn ihr zu der Gruppe gehört, die glaubt, bereits alles verstanden zu haben, lest ihr bitte als Hausaufgabe im Buch die folgenden Absätze und die Hefteinträge. Die Datei mit den Hefteinträgen haltet ihr bitte morgen Nachmittag bereit (z.B. geöffnet in einem Fenster auf dem PC, an dem ihr arbeitet). Wir machen eine Videokonferenz, besprechen noch einmal alles und lösen dann die in der pdf-Datei enthaltenen Aufgaben!
- Die Teilchenzahl (S. 36)
- Die Stoffmenge (S. 36-37)
- Teilchenzahl und Stoffmenge (S. 37)
- Teilchenzahl und Masse (S. 37)
- Molare Masse und molares Volumen (S. 38)
- Die molare Masse (S. 38)
- Hefteinträge zu dieser und letzter Stunde (Punkt 4 wurde noch nicht besprochen): pdf-Datei
Distanzunterricht Donnerstag, 14.01. Chemie
Um 08:15 Uhr findet die BBB-Konferenz statt, um die Anwesenheit zu kontrollieren. Bis dahin macht ihr ab 08:00 Uhr bitte folgendes:
Scrollt auf dieser Seite nach unten bis zum Abschnitt "Distanzlernen für Donnerstag, 17.12.". Wiederholt die dort gestellte Aufgabe im ersten lilafarbenen Block "Bindungsarten". Das sollte in 15min. zu schaffen sein. Startet dann bitte pünktlich die BBB-Konferenz.
Nach der Anwesenheitskontrolle bearbeitet ihr bitte die folgenden Aufgaben alleine. Sollte BBB stabil laufen, können wir das gerne in Form von Gruppenarbeiten mit anschließender Besprechung durchführen. Sollte die Verbindung schlecht sein oder abbrechen, könnt ihr die Aufgaben hier auch alleine bearbeiten.
Wechselt um 08:45 Uhr auf jeden Fall zum Biologie-Auftrag!
Aufgaben:
- Salze 1
Formuliere die chemische Gleichung zur Bildung von Natriumoxid aus den Elementen
- Bestimme die Anzahl an Valenzelektronen von Natrium und Sauerstoff.
- Leite daraus ab, welche Ionen diese Stoffe bilden werden
Na --> Na+ + e-
O + 2e- --> O2-
(Eine chemische Gleichung ist hier nicht unbedingt nötig, es genügt, wenn ihr die richtigen Ionen ableiten könnt)
- Aus den Ionen muss sich ein Salz bilden, das insgesamt neutral ist. In welchem Verhältnis müssen sich die Ionen dazu zusammen finden?
- Wie formuliert man das als chemische Formel?
2 Na+ und 1 O2- Teilchen ergeben insgesamt die chemische Formel Na2O
- Nun kann man beginnen die chemische Gleichung aufzustellen. Dabei ist darauf zu achten, dass Sauerstoff zur HONClBrIF-Gruppe gehört!
- Alle Edukte links, Reaktionspfeil, Produkt rechts und ausgleichen bitte!
4 Na + O2- --> 2Na2O
- Salze 2
Begründe, warum Salze in der Regel einen sehr hohen Siedepunkt haben, Moleküle eher niedrigere!
Eine gute Begründung enthält folgende Aspekte:
- Man erklärt zunächst, was "Sieden überhaupt bedeutet"!
Beim "Sieden" müssen die Teilchen, aus denen sich ein Stoff zusammensetzt voneinander getrennt werden.
- Dann kann man darauf eingehen, warum die Siedetemperatur ganz generell unterschiedlich sein kann, wovon sie also allgemein abhängt!
Es kommt auf die Kräfte an, welche die Teilchen zusammenhält.
- Jetzt kann man konkret werden und auf die hier vorliegenden Unterschiede dieser Kräfte eingehen!
Salze bestehen aus Ionen, die alle geladen sind. Unterschiedlich geladene Teilchen ziehen sich (stark) an, daher haben Metalle im Vergleich zu Molekülen hohe Siedepunkte. Moleküle sind in der Regel nämlich neutral. Sie ziehen Nachbarmoleküle kaum an. Daher lassen sie sich leicht (schon bei geringen Temperaturen) voneinander trennen und der Stoff siedet.
Warum sich Moleküle doch etwas gegenseitig anziehen und manche Moleküle daher schon höhere Siedepunkte besitzen können, besprechen wir demnächst.
- Moleküle
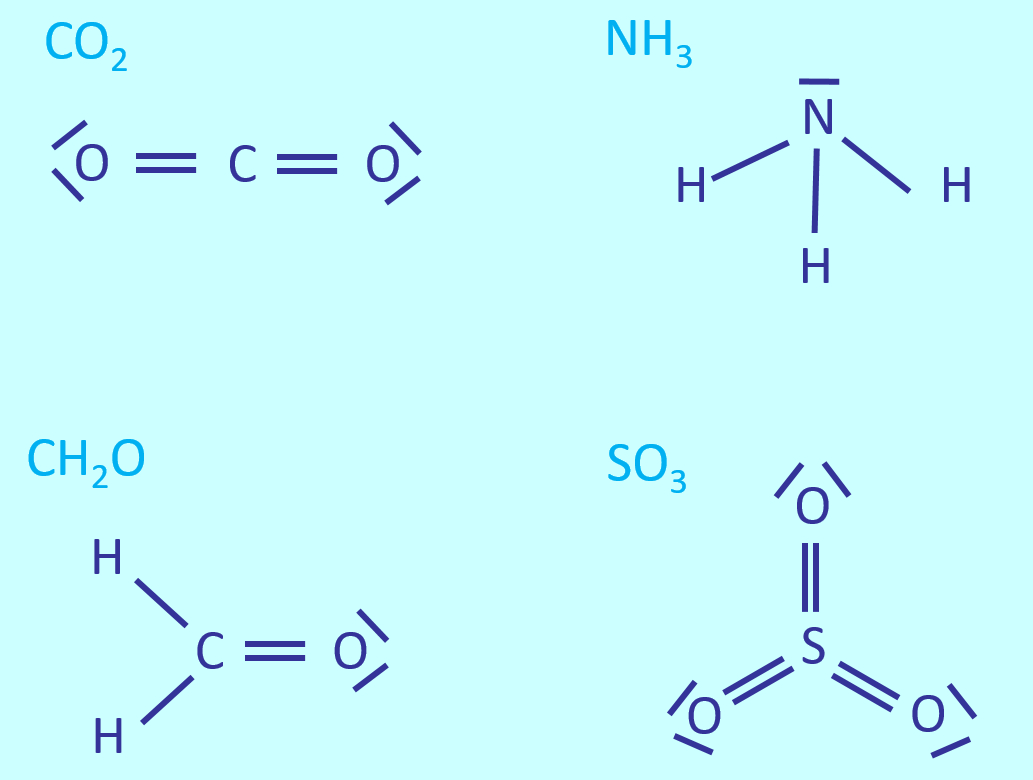
Zeichnet die Valenzstrichformeln für: CO2, NH3, CH2O, SO3
- Metalle
Begründe, warum Metalle in der Regel sehr gute elektrische Leiter sind!
- Es bietet sich an, hier zunächst den Aufbau von Metallen zu beschreiben.
Man kann das natürlich auch mit Worten beschreiben, dann sollten auf jeden Fall die Begriffe "positiv geladenene Atomrümpfe" und "frei bewegliches Elektronengas" auftauchen. Eine Skizze sieht so aus:
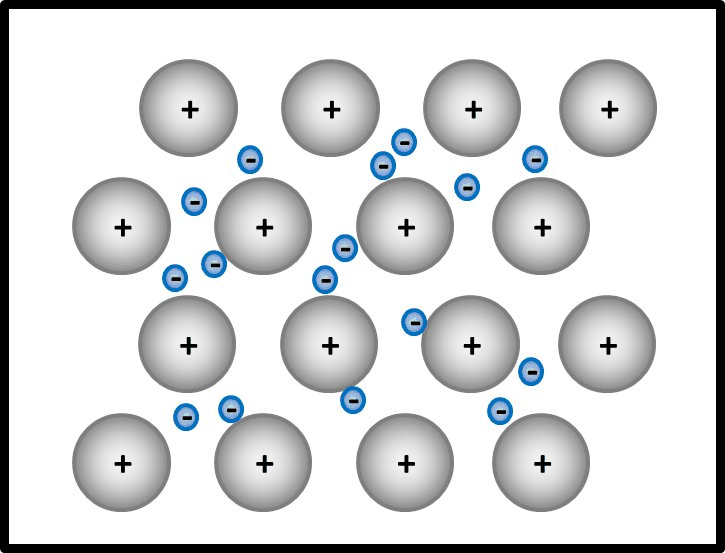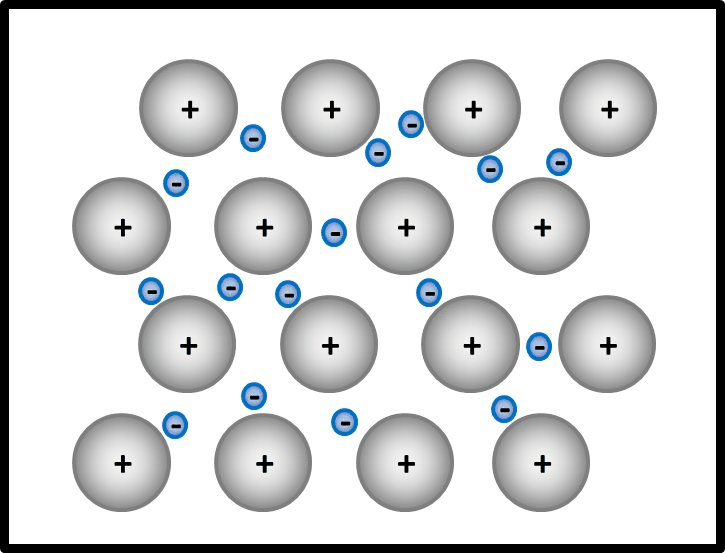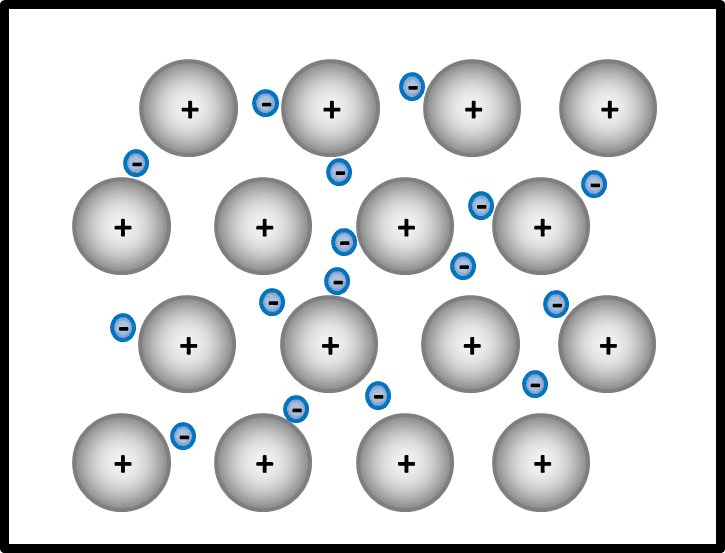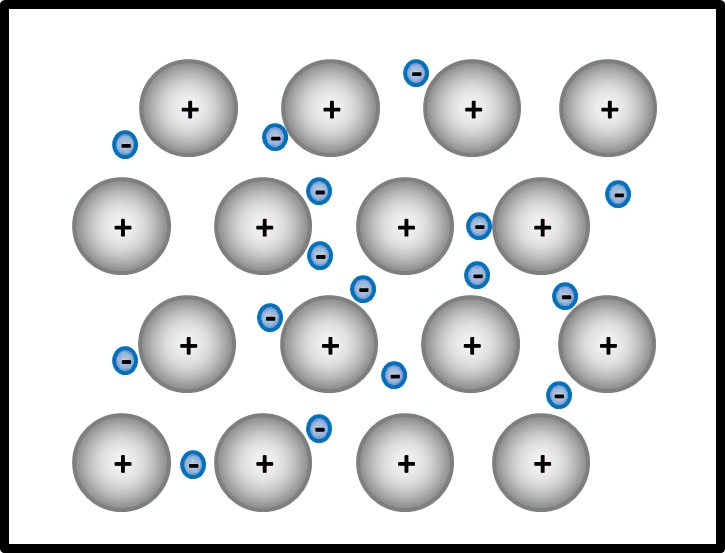
- Jetzt stellt man den Zusammenhang mit der elektrischen Leitfähigkeit her!
Elektrisch leitend ist ein Stoff dann, wenn geladene Teilchen durch ihn fließen können. Hier sind frei bewegliche, negativ geladene Elektronen vorhanden. Damit sind alle Bedingungen erfüllt.
Distanzunterricht Freitag, 15.01. Chemie
Bitte bearbeitet die folgende Einheit am besten in der eigentlichen Unterrichtszeit von 08:45 - 09:30 Uhr. Ihr benötigt das Arbeitsblatt, welches ihr vor den Ferien erhalten habt und auf dem die Vorderseite bereits ausgefüllt ist. Solltet ihr das AB nicht mehr finden, könnt ihr es hier noch einmal herunterladen:
pdf-Datei
Schaut bitte zunächst das folgende Video. Es enthält eine Zusammenfassung der letzten Einheit und erklärt einen neuen Aspekt. Während des Videos solltet ihr auch das AB auf der Rückseite ausfüllen. Nach dem Video bearbeitet bitte die Aufgaben darunter. Lasst euch die Lösung erst anzeigen, wenn ihr tatsächlich eine gefunden habt!
Aufgaben:
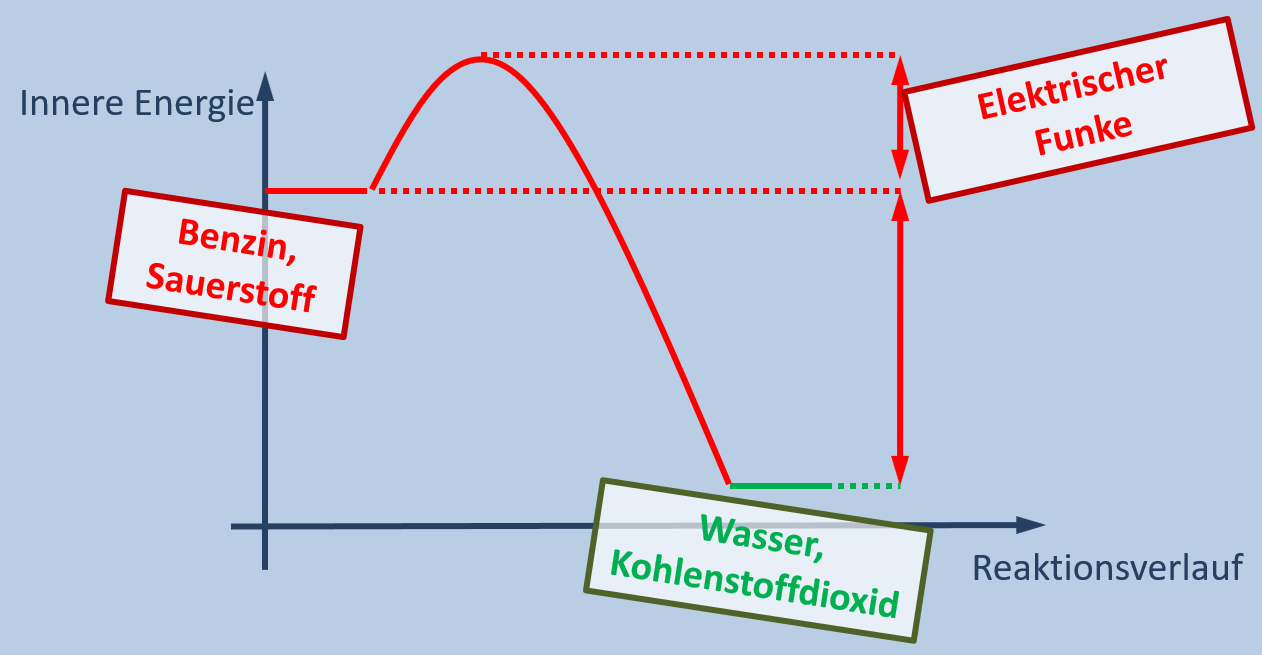
Startet man ein Auto, so wird durch das Umdrehen des Schlüssels etwas Energie aus der Batterie in einen elektrischen Funken im Motor umgewandelt, der vergastes Benzin entzünden. Dabei reagiert das Benzin mit Sauerstoff. Wenn der Motor läuft, könnte man die Batterie auch entfernen.
- Erkläre, ob es sich bei der Verbrennung von Benzin im Motor eines Autos um einen exothermen oder endothermen Vorgang handelt!
- Zeichne ein Energie-Reaktionsverlaufs-Diagramm, in dem die wichtigen Begriffe aus dem Text der Grafik richtig zugeordnet sind!
Es muss sich um eine exotherme Reaktion handeln. Sie muss nur einmal kurz durch Zufuhr von Aktivierungsenergie gestartet werden. Danach wird ständig Energie (in Form von Wärme oder auch Bewegungsenergie) frei.
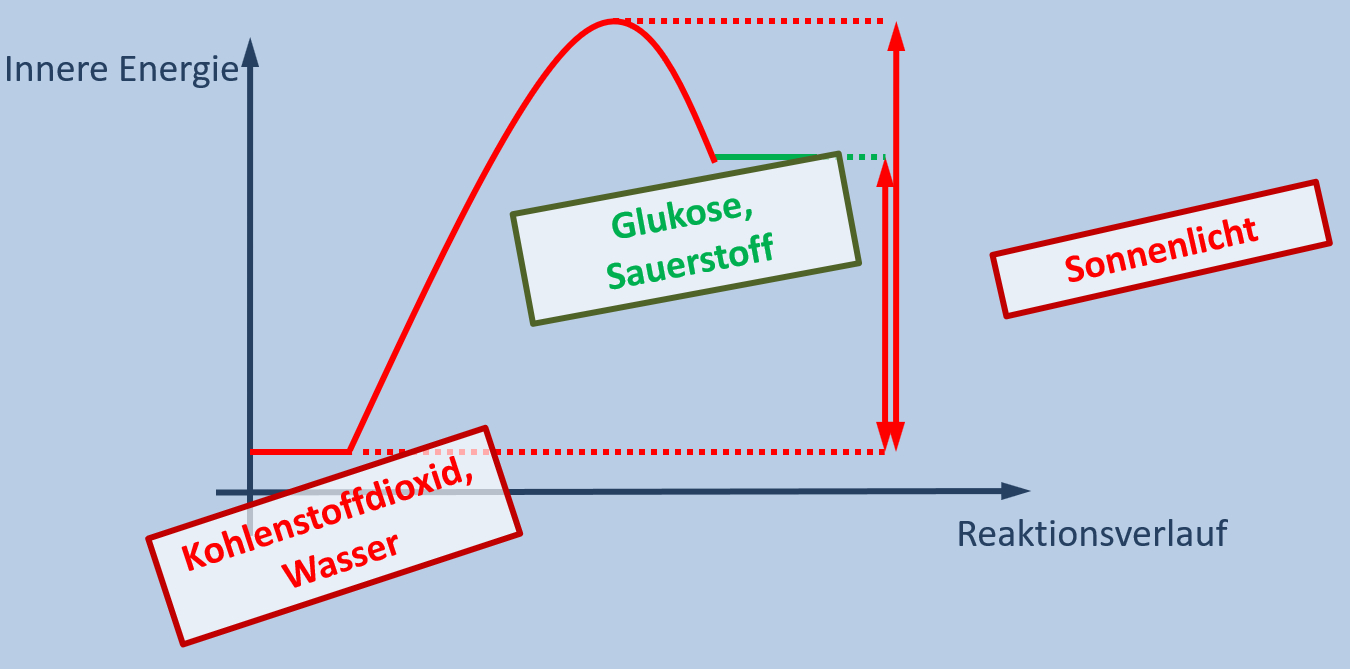
Pflanzen können mit Hilfe von Sonnenlicht aus Kohlenstoffdioxid und Wasser die Stoffe Glukose und Sauerstoff herstellen. Bei manchen Unterwasserpflanzen kann man den entstehenden Sauerstoff sehr schön sehen, da er in Form von Gasbläschen aufsteigt. Das funktioniert allerdings nur solange, wie die Unterwasserpflanze mit Licht bestrahlt wird. Verdunkelt man die Pflanze entstehen auch keine Gasblasen mehr.
- Erkläre, ob es sich bei der Verbrennung von Benzin im Motor eines Autos um einen exothermen oder endothermen Vorgang handelt!
- Zeichne ein Energie-Reaktionsverlaufs-Diagramm, in dem die wichtigen Begriffe aus dem Text der Grafik richtig zugeordnet sind!
Es muss sich um eine endotherme Reaktion handeln. Nur solange die Pflanze von Licht (Energie) getroffen wird, entstehen die Produkte (zu sehen am aufsteigenden Sauerstoff)
Distanzunterricht Donnerstag, 14.01. Chemie
Um 08:15 Uhr findet die BBB-Konferenz statt, um die Anwesenheit zu kontrollieren. Bis dahin macht ihr ab 08:00 Uhr bitte folgendes:
Scrollt auf dieser Seite nach unten bis zum Abschnitt "Distanzlernen für Donnerstag, 17.12.". Wiederholt die dort gestellte Aufgabe im ersten lilafarbenen Block "Bindungsarten". Das sollte in 15min. zu schaffen sein. Startet dann bitte pünktlich die BBB-Konferenz.
Nach der Anwesenheitskontrolle bearbeitet ihr bitte die folgenden Aufgaben alleine. Sollte BBB stabil laufen, können wir das gerne in Form von Gruppenarbeiten mit anschließender Besprechung durchführen. Sollte die Verbindung schlecht sein oder abbrechen, könnt ihr die Aufgaben hier auch alleine bearbeiten.
Wechselt um 08:45 Uhr auf jeden Fall zum Biologie-Auftrag!
Aufgaben:
- Salze 1
Formuliere die chemische Gleichung zur Bildung von Natriumoxid aus den Elementen
- Bestimme die Anzahl an Valenzelektronen von Natrium und Sauerstoff.
- Leite daraus ab, welche Ionen diese Stoffe bilden werden
Na --> Na+ + e-
O + 2e- --> O2-
(Eine chemische Gleichung ist hier nicht unbedingt nötig, es genügt, wenn ihr die richtigen Ionen ableiten könnt)
- Aus den Ionen muss sich ein Salz bilden, das insgesamt neutral ist. In welchem Verhältnis müssen sich die Ionen dazu zusammen finden?
- Wie formuliert man das als chemische Formel?
2 Na+ und 1 O2- Teilchen ergeben insgesamt die chemische Formel Na2O
- Nun kann man beginnen die chemische Gleichung aufzustellen. Dabei ist darauf zu achten, dass Sauerstoff zur HONClBrIF-Gruppe gehört!
- Alle Edukte links, Reaktionspfeil, Produkt rechts und ausgleichen bitte!
4 Na + O2- --> 2Na2O
- Salze 2
Begründe, warum Salze in der Regel einen sehr hohen Siedepunkt haben, Moleküle eher niedrigere!
Eine gute Begründung enthält folgende Aspekte:
- Man erklärt zunächst, was "Sieden überhaupt bedeutet"!
Beim "Sieden" müssen die Teilchen, aus denen sich ein Stoff zusammensetzt voneinander getrennt werden.
- Dann kann man darauf eingehen, warum die Siedetemperatur ganz generell unterschiedlich sein kann, wovon sie also allgemein abhängt!
Es kommt auf die Kräfte an, welche die Teilchen zusammenhält.
- Jetzt kann man konkret werden und auf die hier vorliegenden Unterschiede dieser Kräfte eingehen!
Salze bestehen aus Ionen, die alle geladen sind. Unterschiedlich geladene Teilchen ziehen sich (stark) an, daher haben Metalle im Vergleich zu Molekülen hohe Siedepunkte. Moleküle sind in der Regel nämlich neutral. Sie ziehen Nachbarmoleküle kaum an. Daher lassen sie sich leicht (schon bei geringen Temperaturen) voneinander trennen und der Stoff siedet.
Warum sich Moleküle doch etwas gegenseitig anziehen und manche Moleküle daher schon höhere Siedepunkte besitzen können, besprechen wir demnächst.
- Moleküle
Zeichnet die Valenzstrichformeln für: CO2, NH3, CH2O, SO3
- Metalle
Begründe, warum Metalle in der Regel sehr gute elektrische Leiter sind!
- Es bietet sich an, hier zunächst den Aufbau von Metallen zu beschreiben.
Man kann das natürlich auch mit Worten beschreiben, dann sollten auf jeden Fall die Begriffe "positiv geladenene Atomrümpfe" und "frei bewegliches Elektronengas" auftauchen. Eine Skizze sieht so aus:

- Jetzt stellt man den Zusammenhang mit der elektrischen Leitfähigkeit her!
Elektrisch leitend ist ein Stoff dann, wenn geladene Teilchen durch ihn fließen können. Hier sind frei bewegliche, negativ geladene Elektronen vorhanden. Damit sind alle Bedingungen erfüllt.
Distanzunterricht Donnerstag, 14.01. Bio
In den letzten Stunden vor den Weihnachtsferien ging es um Prozesse, die sich auf molekularer Ebene abspielen. Ihr habt gesehen, wie in den Mitochondrien energiereiches ATP aus Zucker und Sauerstoff hergestellt wird. Das Thema war im Prinzip abgeschlossen und wir machen einen großen Sprung zur Ökologie.
Das Wort ist euch sicher geläufig, die genaue Bedeutung wahrscheinlich nicht unbedingt. Ihr seht unten zwei Videos, die sich mit Grundbegriffen der Ökologie beschäftigen. Die Videos besitzen eine hohe Informationsdichte und sind unter Umständen etwas schnell. Trotzdem sind sie ganz gut gelungen und bieten vielleicht etwas Abwechslung. Es werde euch hier Ausschnitte abgespielt. Auf yt direkt könnt ihr die Videos aber auch ganz anschauen.
Schaut beide Videos und bearbeitet anschließend die Aufgaben darunter!
Aufgaben:
Klickt zunächst auf folgenden Link. Ihr gelangt zu einer Seite, die "Eco-Spheres" verkauft. Ein angeblich ursprünglich von der NASA entwickeltes "Ökosystem" für den Schreibtisch. Lest die Produktinformationen und kehrt dann wieder hierher zurück!
Zur Eco-Sphere
Aufgaben:
- Wende die soeben gelernten Fachgriffe an und ordnen ihnen die richtigen Objekte aus der Eco-Sphere zu!
- Was an der Eco-Sphere ist Biotop, was Biozönose?
- Welche Organismen sind Produzenten, Konsumenten und Reduzenten?
- Biotop: Glasgefäß, Steinchen, Muschel-Schalen (Das Gefäß enthält keine lebenden Muscheln) Gorgonie, Wasser; Biozönose: grüne Faden- und braune Flächen-Algen, Garnelen, Mikroorganismen
- Produzenten: grüne Faden- und braune Flächen-Algen, Konsumenten: Garnelen, Reduzenten: Mikroorganismen
Es gibt drei Begriff, die eher aus der Physik stammen und die Wechselwirkung von Systemen mit ihrer Umgebung beschreiben:
- Offene Systeme
Offen bedeutet, dass SOWOHL Energie mit der Umgebung ausgetauscht werden, ALS AUCH Stoffe
- Geschlossene Systeme
Bei geschlossenen System kann zwar Energie mit der Umgebung ausgetauscht werden, allerdings keine Stoffe
- Isolierte Systeme
Isolierte System stehen in überhaupt keinem Austausch mit der Umgebung.
Ökosysteme sind in der Regel offene Systeme. Betrachten wir einen See: Ein im See lebender Frosch könnte den See durchaus verlassen und in den angrenzenden Wald hüpfen und dort Kot absetzen. Damit wären Stoffe aus dem See in die Umgebung gelangt. Umgekehrt könnte auch ein Ente von weit her angeflogen können und Fischeier, die an ihrem Gefieder hingen im See hinterlassen. Damit wären Stoffe in den See aus der Umgebung eingetragen worden.
Auch ein Energieaustausch ist möglich: Wenn die Sonne scheint, können die Sonnen strahlen in den See eindringen und ihn aufheizen. Nachts kann diese Wärme z.B. an die Atmosphäre wieder abgegeben werden.
Beurteile begründet, ob die Eco-Sphere tatsächlich ein Öko-System in diesem Sinne ist.
Ein Energieaustausch ist zwar möglich. Das Glasgefäß lässt ja z.B. Lichtstrahlen ein- und austreten; ein Stoffaustausch ist jedoch mit der Umgebung nicht möglich. Daher ist dieses System geschlossen und unterscheidet sich in diesem Punkt von offenen Ökosystemen in der Natur
Freiwillig:
Vor einigen Jahren versuchte man mit einer Art Gewächshaus die Erde nachzuahmen, um zu testen, ob man in einem geschlossenen System (z.B. auf dem Mars) als Mensch länger überleben könnte. Das Projekt hieß "Biosphäre 2". Wer möchte, kann einen 7min. Film dazu schauen:
Hausaufgabe:
Lest im Buch S. 62 - 63
Lasst euch das, was wir gestern (Montag) besprochen haben noch einmal kurz durch den Kopf gehen. Ihr könnt dazu auf dieser Seite etwas nach unten scrollen und die Fragen überfliegen, die im letzten Arbeitsauftrag behandelt wurden.
Wie würdet ihr in höchstens drei Sätzen zusammenfassen, was ihr aus dieser letzten Einheit mitgenommen habt?
Möglich wäre z.B.:
- Ein Schokokuchen ist schon was leckeres...
- Auf "Vogelhäuschen selber bauen" hätte ich ja gar keinen Bock. Da kauf ich lieber eins.
- Eine Tonne Äpfel auf einem Anhänger??? Auf den Anhänger von meinem Onkel passen 16 Tonnen!
O.k., das könnten zwar auch Dinge gewesen sein, die euch durch den Kopf gegangen sind, aber jetzt mal in Bezug auf Chemie!
Möglich wäre z.B.:
- In chemischen Gleichungen spielt die Anzahl von Teilchen (Atomen, Molekülen, Salzeinheiten) eine Rolle
- Leider kann man solche Teilchen aber nicht abzählen
- Man müsste die Masse von diesen Teilchen wissen, damit man etwas damit anfangen kann
Ihr sollt heute einen kleinen Versuch durchführen, mit dem man die Masse von kleinen Teilchen ziemlich genau bestimmen kann, auch wenn man sie nicht direkt wiegt. Mit einzelnen Atomen oder Molekülen könnt ihr natürlich nicht arbeiten, daher nehmen wir andere "kleine Teilchen". Ihr benötigt also:
- Entweder Reiskörner oder trockene Erbsen oder trockene Linsen oder sonst irgendetwas kleines (Reißnägel, Büroklammern etc.)
- Eine Küchenwaage
- Geduld
Die Objekte, die ihr euch aussucht, sollten so klein (und leicht) sein, dass eine Küchenwaage "nichts" anzeigt, wenn man eins dieser Objekte darauf legt. Zählt jetzt so viele Teilchen ab (z.B. 100, evtl. aber auch 1000), dass eure Küchenwaage einen "vernünftigen Wert" anzeigt, ich würde empfehlen so um die 10 Gramm.
Ihr könnt auch umgekehrt vorgehen: Wiegt exakt 10,0g ab und bestimmt dann die in dieser Menge enthaltene Anzahl an Objekten.
Berechnet aus diesen beiden Werten (Anzahl und Gewicht) das Gewicht eines Teilchens. Recherchiert dann im Internet ob ihr einen Wert findet, der euer Ergebnis bestätigt (oder auch widerlegt). Wenn ihr Pflanzenteile genommen habt, dann werdet ihr wahrscheinlich sehr schnell auf Wikipedia fündig. Als Suchtipp kann ich euch auch den Begriff "Tausendkornmasse" empfehlen.
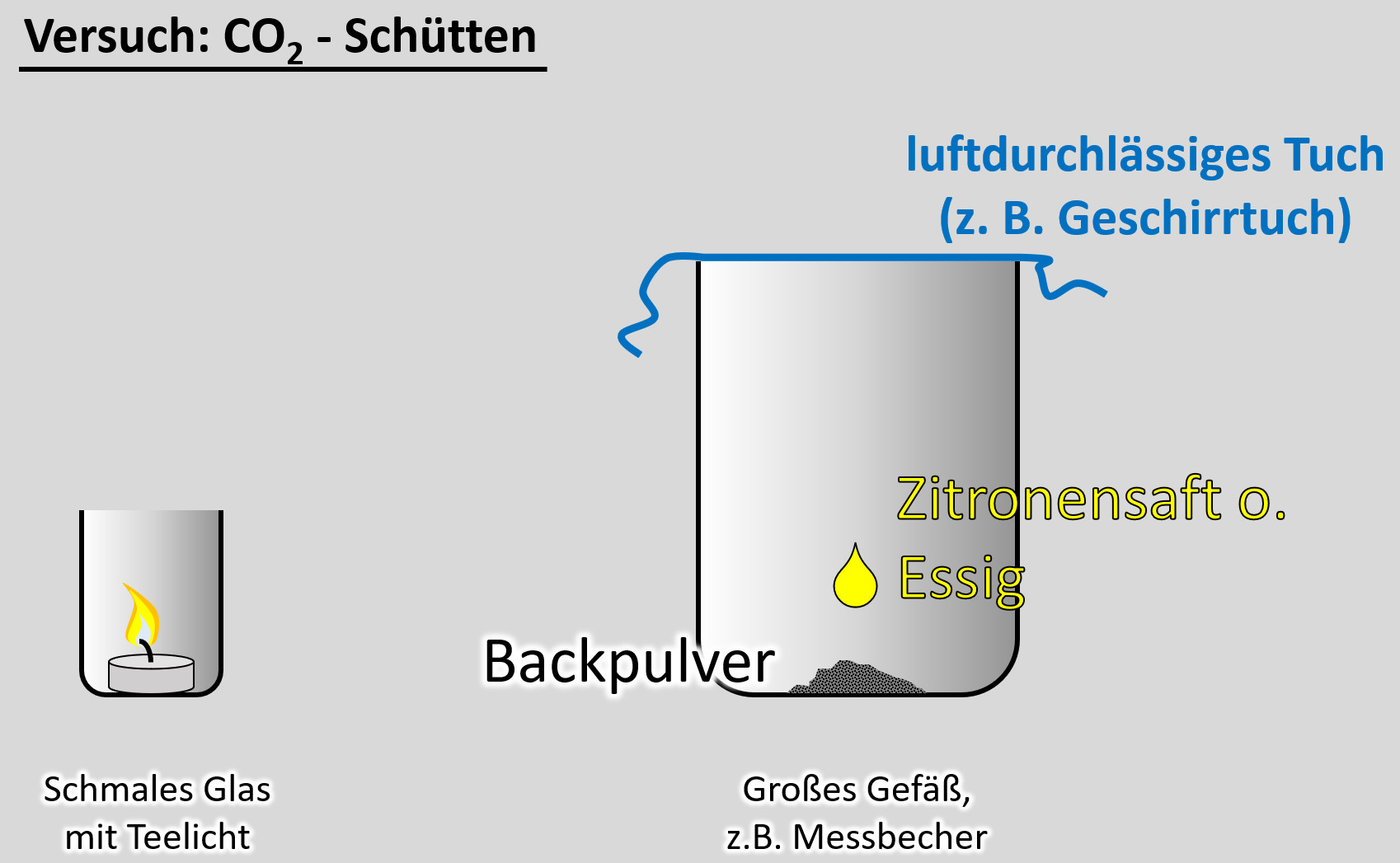
Ein freiwilliger Versuch. Ihr benötigt dazu:
- ein schmale Glas, in das gerade so ein Teelicht passt
- ein Teelicht
- ein größeres Gefäß, z.B. Messbecher
- ein Geschirrtuch (o.ä.)
- ein Päckchen Backpulver
- Essig oder besser: Essigessenz
- Entzündet das Teelicht im schmalen Glas
- Gebt das Backpulver in das große Gefäß und legt das Geschirrtuch bereit
- Schüttet nun etwa 50 - 100mL Essig auf das Backpulver und bedeckt dann sofort das Gefäß mit dem Geschirrtuch. (Hinweis: Bei dem Versuch entsteht das Gas Kohlenstoffdioxid. Das ist schwerer als Luft und soll im Messbecher bleiben. Durch kleinste Luftverwirbelungen wird es aber aus dem Messbecher gespült. Mit dem Geschirrtuch soll das verhindert werden.
- Wartet ab, bis die Gasentwicklung nachlässt. Euer Messbecher ist nun randvoll mit Kohlenstoffdioxid (was man aber nicht sehen kann).
- Zieht nun vorsichtig das Geschirrtuch ab. Und gießt das Kohlenstoffdioxid in das schmale Gefäß mit der Kerze. Achtung: Nicht den Essig in das schmale Gefäß gießen!
Beobachtung/Erklärung:
Da das Gas Kohlenstoffdioxid schwerer als Luft ist, wird es in das schmale Glas "fallen" und dort die Luft verdrängen. Eine Verbrennung ist in reinem Kohlenstoffdioxid nicht möglich. Daher sollte die Kerze erlöschen. Wenn ihr auf "Video" klickt, seht ihr eine Variante, so wie es aussehen sollte.