|
|
| Zeile 163: |
Zeile 163: |
| |Lösung|Lösung ausblenden}} | | |Lösung|Lösung ausblenden}} |
| <br> | | <br> |
| |Farbe= #607
| |
| |Rahmen= 0
| |
| |Rahmenfarbe= #DCF
| |
| |Hintergrund= #DCF
| |
| }}
| |
|
| |
| === Chemische Reaktionen einteilen ===
| |
| {{Box-spezial
| |
| |Titel=<span style="color:#607">'''Drei Grundtypen chemischer Reaktionen'''</span>
| |
| |Inhalt=
| |
| Das folgende Video (3:28) stammt aus der Corona-Zeit und wurde von einem Lehrer für das Home-Schooling angefertigt. Dort werden drei Grundtypen chemischer Reaktionen theoretisch vorgestellt. Prägt euch die Begriffe ein, im Anschluss sollt ihr sie anwenden! <br>
| |
| {{#ev:youtube|WSVnJPBwpek}}<br>
| |
| <br>
| |
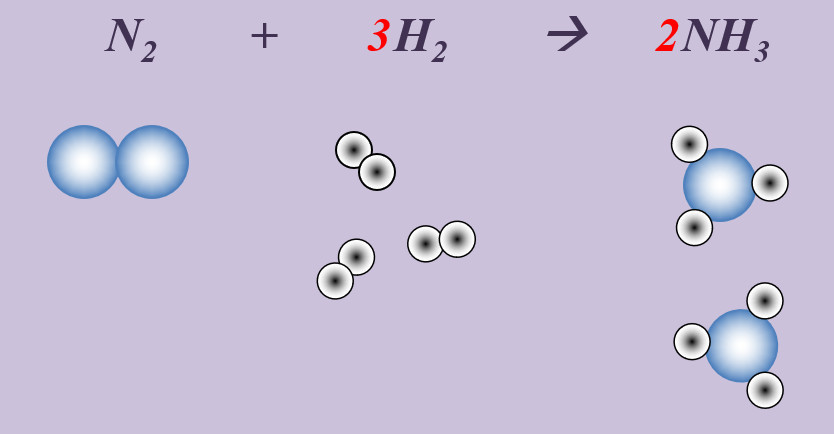
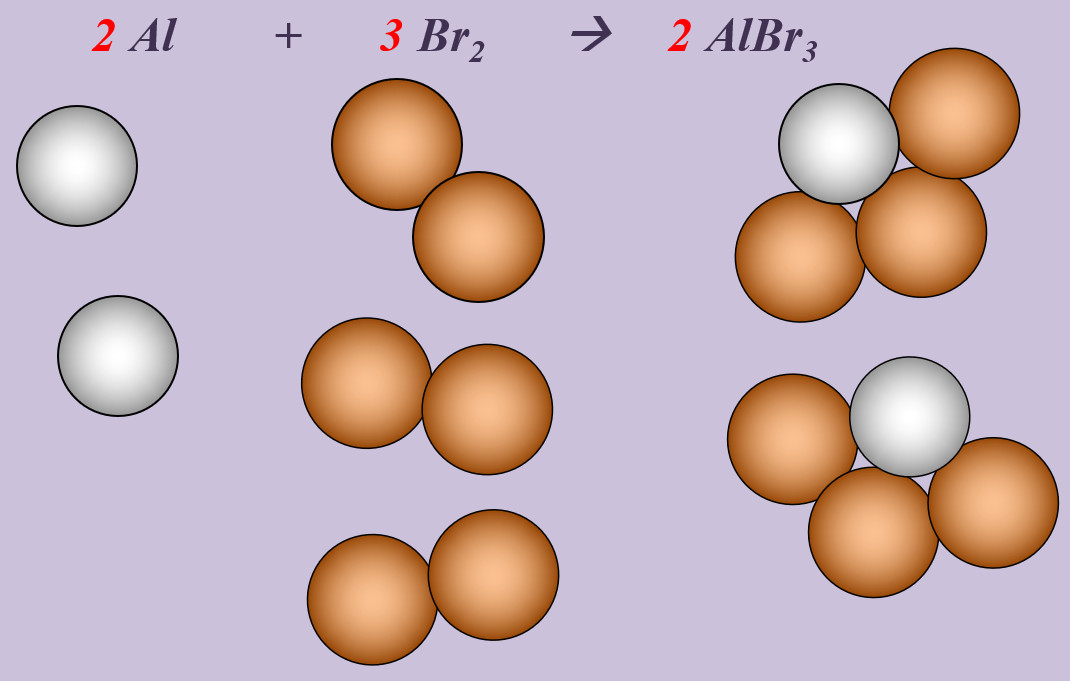
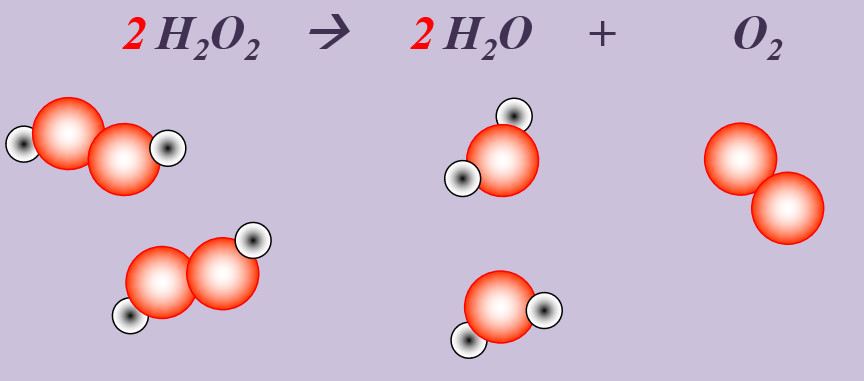
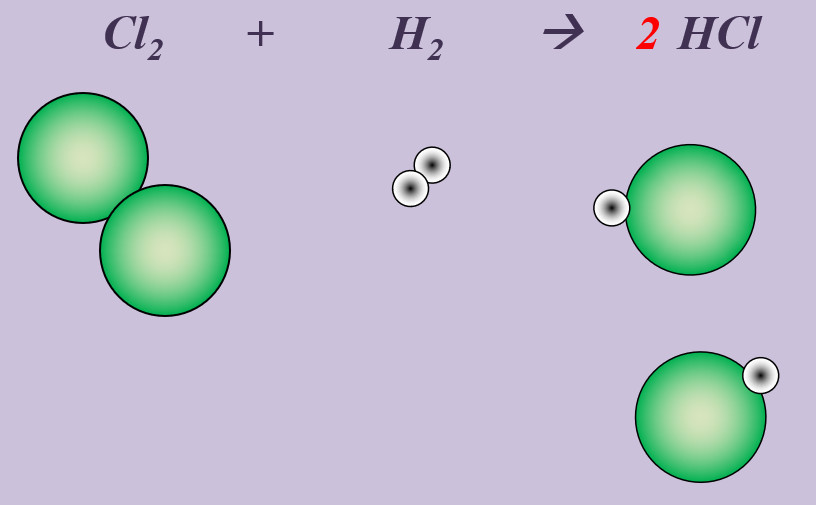
| '''Aufgaben:''' Stellt für die folgenden Reaktionen die chemische Gleichung auf. Gebt an, ob es sich um eine Synthese, Analyse oder Umsetzung handelt!<br>
| |
| <br>
| |
| * Eisenpulver und Schwefelpulver wird vermischt. Man taucht einen glühenden Nagel kurz in das Gemisch und es beginnt eine starke Reaktion. Nach und nach glüht das gesamte Gemisch auf. Am Ende liegt der Stoff Pyrit (FeS<sub>2</sub>) vor.
| |
| {{Lösung versteckt|
| |
| * '''Chemische Gleichung''': Fe + 2 S --> FeS<sub>2</sub>
| |
| * '''Grundtyp''': Synthese. Begründung: Aus '''mehreren Edukten''' wird '''ein Produkt'''
| |
| |Lösung|Lösung ausblenden}}<br>
| |
| <br>
| |
| * Quecksilberoxid (HgO) wird in einem Reagenzglas mit dem Bunsenbrenner stark erhitzt. Solange sich das RG in der BB-Flamme befindet, strömt Sauerstoff aus dem RG und es bilden sich am Rand kleine Quecksilbertröpfchen
| |
| {{Lösung versteckt|
| |
| * '''Chemische Gleichung''': 2 HgO --> 2 Hg + O<sub>2</sub><br>
| |
| * '''Grundtyp''': Analyse. Begründung: Aus '''einem Edukt''' werden '''mehrere Produkte'''
| |
| |Lösung|Lösung ausblenden}}<br>
| |
| <br>
| |
| * In einem RG befinden sich Wasser und ein Stück Magnesium-Band. Am oberen Ende ist das RG mit einem Stopfen verschlossen, in dem ein dünnes Glasrohr steckt. Das Wasser im RG wird vorsichtig erhitzt, so dass es verdampft und alle anderen Gase aus dem RG verbrennt. Es liegt also ein Stück Magensiumband in gasförmigem Wasser vor. Entzünden man das Magnesiumband dann an einer Stelle, reagiert es mit dem Wasser. Sobald die Reaktion gestartet ist, reagiert das gesamte Magnesiumband nach und nach auf der gesamten Länge unter Freisetzung großer Mengen von Licht und Wärme. Nach der Reaktion bleibt der der Stoff Magnesiumoxid (MgO) im RG übrig und während der Reaktion kann man zeigen, dass aus dem dünnen Glasrohr im Stopfen Wasserstoff entweicht.
| |
| {{Lösung versteckt|
| |
| * '''Chemische Gleichung''': Mg + H<sub>2</sub>O --> MgO + H<sub>2</sub><br>
| |
| * '''Grundtyp''': Umsetzung. Begründung: Aus '''mehreren Edukten''' werden '''mehrere Produkte'''
| |
| |Lösung|Lösung ausblenden}}<br>
| |
| <br>
| |
| Hier ein paar Videos, in denen ihr die chemischen Reaktionen dieser Einheit sehen könnt: <br>
| |
| Ein relativ ausführliches Video zur Synthese von Eisensulfid (Pyrit):<br>
| |
| {{#ev:youtube|8c01I9Pq0is}}<br>
| |
| <br>
| |
| Die Thermolyse von Quecksilberoxid:<br>
| |
| {{#ev:youtube|8jnLKkagFjw}}<br>
| |
| <br>
| |
| Die Umsetzung von Magnesium in Wasserdampf (mit lustiger Musik... YEAH!):
| |
| {{#ev:youtube|IQ8Tx0gWM1E|||||start=0&end=115}}<br>
| |
| <br>
| |
| '''Hausaufgabe (könnt ihr auch sofort erledigen):'''<br>
| |
| Entscheidet auf dem Arbeitsblatt, ob es sich bei den Reaktionen 1, 3, 5 und 7 auf der Vorderseite (links) und den Reaktionen 3, 8 und 10 auf der Rückseite (rechts) um eine Synthese, Analyse oder Umsetzung handelt.<br>
| |
| |Farbe= #607 | | |Farbe= #607 |
| |Rahmen= 0 | | |Rahmen= 0 |