8a 2022 23: Unterschied zwischen den Versionen
Aus RMG-Wiki
Markierung: Quelltext-Bearbeitung 2017 |
Markierung: Quelltext-Bearbeitung 2017 |
||
| (10 dazwischenliegende Versionen desselben Benutzers werden nicht angezeigt) | |||
| Zeile 4: | Zeile 4: | ||
|Titel=<span style="color:#900">'''Termine'''</span> | |Titel=<span style="color:#900">'''Termine'''</span> | ||
|Inhalt= | |Inhalt= | ||
* '''2. Schulaufgabe''': | * '''2. Schulaufgabe''': Montag, 19.06.23 <br> | ||
|Farbe= #900 | |Farbe= #900 | ||
|Rahmen= 0 | |Rahmen= 0 | ||
| Zeile 13: | Zeile 13: | ||
=== aktuelle Aufgaben zum Üben === | === aktuelle Aufgaben zum Üben === | ||
{{Box-spezial | {{Box-spezial | ||
| Zeile 61: | Zeile 19: | ||
Allgemein müsst ihr mit folgenden Größen umgehen können: | Allgemein müsst ihr mit folgenden Größen umgehen können: | ||
* Masse eines Stoffes: <math>m(X)</math>, Einheit: <math>g</math> (Gramm) | * Masse eines Stoffes: <math>m(X)</math>, Einheit: <math>g</math> (Gramm) | ||
* Die tatsächlich Anzahl von Teilchen eines Stoffes: <math>N(X)</math>, keine Einheit | |||
* Das Volumen eines (gasförmigen) Stoffes: <math>V(X)</math>, Einheit: <math>L</math> (Liter) | |||
* Stoffmenge eines Stoffes: <math>n(X)</math>, Einheit: <math>mol (Mol)</math> | |||
* molare Masse eines Stoffes: <math>M(X)</math>, Einheit <math>\frac{g}{mol} </math>, kann für Atome aus dem PSE abgeleitet werden | * molare Masse eines Stoffes: <math>M(X)</math>, Einheit <math>\frac{g}{mol} </math>, kann für Atome aus dem PSE abgeleitet werden | ||
* Die Avogadrokonstante <math>N_A = 6,022 \cdot 10^{23} \frac{1}{mol}</math> | * Die Avogadrokonstante <math>N_A = 6,022 \cdot 10^{23} \frac{1}{mol}</math> | ||
* molares Volumen eines (gasförmigen) Stoffes bei Standardbedingungen (273°C und 1013hPa): <math>V_m = 22,4</math>, Einheit <math>\frac{L}{mol} </math> | |||
<br> | <br> | ||
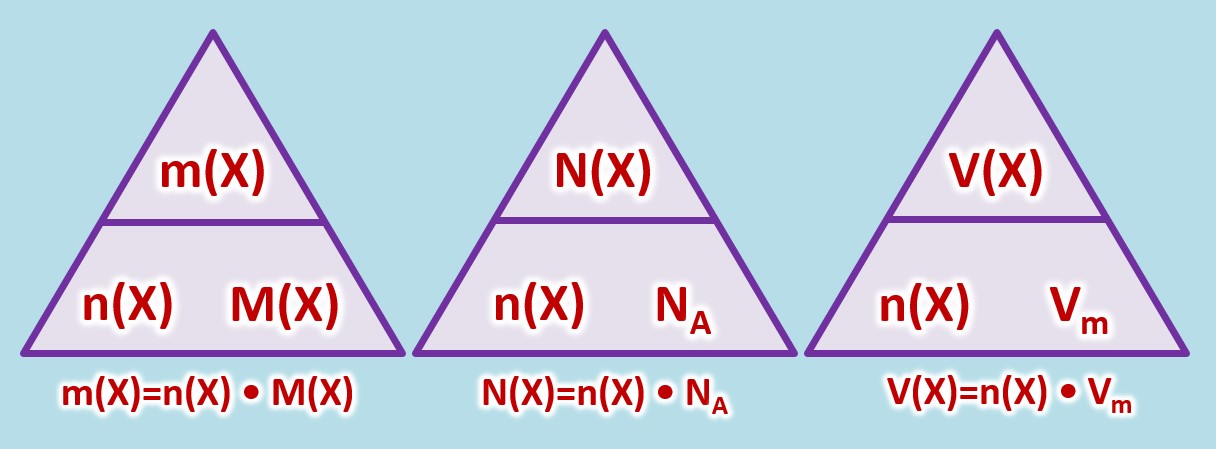
Es gelten die folgenden Zusammenhänge: | Es gelten die folgenden Zusammenhänge: | ||
[[Datei: | [[Datei:C8NTG_ReMiMoGr_3ZH_3ecke.jpg]]<br> | ||
<br><br> | <br><br> | ||
|Farbe= #607 | |Farbe= #607 | ||
| Zeile 404: | Zeile 364: | ||
|Tipp|Lösung ausblenden}} | |Tipp|Lösung ausblenden}} | ||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
{{Box-spezial | |||
|Titel=<span style="color:#080">'''Abschlussaufgaben zum Thema Salze'''</span> | |||
|Inhalt= | |||
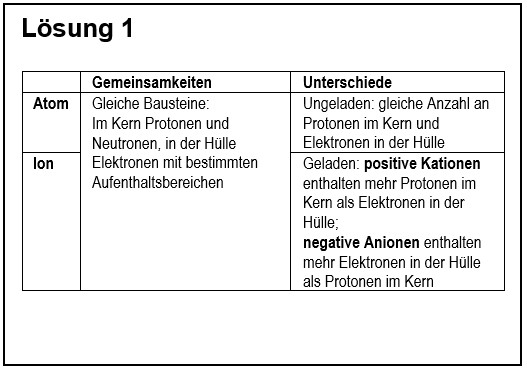
1. Vergleiche in übersichtlicher Form ein '''Atom''' mit einem '''Ion'''! | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg1.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
2. Beschreibe mit Hilfe einer chemischen Gleichung die Bildung von Cäsiumchlorid aus den Elementen1 Stelle vorher die Gleichungen zur Bildung der Ionen aus den Elementen auf! | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg2.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
3. Wähle aus den folgenden Eigenschaften diejenigen aus, die sich mit dem Ionengitter von Salzen erklären lassen: Verformbarkeit - große Bindungskräfte - Löslichkeit - elektrische Leitfähigkeit - Sprödigkeit - niedrige Siedetemperatur - Reaktionsträgheit. | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg3.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
4. Beziehe zu folgender Aussage begründet Stellung: Beim Schmelzen von Kaliumbromid müssen Ionen entstanden sein, weil die Schmelze elektrisch leitfähig ist. | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg4.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
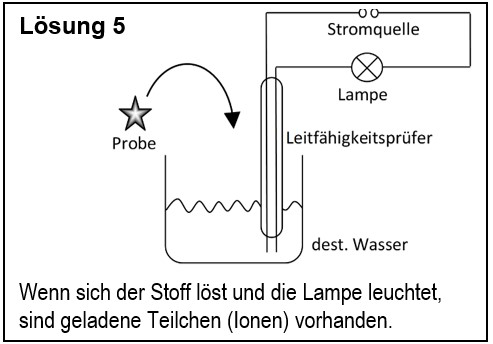
5. Entwirf einen Versuch, mit dem man zeigen kann, dass ein unbekannter Feststoff aus Ionen besteht. | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg5.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
6. Formuliere (mit Ionengleichungen) die Bildung von folgenden Salzen: Mg<sub>3</sub>N<sub>2</sub>, CaO, KI, BaCl<sub>2</sub> und Aluminiumfluorid | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg6.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
7. Sortiere folgende Teilchen nach abnehmender Teilchengröße: Li<sup>+</sup>, K, S<sup>2-</sup>, Na<sup>+</sup> | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg7.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
8. Ermittle das Zahlenverhältnis der Ionen in folgenden Salzen: Kaliumsulfid, Aluminiumoxid, Natriumbromid, Calciumoxid. | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_AbschlA_Salze_Lsg8.jpg]] | |||
|Lösungsvorschlag|Lösung ausblenden}} | |||
|Farbe= #080 | |Farbe= #080 | ||
|Rahmen= 0 | |Rahmen= 0 | ||
| Zeile 428: | Zeile 430: | ||
* 1. Übung: Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Flammenfärbung.pdf| Hier klicken]] | * 1. Übung: Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Flammenfärbung.pdf| Hier klicken]] | ||
* 2. Übung: Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Flammenfärbung2.pdf| Hier klicken]] | * 2. Übung: Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Flammenfärbung2.pdf| Hier klicken]] | ||
''' | '''20.03. - 08.05.: Fällungsreaktionen''' | ||
* Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung_ClBrI_V2.pdf| Hier klicken]] <span style="color:#F00">neue Version hochgeladen am 14.04., Fehler ausgebessert</span><br> | * Anleitung + Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung_ClBrI_V2.pdf| Hier klicken]] <span style="color:#F00">neue Version hochgeladen am 14.04., Fehler ausgebessert</span><br> | ||
* Erklärung der Fällungsreaktion auf Teilchenebene als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung_Teilchenebene.pdf| Hier klicken]] | * Erklärung der Fällungsreaktion auf Teilchenebene als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung_Teilchenebene.pdf| Hier klicken]] | ||
* Unterscheidung von Silberchlorid-, Silberbromid und Silberiodid-Niederschlag als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung2_U_ClBrI.pdf| Hier klicken]] | * Unterscheidung von Silberchlorid-, Silberbromid und Silberiodid-Niederschlag als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung2_U_ClBrI.pdf| Hier klicken]] | ||
* Fällung und Unterscheidung von Carbonat- und Sulfat-Ionen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung_CarboSulf.pdf| Hier klicken]] | * Fällung und Unterscheidung von Carbonat- und Sulfat-Ionen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Fällung_CarboSulf.pdf| Hier klicken]] | ||
'''15.05-22.05.: Ionenlotto''' | |||
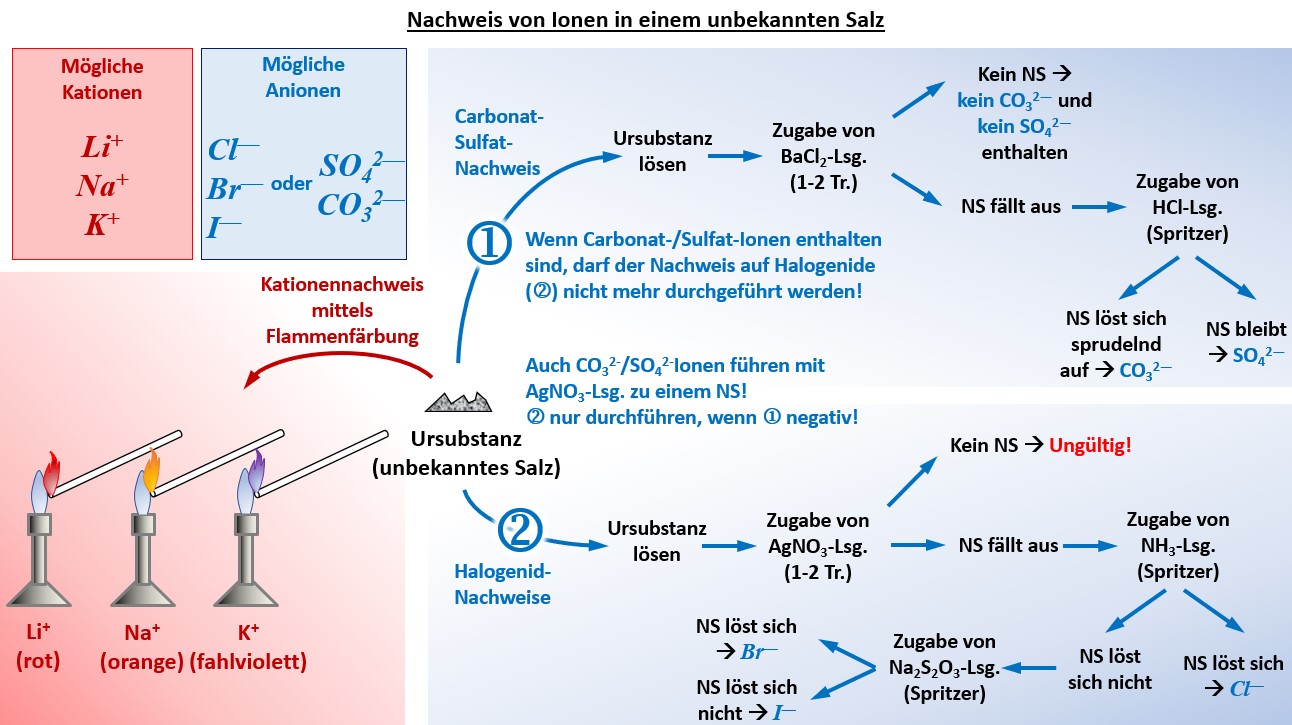
* Im Unterricht gestellte Aufgabe: "Identifiziere in der unbekannten Salzprobe die vorhanden Kationen und Anionen! Die Salzprobe enthält eines der folgenden Kationen: K<sup>+</sup>, Na<sup>+</sup>, Li<sup>+</sup> und eines der folgenden Anionen: Cl<sup>-</sup>, Br<sup>-</sup>, I<sup>-</sup>, CO<sub>3</sub><sup>2-</sup>, SO<sub>4</sub><sup>2-</sup>. Fertige ein sauberes Protokoll an, in dem vor allem die Durchführung und das Ergebnis dargestellt wird!" | |||
* Zwei zu dieser Aufgabe passende Muster-Protokoll als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_Ionenlotto_ML.pdf| Hier klicken]] | |||
* Übersicht über die praktisch durchzuführenden Schritte: | |||
{{Lösung versteckt| | |||
[[Datei:G9_C8_Ü_011_NachweisGesamt_V2.jpg]]<br> | |||
|Grafische Darstellung einblenden|Lösung ausblenden}} | |||
<br> | |||
'''Montag, 03.07.''' | |||
* Eigenschaften von Alkanen (einfache Kohlenwasserstoffe) | |||
* Versuchsprotokoll zum Herunterladen als .pdf-Datei: [[Spezial:FilePath/G9_C8_VProt_EigenschaftenAlkane.pdf| Hier klicken]] | |||
|Farbe= #30F | |Farbe= #30F | ||
|Rahmen= 0 | |Rahmen= 0 | ||
| Zeile 441: | Zeile 453: | ||
===Lernstoff für angekündigte Leistungsnachweise=== | ===Lernstoff für angekündigte Leistungsnachweise=== | ||
{{Box-spezial | |||
|Titel= | |||
|Inhalt= Schulaufgabe am 19.06. | |||
Neben den Hefteinträgen und dem oben genannten Grundwissen, eignen sich folgende Seiten im Buch (Galvani - Chemie 8) zur Vorbereitung auf die Schulaufgabe: | |||
* S. 146 - 147: Aufbau von Salzen | |||
* S. 150 - 151: Verhältnisformeln | |||
* S. 152 - 153: Periodensystem der Atome und Ionen | |||
* S. 154 - 155: Eigenschaften von Salzen | |||
* S. 162 - 163 : Ionennachweise | |||
* S. 164: Flammenfärbung | |||
* S. 174 - 176: Metalle und ihre Eigenschaften | |||
* S. 120 - 121: Atommasse | |||
* S. 122 - 124: Stoffmenge, molare Masse und molares Volumen | |||
|Farbe= #30F | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFF | |||
|Hintergrund= #DFF | |||
}} | |||
{{Box-spezial | {{Box-spezial | ||
|Titel= | |Titel= | ||
Aktuelle Version vom 3. Juli 2023, 13:23 Uhr
Chemie
aktuelle Aufgaben zum Üben
Online-Unterricht am 09.01.2023
Grundwissen
Versuchsprotokolle
Lernstoff für angekündigte Leistungsnachweise