Benutzer:Thomas Lux: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
Keine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
||
| Zeile 21: | Zeile 21: | ||
{{Lösung versteckt| | {{Lösung versteckt| | ||
Das sind die Elektronen, die sich bei Atomen eines bestimmten Elements auf der äußersten Schale befinden. | |||
|Lösung 1|Lösung ausblenden}} | |Lösung 1|Lösung ausblenden}} | ||
| Zeile 27: | Zeile 27: | ||
{{Lösung versteckt| | {{Lösung versteckt| | ||
Ca: 2 VE, Li: 1 VE, I: 7 VE | |||
|Lösung 2|Lösung ausblenden}} | |Lösung 2|Lösung ausblenden}} | ||
| Zeile 33: | Zeile 33: | ||
{{Lösung versteckt| | {{Lösung versteckt| | ||
Die Anzahl der VE entspricht der Hauptgruppen-Nr. im PSE. | |||
|Lösung 3|Lösung ausblenden}} | |Lösung 3|Lösung ausblenden}} | ||
* Bestimme die chemische Formel des Salzes Berylliumbromid! | * Bestimme die chemische Formel des Salzes '''Berylliumbromid'''! | ||
{{Lösung versteckt| | {{Lösung versteckt| | ||
< | <Beryllium besitzt 2 VE. Um Edelgaskonfiguration zu erreichen, muss es diese beiden abgeben. Es entstehen Be<sup>2+</sup>-Ionen. Brom besitzt 7 VE. Um Edelgaskonfiguration zu erreichen muss es ein Elektron aufnehmen. Es entstehen Br<sup>-</sup>-Ionen. Damit ein neutrales (nicht geladenes) Salz entsteht und keine Elektronen verloren gehen oder übrig bleiben, müssen immer zwei Bromid-Atome mit einem Beryllium-Atom reagieren. Die Formel des entstehenden Salzes lautet dann BeBr<sub>2</sub> | ||
|Lösung 4|Lösung ausblenden}} | |Lösung 4|Lösung ausblenden}} | ||
Das genügt | Das genügt als Wiederholung. Jetzt zum yt-Video (10:06 min.): [https://www.youtube.com/watch?v=PsR-HRiGAzA Hier klicken] | ||
|Farbe= #607 | |Farbe= #607 | ||
|Rahmen= 0 | |Rahmen= 0 | ||
| Zeile 48: | Zeile 48: | ||
|Hintergrund= #DCF | |Hintergrund= #DCF | ||
}} | }} | ||
{{Lösung versteckt| | {{Lösung versteckt| | ||
Version vom 21. März 2020, 11:57 Uhr
Hallo! Meine Benutzer-Seite ist eine Art Steinbruch, in der hauptsächlich für mich wichtige Vorlagen liegen und einige Tests laufen...
Zu den Arbeitsaufträgen (Corona)
Zur Schulentwicklungs-Testseite
Zur Studien- und Berufsorientierung
Zur Studien- und Berufsorientierung der Mittelstufe
Biologie-Rätsel des Monats
Error: h5p.org is not an authorized iframe site.<script src="https://h5p.org/sites/all/modules/h5p/library/js/h5p-resizer.js" charset="UTF-8"></script>
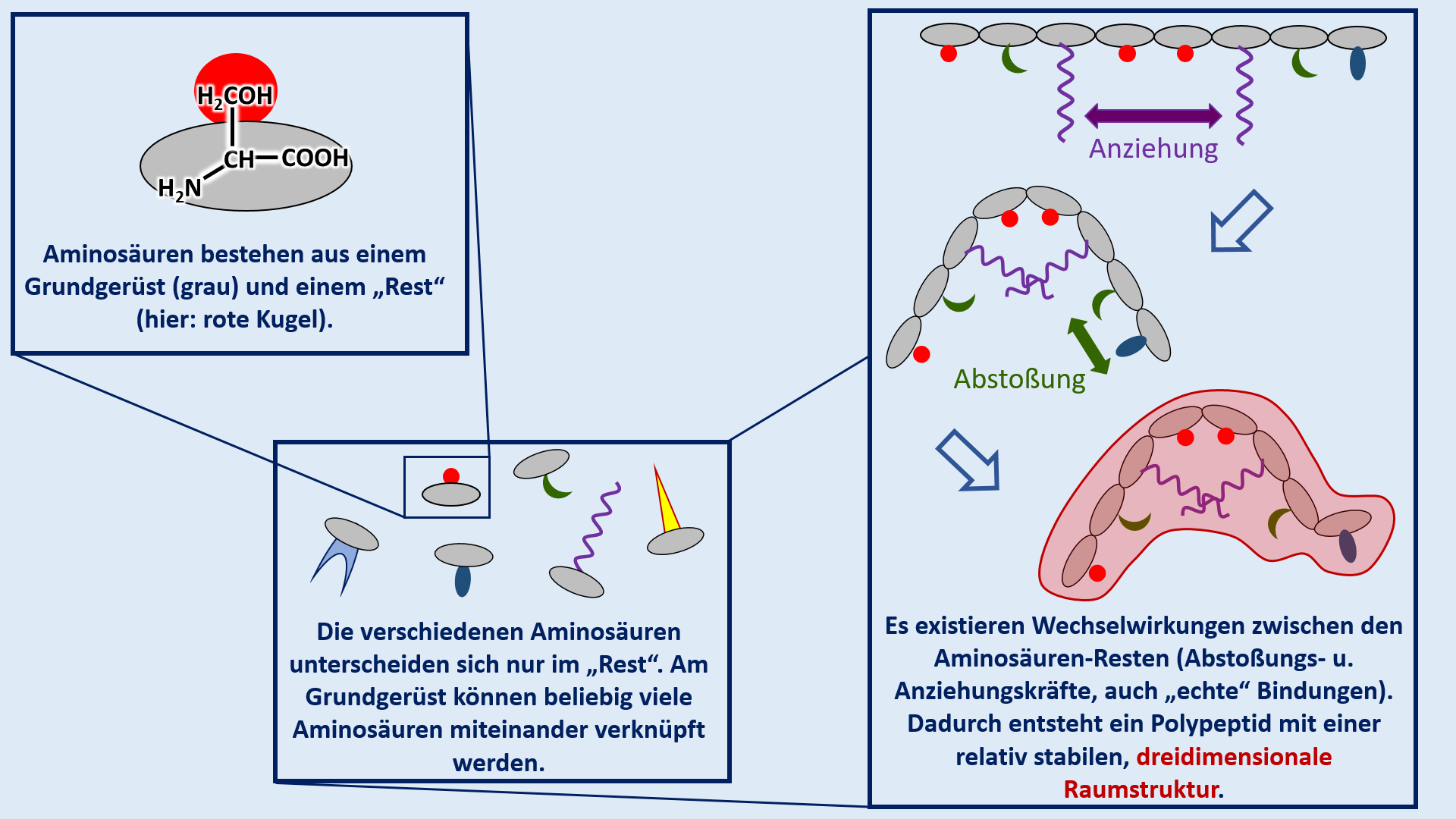
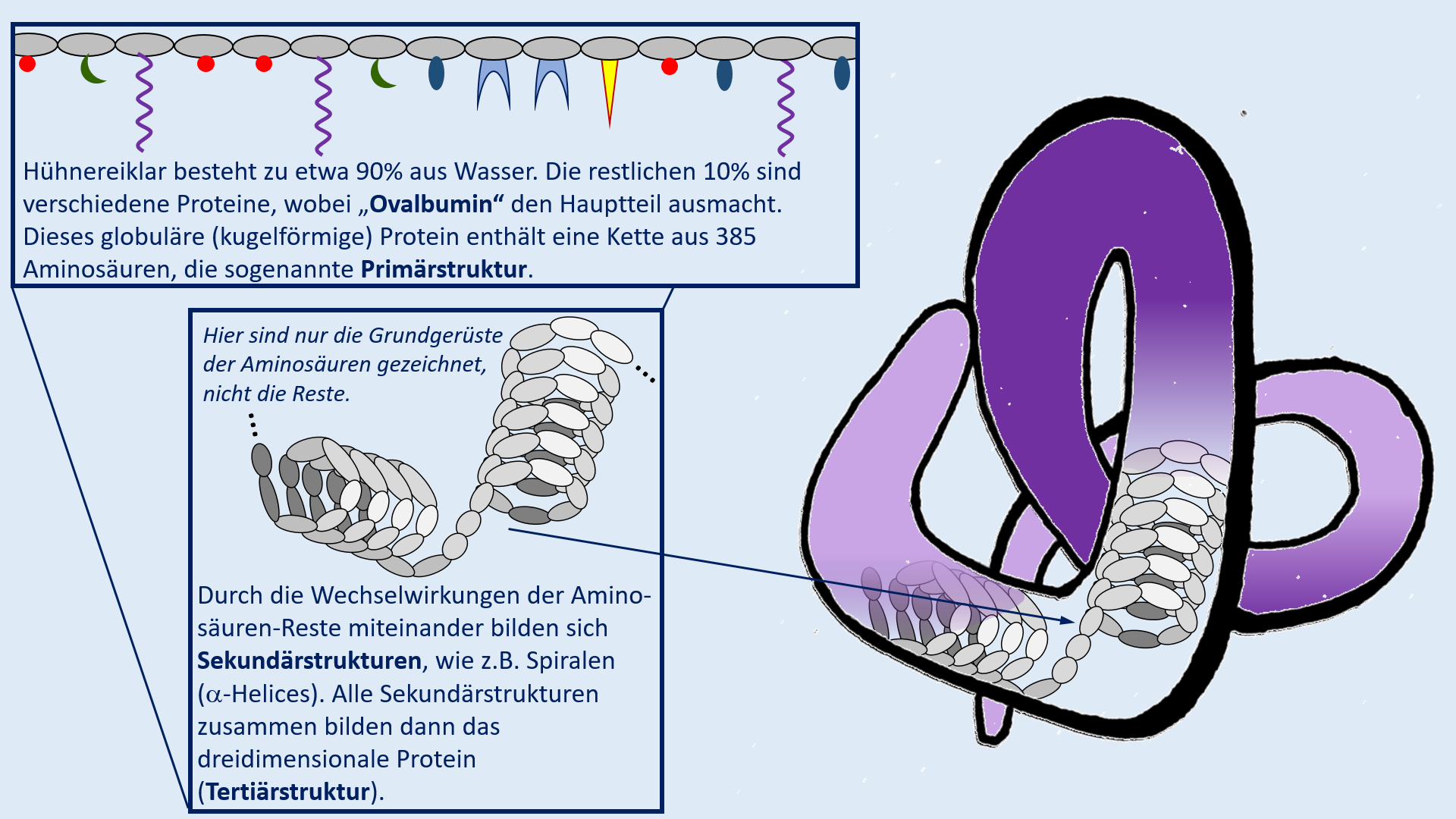
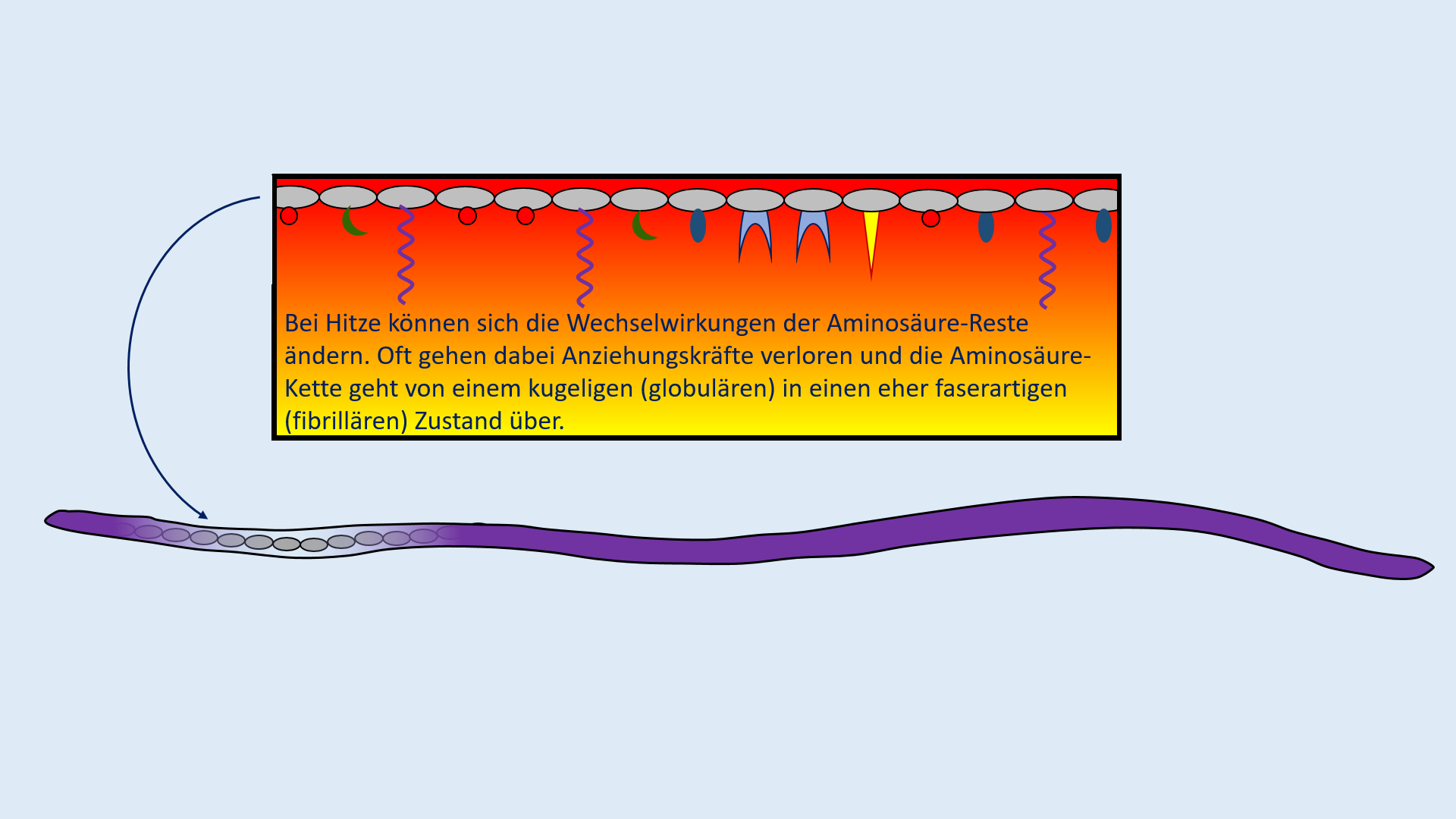
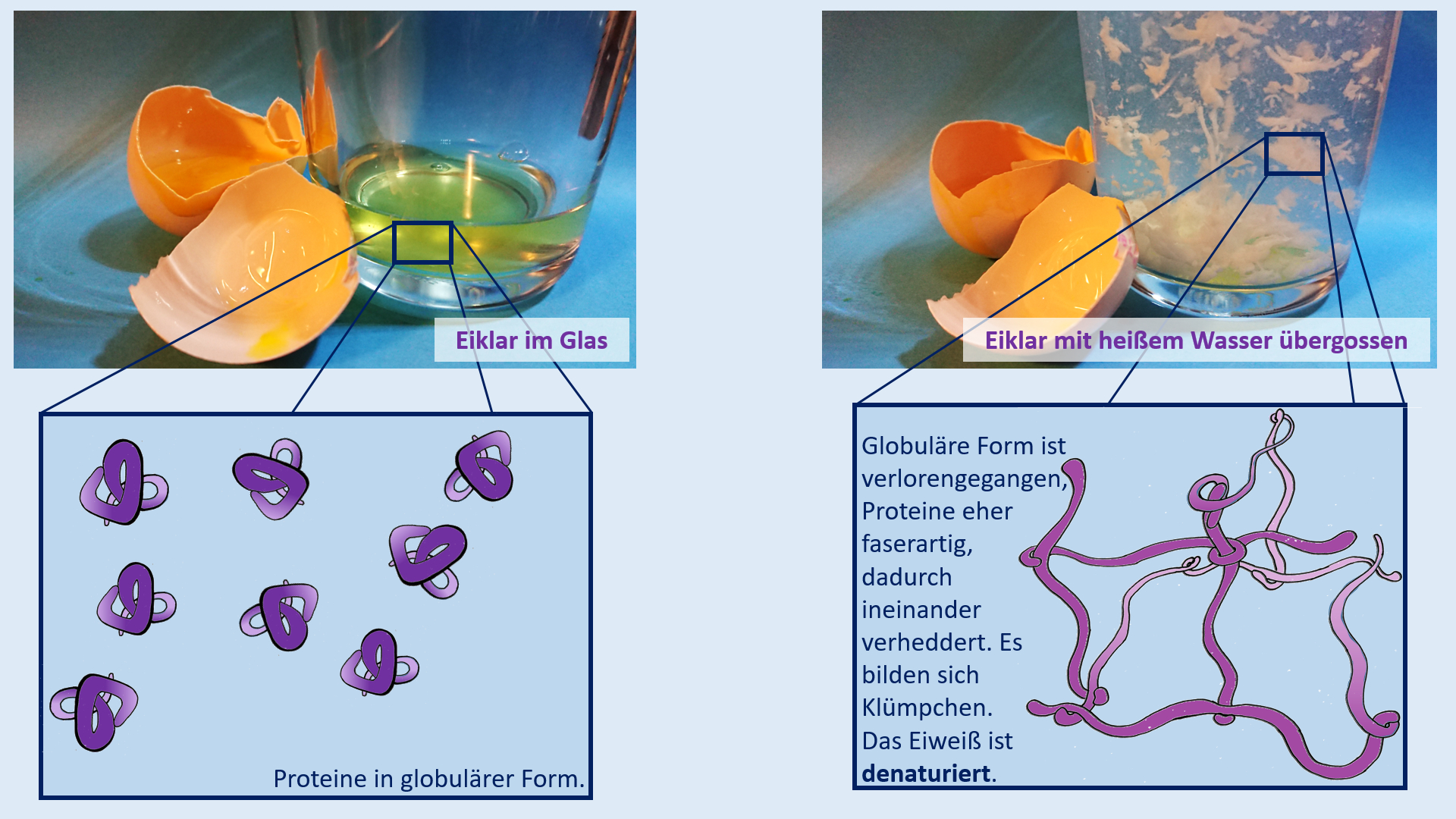
Test. Einheit: Eiweiße
Test Schulentwicklungsteam
|
Respekt und Werte-Erziehung
|
Individuelle Förderung und Individualisierung |
Berufswahlkompetenz
|
Kommunikation
|
Respekt und Werte-Erziehung
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
Individuelle Förderung und Individualisierung
- im Moment keine interessanten Fortbildungen zu diesem Thema -
Berufswahlkompetenz
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
Kommunikation
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
- Hochinteressante Fortbildung zum Thema Resilienz, bei uns am RMG! 24.10., 19:00 Uhr
- Klicke hier auf diesen [link]
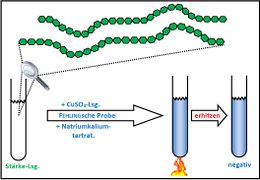
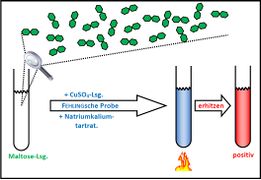
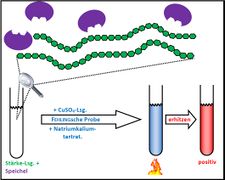
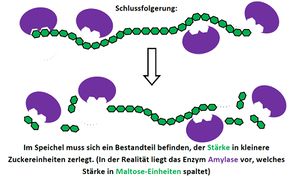
Biologie
Visualisierung der Unterrichtsversuche zum Thema "Verdauungsprozesse im Mund".
Chemie
Das Anfertigen eines Versuchsprotokolls stellt eine wichtige Grundfertigkeit dar. Auch im Hinblick auf das spätere Erstellen einer Seminararbeit. In den naturwissenschaftlichen Fächern ist die typische Gliederung einer Arbeit nämlich einem Versuchsprotokoll ganz ähnlich. Hier zwei gelungene Beispiele:
neue Überschrift
Termine
|
Externe Links- im Moment keine externen links -
|
Termine
|
Externe Links
|
Hefteinträge
1. Evolution
1.1 Ein kurzer historischer Abriss zur Entwicklung des Evolutionsgedankens
Neu, 04.10. Buch S. 17, 28-31 (das Buch ist hier sehr ausführlich) + Hefteintrag:
1.4 Darwins Evolutionstheorie +
Stoff aus der 11. Klasse
Eine Übersicht über wichtige Inhalte des Kapitels "Populationswachstum und Biodiversität" aus der 11. Jahrgangsstufe liefern die folgenden Einträge: