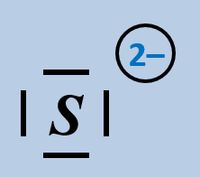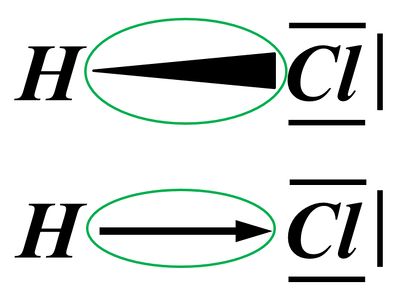10d 2019 20/Chemie: Unterschied zwischen den Versionen
KKeine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
Markierung: Quelltext-Bearbeitung 2017 |
||
| (16 dazwischenliegende Versionen desselben Benutzers werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
== | Diejenigen unter euch, die in der Oberstufe Chemie belegt haben, sollten diese Aufgaben wirklich bearbeiten. Bitte meldet mir Unklarheiten auch möglichst zeitnah zurück. Für diejenigen, die kein Chemie belegt haben, können die Aufgaben trotzdem ganz nützlich sein. Vor allem in der ersten Hälfte der elften Klasse in Biologie wird oft auf die chemischen Grundlagen bestimmter Stoffwechselreaktionen zurückgegriffen. | ||
[[Datei: | <br> | ||
<br> | |||
==Arbeitsauftrag Chemie für den 27.05.== | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Verbesserung der Hausaufgabe'''</span> | |||
|Inhalt= | |||
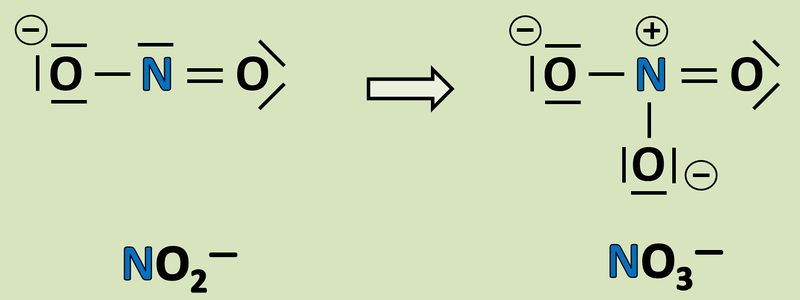
Wendet das gelernte Verfahren zur Bestimmung der Oxidationszahlen auf folgende Reaktion an und gebt an, wie viele Elektronen hier frei werden oder aufgenommen werden! <br> | |||
[[Datei:Redox1_AA1_NO2_NO3.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
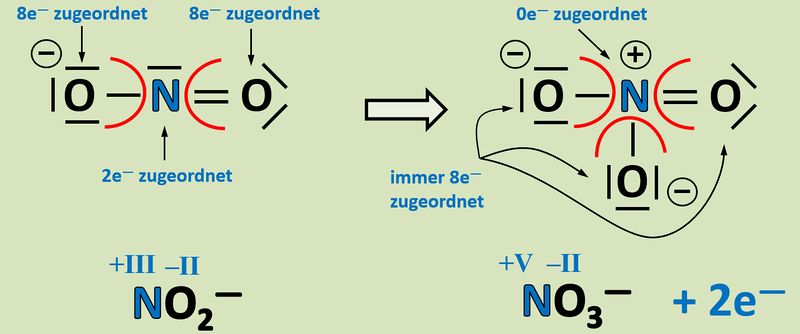
'''Oxidation''': Es werden zwei Elektronen abgegeben.<br> | |||
[[Datei:Redox1_ML1_Nitrit_Nitrat.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
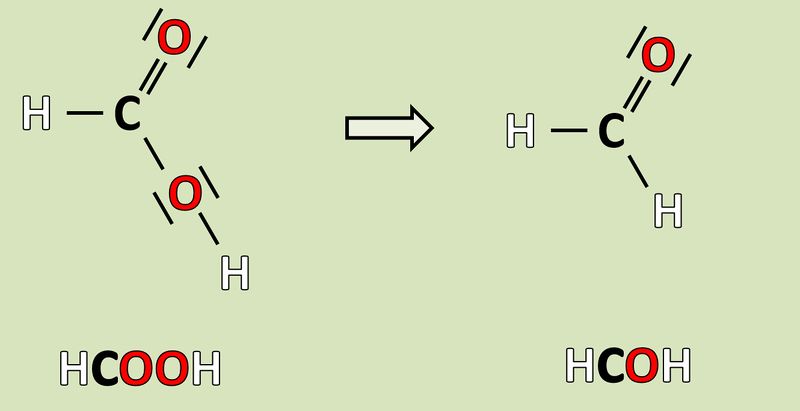
[[Datei:Redox1_AA1_HCOOH_HCOH.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
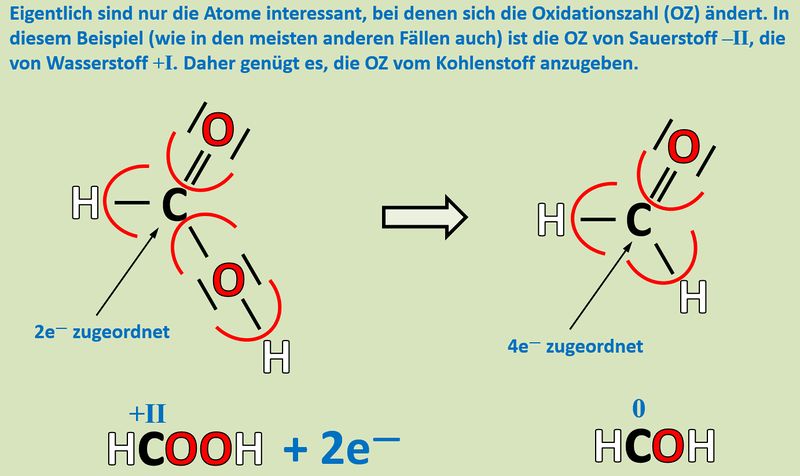
'''Reduktion''': Es werden zwei Elektronen aufgenommen.<br> | |||
[[Datei:Redox1_ML3_Säure_Aldehy.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
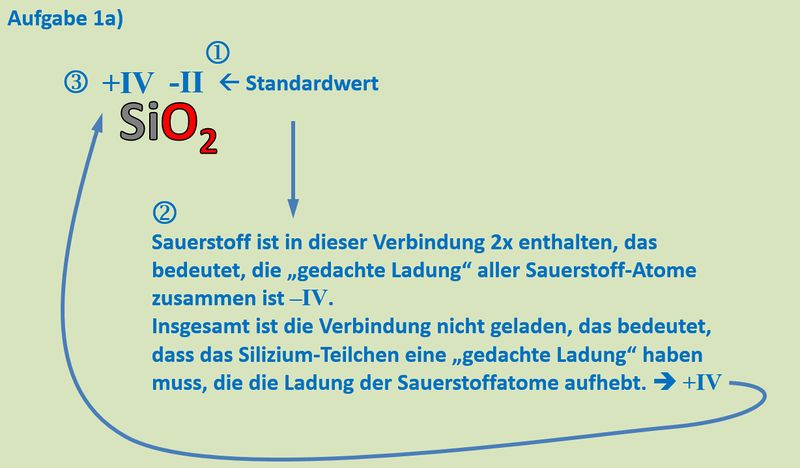
Buch, S. 75 Aufgabe 1a<br> | |||
{{Lösung versteckt| | |||
[[Datei:Redox1_MLHA_1a.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
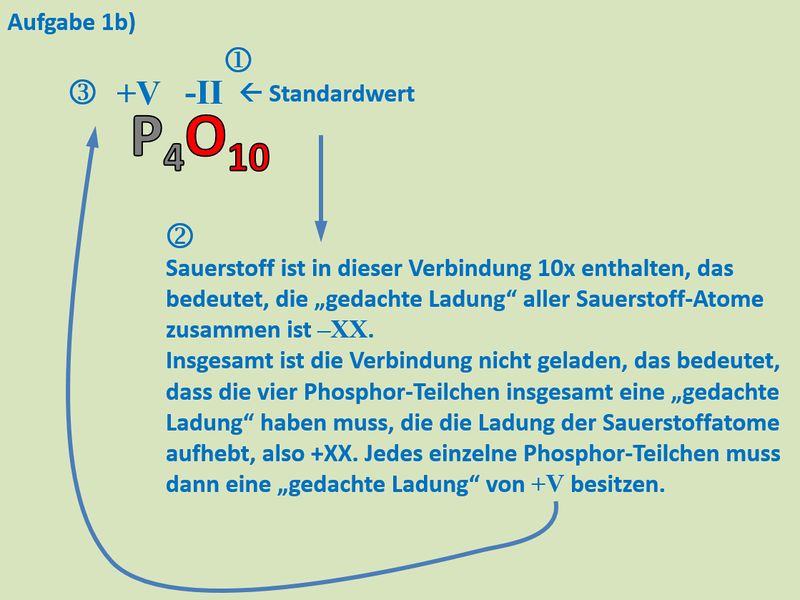
Buch, S. 75 Aufgabe 1b<br> | |||
{{Lösung versteckt| | |||
[[Datei:Redox1_MLHA_1b.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
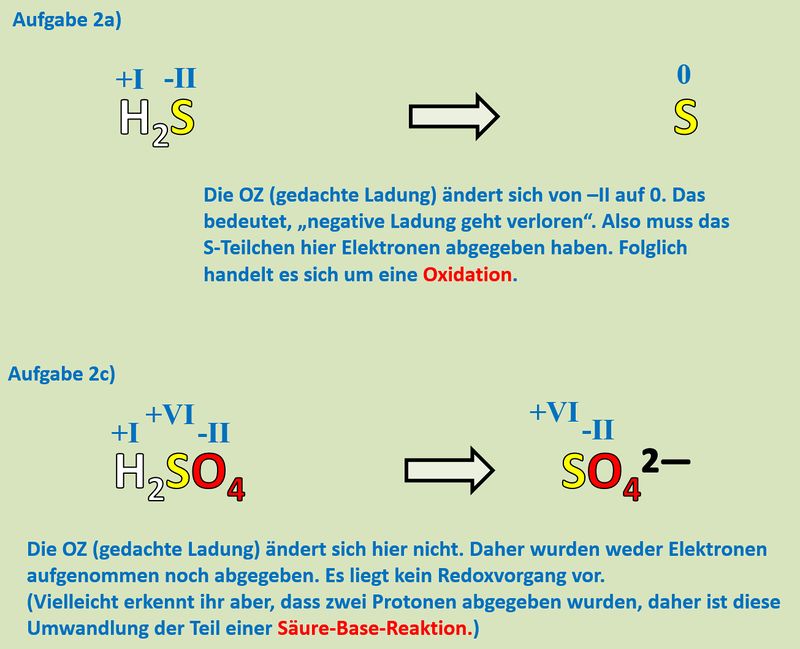
Buch, S. 75 Aufgabe 2a und c<br> | |||
{{Lösung versteckt| | |||
[[Datei:Redox1_MLHA_2ac.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
==Arbeitsauftrag Chemie für den 25.05.== | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Redox-Reaktionen'''</span> | |||
|Inhalt= | |||
In der letzten Einheit habt ihr einen typischen Reaktionstyp kennengelernt: Die '''Säure-Base-Reaktion'''. Dabei wird ein '''Proton''' von einem Teilchen auf ein anderes übertragen. Heute soll es um einen Reaktionstyp gehen, bei dem '''Elektronen''' von einem Teilchen auf ein anderes übertragen werden. Ihr kennt solche Reaktionen bereits von der Bildung von Salzen aus den Elementen. Dabei gibt das Metall Elektronen ab. Diese Teilreaktion wird als '''Oxidation''' bezeichnet. Das Nichtmetall nimmt die Elektronen auf. Diese Teilreaktion wird als '''Reduktion''' bezeichnet. Beide Teilreaktionen können ähnlich wie bei Säure-Base-Reaktionen nur gemeinsam ablaufen. Die Elektronen können nicht irgendwo hin ins Nirvana abgegeben werden oder "aus der Luft" aufgenommen werden. Es muss immer der passende Partner vorhanden sein. Beide Teilreaktionen, die also immer zusammen ablaufen werden als '''Redox-Reaktion''' bezeichnet. <br> | |||
Zur Vereinfachung ist es aber tatsächlich üblich, beide Teilreaktionen getrennt voneinander zu betrachten, mit Elektronen die bei der Oxidation "herauskommen" und Elektronen, die bei der Reduktion "irgendwoher" aufgenommen werden.<br> | |||
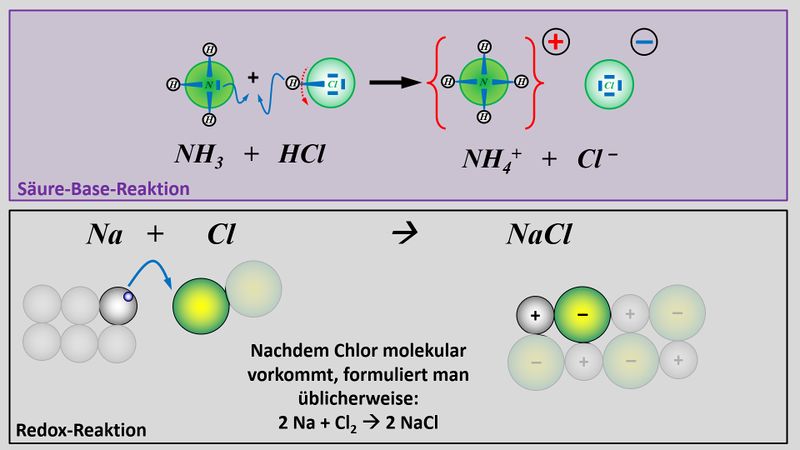
Zum Vergleich hier noch einmal eine Säure-Base-Reaktion und eine Redoxreaktion in bildlicher Darstellung:<br> | |||
[[Datei:Redox1_VGL_SäBa_Redox.jpg|800px]]<br> | |||
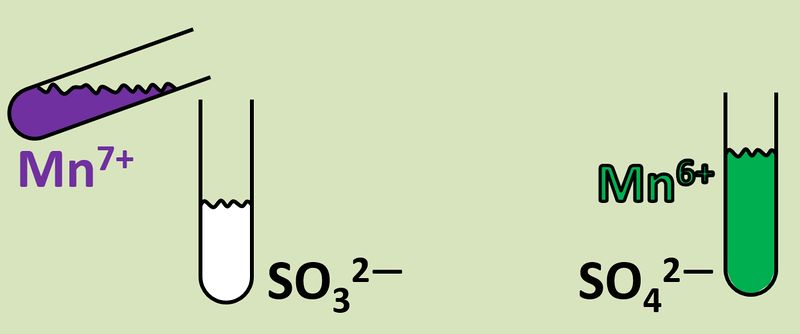
Im oberen Beispiel ist bei der Bildung von Natriumchlorid sehr einfach zu erkennen, wer die Elektronen abgibt (das Na-Atom) und wer sie aufnimmt (das Cl-Atom). Im folgenden Beispiel ist das nicht so einfach: Eine violette Permanganat-Lsg. (die vereinfacht Mn<sup>7+</sup>-Ionen enthält), die man in eine bestimmte Sulfit-Lsg. tropft, färbt sich grün (was auf Mn<sup>6+</sup>-Ionen zurückzuführen ist). Gleichzeitig tauchen im Reagenzglas Sulfat-Ionen auf: <br> | |||
[[Datei:Redox1_VMn7zuMn6.jpg|800px]]<br> | |||
Dass die Mn<sup>7+</sup>-Ionen offensichtlich ein Elektron aufgenommen haben (also eine Reduktion vorliegt), ist leicht an der Ladung zu erkennen. Aber woher kommt dieses Elektronen?<br> | |||
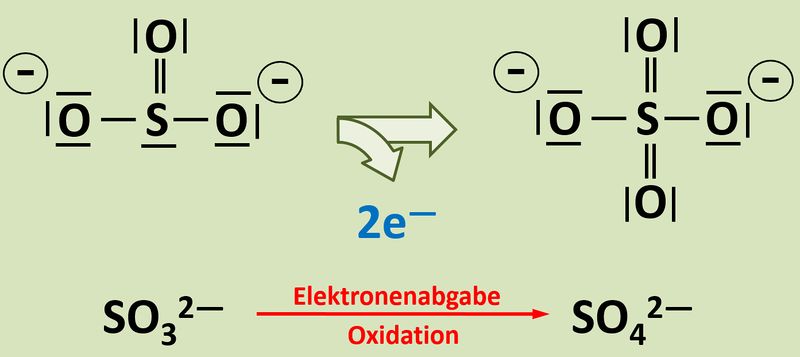
Zunächst einmal: In dem dargestellten Versuch sind noch eine Reihe weiterer Teilchen beteiligt, aber die spielen hier keine Rolle. Das Elektron stammt tatsächlich aus der Reaktion vom Sulfit zum Sulfat: <br> | |||
[[Datei:Redox1_So3zuSo4_Blanc.jpg|800px]]<br> | |||
Woher soll man erkennen, dass diese Reaktion Elektronen liefert, also eine Oxidation stattfindet?<br> | |||
Der Trick besteht nun darin auch Moleküle formal (also "nicht in echt") in Ionen zu zerlegen. Denn bei Ionen zeigt eine sich verändernde Ladung sehr klar an, ob Elektronen aufgenommen oder abgegeben wurden.<br> | |||
Um diese Zerlegung vorzunehmen, betrachtet man alle bindenden Elektronenpaare in einem Molekül und teilt sie formal demjenigen Bindungspartner zu, der die höhere Elektonegativität (EN) hat. Nur bei exakt gleichen Partnern bekommt jeder ein Elektron des Paares zugeordnet.<br> | |||
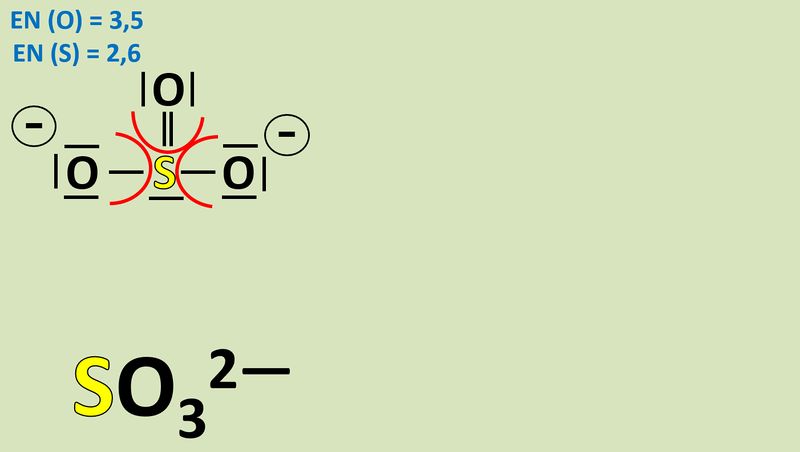
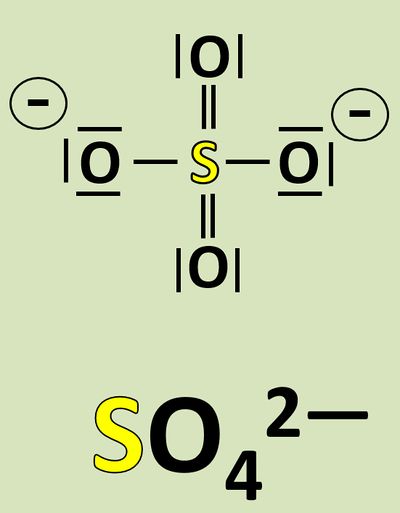
Bsp.: Sulfit-Ion:<br> | |||
[[Datei:Redox1_Sulfit_OZbestimmen_1.jpg|800px]]<br> | |||
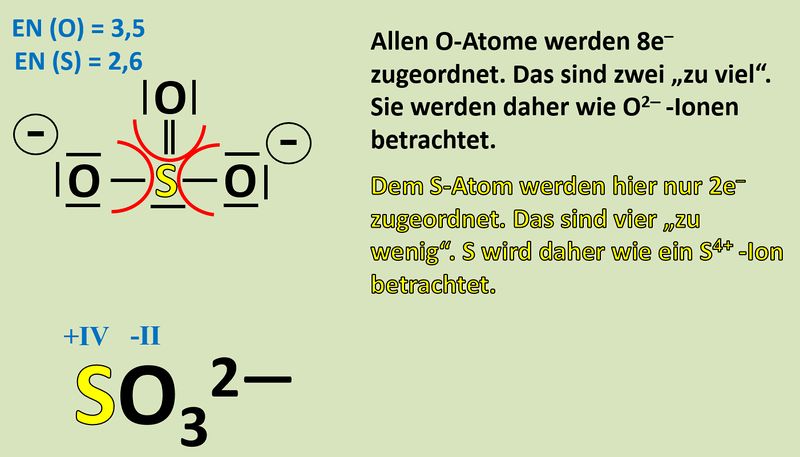
Nun zählt man die Elektronen, die jedem Atom auf diese Weise zugeordnet wurden und vergleicht diese Anzahl mit der Anzahl an Valenzelektronen, die dieses Atom laut PSE haben sollte. Liegen mehr Elektronen vor als "normal" entspricht die überschüssige Anzahl einer negativen Ladung, liegen weniger Elektronen vor, entspricht die fehlende Anzahl einer positiven Ladung. Man spricht allerdings nicht von einer "Ladung", sondern von der Oxidationszahl, die in der Schule üblicherweise als römische Ziffer angegeben wird (mit dem entsprechenden Vorzeichen).<br> | |||
Bsp.: Sulfit-Ion:<br> | |||
[[Datei:Redox1_Sulfit_OZbestimmen_2.jpg|800px]]<br> | |||
<br> | |||
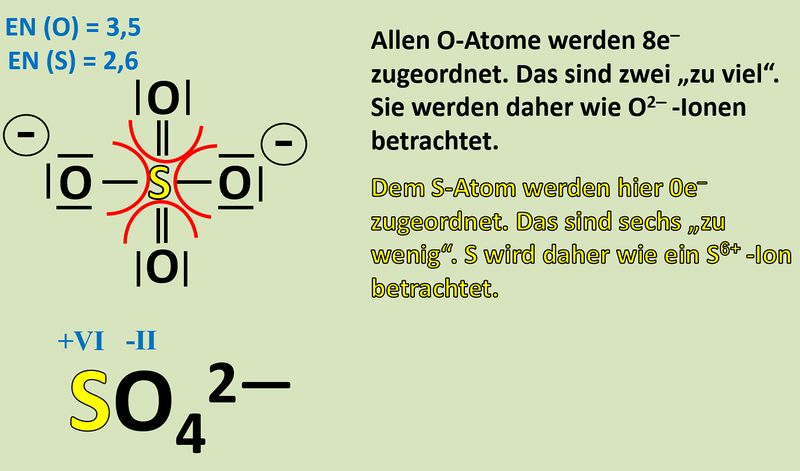
Wendet dieses Verfahren auf das Sulfat-Teilchen an:<br> | |||
[[Datei:Redox1_Sulfat_OZbestimmen_0.jpg|400px]]<br> | |||
{{Lösung versteckt| | |||
[[Datei:Redox1_Sulfat_OZbestimmen.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
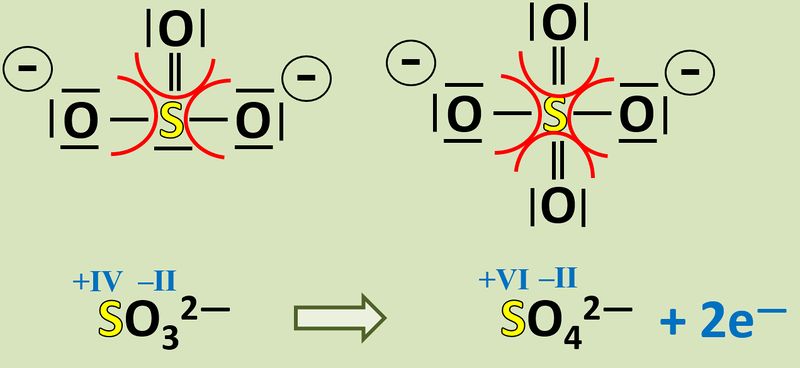
Vergleicht nun Sulfit mit Sulfat. Jetzt kann man besser erkennen, woher die Elektronen für die Reduktion von Mn<sup>7+</sup>-Ionen zu Mn<sup>6+</sup>-Ionen gekommen sind! | |||
<br> | |||
{{Lösung versteckt| | |||
[[Datei:Redox1_Sulfit_zzu_Sulfat_EFluss.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
Manche von euch werden jetzt sagen: "Ja gut... aber woher kommt denn das vierte Sauerstoff-Atom beim Sulfat?<br> | |||
<br> | |||
Sehr gute Frage! - Das ist aber eine andere Baustelle. Wir bleiben heute nur bei dem Problem: Woran erkennt man, wie viele Elektronen bei der Reaktion von Molekülen frei werden (Oxidation) oder aufgenommen werden (Reduktion).<br> | |||
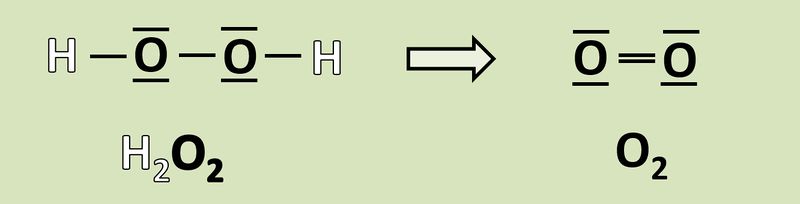
Wendet das heute gelernte Verfahren auf folgende Reaktion an und gebt an, wie viele Elektronen hier frei werden oder aufgenommen werden! <br> | |||
[[Datei:Redox1_AA1_H2O2_O2.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
[[Datei:Redox1_ML1_H2O2_O2.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
[[Datei:Redox1_AA1_NO2_NO3.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
Noch nicht vorhanden! - Wird am Mittwoch hochgeladen!<br> | |||
|Lösung|Lösung ausblenden}} | |||
[[Datei:Redox1_AA1_HCOOH_HCOH.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
Noch nicht vorhanden! - Wird am Mittwoch hochgeladen!<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#060">'''Hausaufgabe'''</span> | |||
|Inhalt= | |||
In eurem Buch ist die Bestimmung der Oxidationszahlen völlig anders erklärt. Das hat Gründe. Ich möchte, dass ihr die Seiten 74 - 75 lest und die Aufgabe 1 a+b und die Aufgabe 2 a+c löst. Schickt mir eure Lösung bitte über den Schulmanager! | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
== Arbeitsauftrag Chemie für den 20.05. == | |||
{{Box-spezial | |||
|Titel=<span style="color:#060">'''Verbesserung der Hausaufgabe'''</span> | |||
|Inhalt= | |||
Lest im Buch die S. 56-57 (Galvani, Chemie S2). Die Inhalte sind hier meiner Meinung nach schön erklärt. Bearbeitet anschließend die... | |||
* Aufgabe 1 | |||
{{Lösung versteckt| | |||
[[Datei:SäBa5_Verb_HA1a.jpg|800px]]<br> | |||
<br> | |||
[[Datei:SäBa5_Verb_HA1b.jpg|800px]]<br> | |||
<br> | |||
[[Datei:SäBa5_Verb_HA1c.jpg|800px]]<br> | |||
<br> | |||
[[Datei:SäBa5_Verb_HA1d.jpg|800px]]<br> | |||
<br> | |||
|Lösung zur Aufgabe 1|Lösung ausblenden}} | |||
* Aufgabe 2 | |||
{{Lösung versteckt| | |||
[[Datei:SäBa5_Verb_HA2.jpg|800px]]<br> | |||
<br> | |||
|Lösung zur Aufgabe 2|Lösung ausblenden}} | |||
* Aufgabe 3 | |||
{{Lösung versteckt| | |||
[[Datei:SäBa5_Verb_HA3.jpg|800px]]<br> | |||
<br> | |||
|Lösung zur Aufgabe 3|Lösung ausblenden}} | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Redoxreaktionen'''</span> | |||
|Inhalt= | |||
Wenn ihr die Hausaufgabe ordentlich verbessert habt, seid ihr für heute mit Chemie fertig. Wenn ihr Probleme mit der Hausaufgabe hattet, schreibt mir bitte möglichst konkret über den Schulmanager, was euch schwer gefallen ist.<br> | |||
Das nächste Thema, welches ich in der kommenden Woche mit euch behandeln möchte heißt '''"Redox-Reaktionen"'''. Diese sind den '''"Säure-Base-Reaktionen"''' teilweise ähnlich. Nur werden hier nicht '''Protonen '''von einem Stoff auf den anderen übertragen, sondern '''Elektronen'''. Doch dazu in der nächsten Einheit mehr... | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
== Arbeitsauftrag Chemie für den 18.05. == | |||
{{Box-spezial | |||
|Titel=<span style="color:#060">'''Verbesserung der Hausaufgabe'''</span> | |||
|Inhalt= | |||
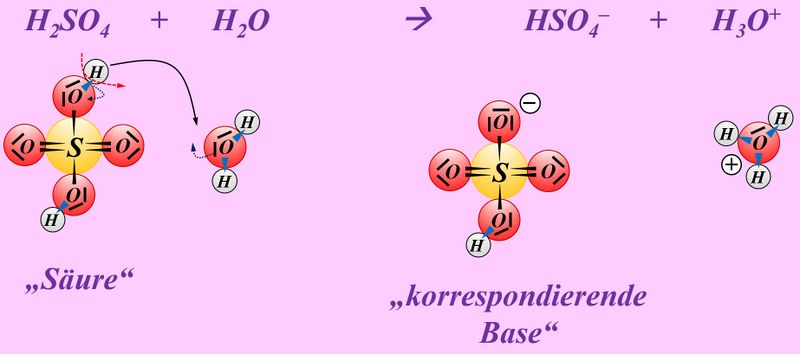
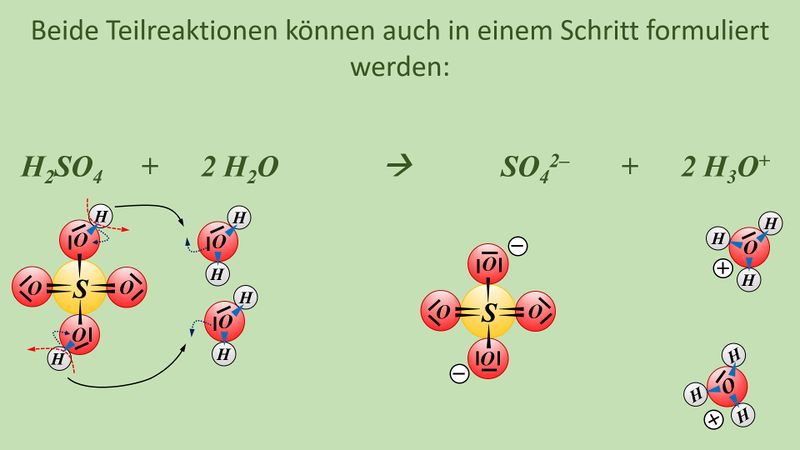
Formuliert die Reaktion von folgenden Stoffen mit Wasser: | |||
* Schwefelsäure | |||
* Iodsäure (HIO<sub>3</sub>) | |||
Formuliert die Neutralisationsreaktion von Schwefelsäure H<sub>2</sub>SO<sub>4</sub> mit Calciumhydroxid Ca(OH)<sub>2</sub> | |||
{{Lösung versteckt| | |||
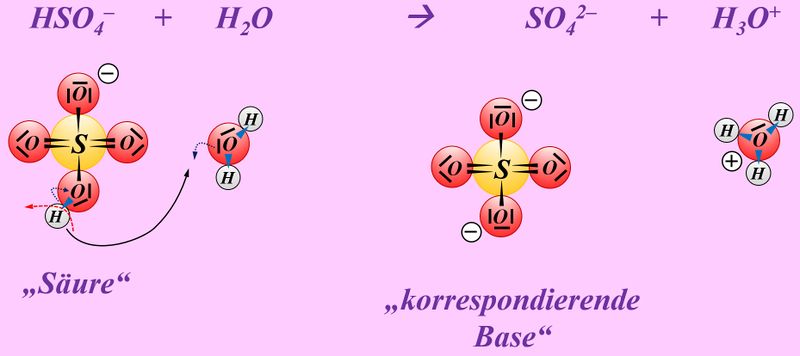
* Schwefelsäure mit Wasser: | |||
[[Datei:SäBa4_Verb_HA1.jpg|800px]]<br> | |||
<br> | |||
[[Datei:SäBa4_Verb_HA2.jpg|800px]]<br> | |||
<br> | |||
[[Datei:SäBa4_Verb_HA3.jpg|800px]]<br> | |||
<br> | |||
* Iodsäure (HIO<sub>3</sub>) mit Wasser | |||
[[Datei:SäBa4_Verb_HA4.jpg|800px]]<br> | |||
<br> | |||
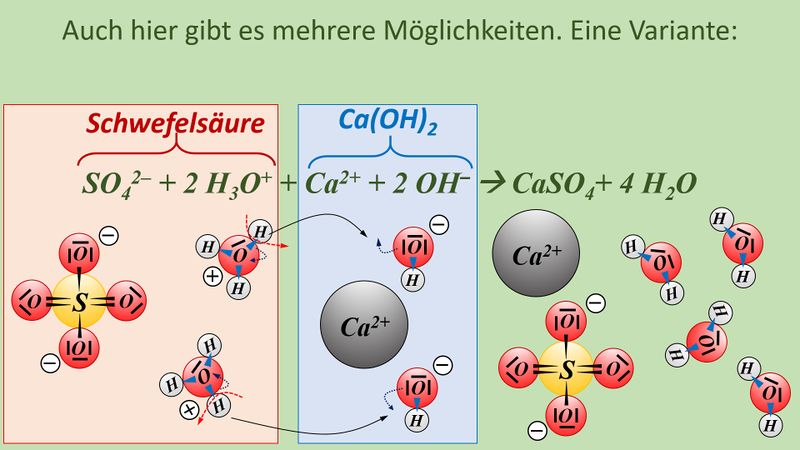
* Neutralisationsreaktion von Schwefelsäure H<sub>2</sub>SO<sub>4</sub> mit Calciumhydroxid Ca(OH)<sub>2</sub> | |||
[[Datei:SäBa4_Verb_HA5.jpg|800px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Indikatoren'''</span> | |||
|Inhalt= | |||
Heute ein Versuch! (Die praktische Durchführung ist freiwillig)<br> | |||
Ihr wisst sicherlich, dass es '''Farbstoffe '''gibt, die durch eine '''Farbänderung '''anzeigen können, ob eine wässrige Lösung eher sauer oder basisch ist. Solche Farbstoffe nennt man '''Säure-Base-Indikatoren'''. Viele farbige Stoffe, die in der Natur vorkommen, sind zu einem solchen säureabhängigen Farbumschlag fähig. Probiert es aus! <br> | |||
<br> | |||
Ihr benötigt: | |||
* Blaukraut/Rotkohl (frisch oder aus der Konserve) | |||
* Zitronensaft | |||
* Natron oder Kernseife | |||
<br> | |||
Zupft ein paar Blätter vom Rotkohl ab, schneidet sie sehr klein und gebt die Schnipsel in ein Glas mit Wasser. Wartet 5 min.<br> | |||
[[Datei:SäBa4_Indikator_Blaukraut_V.jpg|800px]]<br> | |||
Verteilt den so erzeugten violetten "Blaukraut-Saft" auf drei Gläser und verdünnt ihn mit Wasser. Gebt zum einen Glas Zitronensaft, zum anderen Natron oder Kernseife. Vergleicht die drei Gläser! | |||
{{Lösung versteckt| | |||
[[Datei:SäBa4_Indikator_Blaukraut_E.jpg|800px]]<br> | |||
|Ergebnis|Lösung ausblenden}} | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#060">'''Hausaufgabe'''</span> | |||
|Inhalt= | |||
Lest im Buch die S. 56-57 (Galvani, Chemie S2). Die Inhalte sind hier meiner Meinung nach schön erklärt. Bearbeitet anschließend die Aufgaben 1, 2, und 3 auf der S. 57 | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
== Arbeitsauftrag Chemie für den 11.05. == | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Die Säure-Base-Reaktion'''</span> | |||
|Inhalt= | |||
Ihr habt in den letzten beiden Einheiten '''Säuren''' und '''Basen '''kennengelernt. Hier noch einmal eine Kurz-Zusammenfassung über deren typische Eigenschaften auf molekularer Ebene: | |||
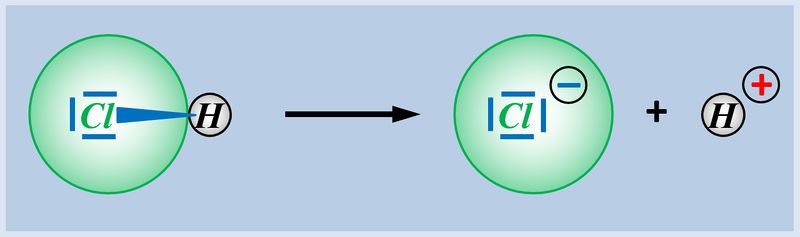
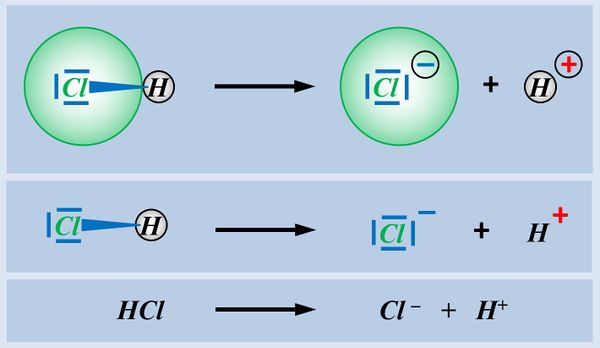
* Säuren können aus einer heterolytischen Bindung zwischen einem Wasserstoff-Atom und einem anderen Atom ein '''Proton abspalten''', z.B. HCl (Hydrogenchlorid):<br> | |||
[[Datei:SäBa3_HCl_alleine.jpg|800px]] | |||
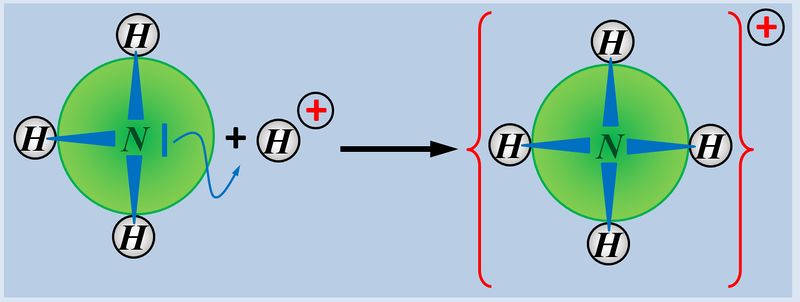
* Basen können ein Proton über ein freies Elektronenpaar ein Proton binden, also aufnehmen, z.B. NH<sub>3</sub> (Ammoniak) | |||
[[Datei:SäBa3_NH3_alleine.jpg|800px]] | |||
<br> | |||
Protonen können aber weder von Säuren einfach so "ins Freie" abgegeben werden, noch fliegen Protonen einfach so in der Gegend herum und können von Basen beliebig aufgenommen werden. Dazu ist immer ein Reaktionspartner nötig, der diese Protonen aufnimmt oder hergibt.<br> | |||
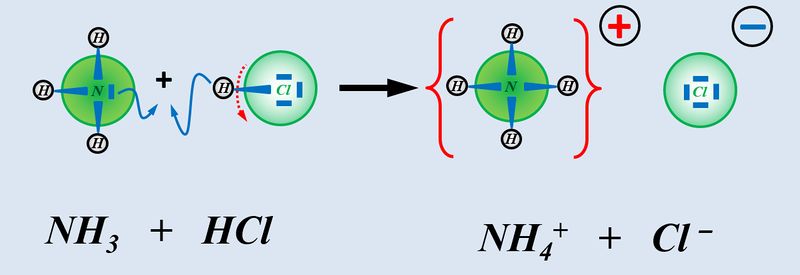
Insofern sind '''Säuren und Basen''' hervorragende '''Reaktionspartner''' und reagieren in einer typischen '''"Säure-Base-Reaktion"''' miteinander:<br> | |||
[[Datei:SäBa3_HCl_mit_NH3.jpg|800px]]<br> | |||
<br> | |||
Wie ihr sehen könnt, entsteht bei dieser Reaktion ein Salz. Also ein Stoff, der aus positiv geladenen Teilchen (hier NH<sub>4</sub><sup>+</sup>) und negativ geladenen Teilchen (hier: Cl<sup>-</sup>) aufgebaut ist. Salze entstehen auch bei der Reaktion von Metallen mit Nichtmetallen, z.B. von Natrium mit Chlor. | |||
* Vergleicht diese beiden Reaktionstypen miteinander! "Vergleichen" heißt: Gemeinsamkeiten und Unterschiede herausstellen. | |||
{{Lösung versteckt| | |||
* Bei der Salzbildung aus '''Metall und Nichtmetall''' gibt das Metall '''Elektronen '''ab, das Nichtmetall nimmt Elektronen auf. | |||
* Bei der Salzbildung aus '''Säure und Base''' gibt die Säure ein '''Proton '''ab, die Base nimmt ein Proton auf. | |||
* Gemeinsamkeit: In beiden Fällen entstehen unterschiedlich geladene Ionen, die das Salz bilden. | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
Die direkte Reaktion einer Säure mit einer Base betrachtet man an dieser Stelle im Unterricht eher selten. Einfach deswegen, weil viele Säure-Base-Reaktionen im Wasser ablaufen. Und Wasser hat ein besondere Eigenschaft. <br> | |||
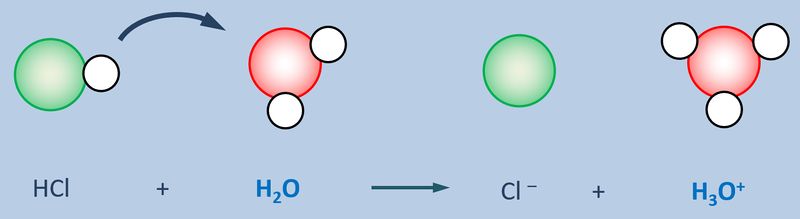
Betrachtet zunächst die hier stark vereinfacht dargestellte Reaktion, die beim Einleiten von HCl-Gas in Wasser abläuft und beschreibt sie mit Worten:<br> | |||
[[Datei:SäBa3_HCl_mit_H2O.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
Ein HCl-Molekül gibt ein Proton an ein Wassermolekül ab. Es entsteht ein Chlorid-Ion und ein Oxonium-Ion (den Namen wusstet ihr wahrscheinlich noch nicht, auch "H<sub>3</sub>O<sup>+</sup>-Teilchen" wäre o.k. gewesen. | |||
|Lösung|Lösung ausblenden}} | |||
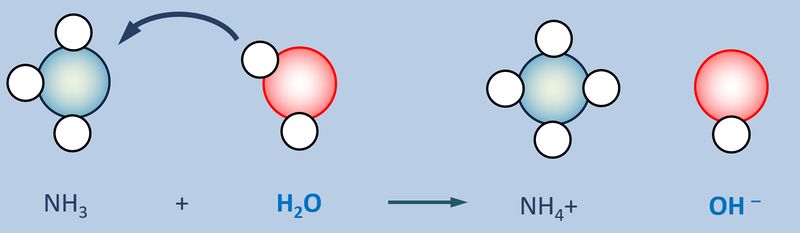
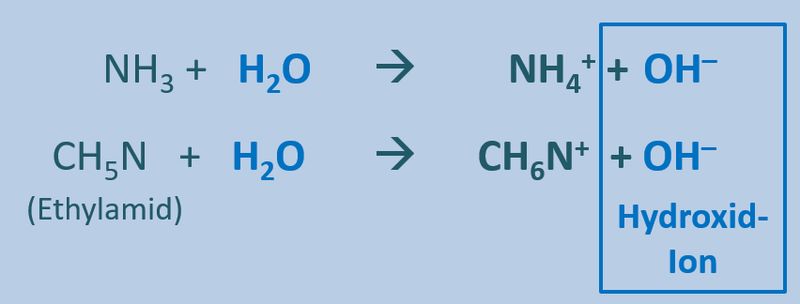
Betrachtet nun die stark vereinfacht dargestellte Reaktion, die beim Einleiten von NH<sub>3</sub>-Gas in Wasser abläuft und beschreibt sie mit Worten:<br> | |||
[[Datei:SäBa3_NH3_und_H2O.jpg|800px]]<br> | |||
{{Lösung versteckt| | |||
Ein Ammoniak-Molekül entreißt einem Wasser-Molekül ein Proton. Es entsteht ein Ammonium-Ion (NH<sub>4</sub><sup>+</sup>-Teilchen) und ein Hydroxid-Ion (OH<sup>-</sup>-Teilchen) | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
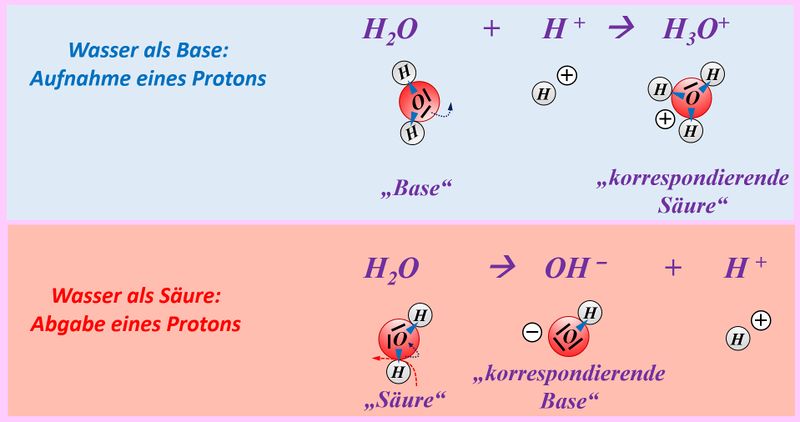
Legt nun den Fokus eurer Betrachtung auf das Wassermolekül. Zunächst zur oberen Gleichung: Was hat das Wassermolekül hier "gemacht"? | |||
{{Lösung versteckt| | |||
Es hat ein Proton aufgenommen. | |||
* Wie heißen Teilchen, die zu einer solchen Reaktion fähig sind? | |||
{{Lösung versteckt| | |||
Basen. | |||
|Lösung|Lösung ausblenden}} | |||
|Lösung|Lösung ausblenden}} | |||
Jetzt zur unteren Gleichung: Was hat das Wassermolekül hier "gemacht"? | |||
{{Lösung versteckt| | |||
Es hat ein Proton abgegeben. | |||
* Wie heißen Teilchen, die zu einer solchen Reaktion fähig sind? | |||
{{Lösung versteckt| | |||
Säuren. | |||
|Lösung|Lösung ausblenden}} | |||
|Lösung|Lösung ausblenden}} | |||
Wasser ist also ein Stoff, der je nach Partner wie eine Säure oder eine Base reagieren kann. Solche Stoffe nennt man '''Ampholyte'''. | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Der Einfluss des Wassers'''</span> | |||
|Inhalt= | |||
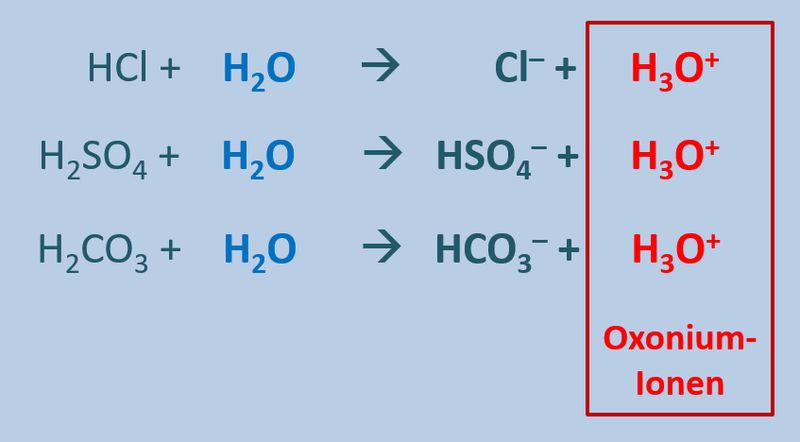
Diese Eigenschaft von Wasser führt dazu, dass beim Zugeben von '''Säuren '''(egal welcher) zu Wasser '''saure Lösungen''' entstehen, die alle eine Gemeinsamkeit haben: Sie enthalten das Oxonium-Ion H<sub>3</sub>O<sup>+</sup>:<br> | |||
[[Datei:SäBa3_divSä_undH2O.jpg|800px]]<br> | |||
<br> | |||
Ähnliches gilt für Basen. Egal welche Basen man in Wasser gibt, es entstehen immer basische Lösungen, die das Hydroxid-Ion enthalten OH<sup>-</sup>:<br> | |||
[[Datei:SäBa3_divBa_undH2O.jpg|800px]]<br> | |||
<br> | |||
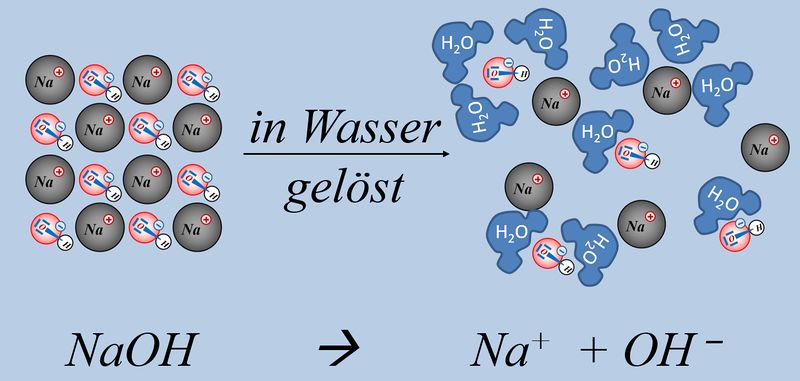
Allerdings gibt es noch eine andere Stoffgruppe, die zu basischen Lösungen führt, in denen OH<sup>-</sup>-Ionen enthalten sind: Nämlich Hydroxid-Salze, wie z.B. NaOH oder KOH oder Ca(OH)<sub>2</sub>. All diese Salze lösen sich in Wasser und setzen dabei Hydroxid-Ionen frei, ohne dass eine chemische Reaktion mit Wasser stattfinden müsste. Das Ergebnis ist aber ein ähnliches wie mit NH<sub>3</sub>, es entsteht eine basische Lösung, die Hydroxid-Ionen enthält:<br> | |||
[[Datei:SäBa3_NaOH_und_H2O.jpg|800px]]<br> | |||
<br> | |||
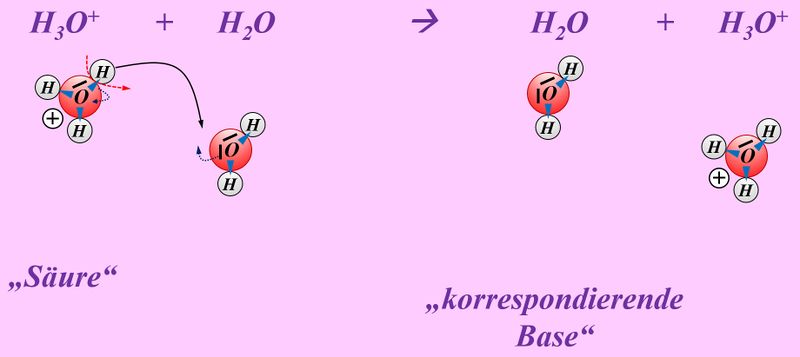
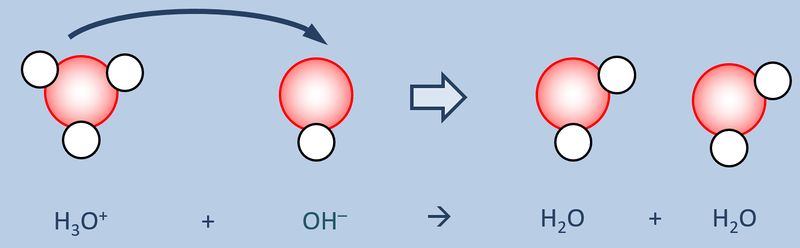
Schüttet man nun eine saure Lösung und eine basische Lösung zusammen, so reagieren eigentlich nicht die Säure und die Base direkt miteinander, sondern die bereits vorher durch den Kontakt mit Wasser gebildeten Oxonium-Ionen H<sub>3</sub>O<sup>+</sup> mit den Hydroxid-Ionen OH<sup>-</sup>:<br> | |||
[[Datei:SäBa3_H3O_und_OH.jpg|800px]]<br> | |||
<br> | |||
Diese Reaktion führ zu einer Verringerung der Oxonium- bzw. Hydroxid-Ionen, die für den sauren bzw. basischen Charakter verantwortlich waren. Die entstehende Lösung ist also weder sauer noch basisch sondern neutral. '''Man kann also sagen, Säuren und Basen neutralisieren sich gegenseitig.''' | |||
<br> | |||
Schüler formulieren folgende Aufgabe oft "stark vereinfacht": | |||
* Formuliere die Neutralisationsgleichung für die Reaktion von Natronlauge mit Salzsäure: | |||
<br> | |||
Lösung der Schüler: HCl + NaOH --> H<sub>2</sub>O + NaCl<br> | |||
<br> | |||
Was dabei übersehen wird: Salzsäure ist nicht das selbe wie HCl. HCl ist ein Gas. Wenn dieses in Wasser gelöst wird, entsteht erst die "Salzsäure". Formuliert die Gleichung für diese Reaktion! | |||
{{Lösung versteckt| | |||
HCl + H<sub>2</sub>O --> H<sub>3</sub>O<sup>+</sup> + Cl<sup>-</sup> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
Auch NaOH ist nicht das gleiche wie Natronlauge. Diese entsteht erst durch Lösen von NaOH in Wasser. Formuliert die Gleichung für diese Reaktion! | |||
{{Lösung versteckt| | |||
NaOH --> Na<sup>+</sup> + OH<sup>-</sup> | |||
|Lösung|Lösung ausblenden}} | |||
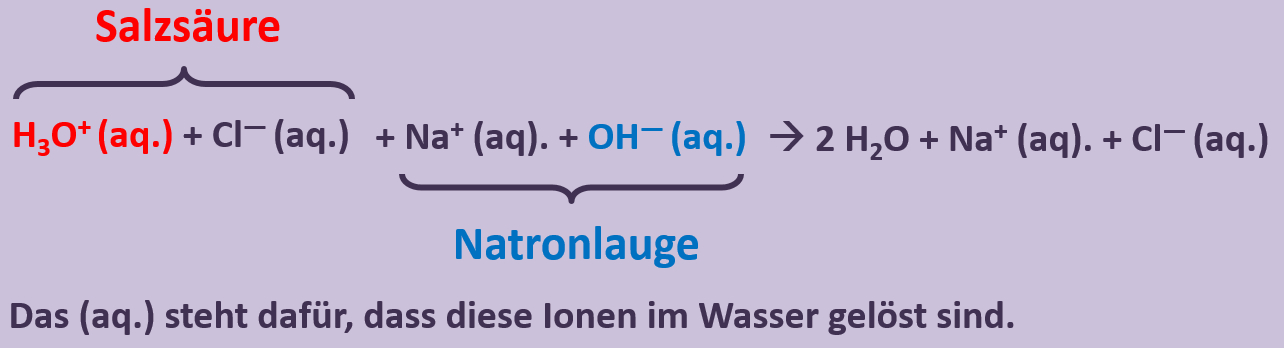
Man sollte also besser formulieren: <br> | |||
[[Datei:SäBa3_NaOH_und_HCl_mit_H2O.jpg]]<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#060">'''Hausaufgabe'''</span> | |||
|Inhalt= | |||
Formuliert die Reaktion von folgenden Stoffen mit Wasser: | |||
* Schwefelsäure | |||
* Iodsäure (HIO<sub>3</sub>) | |||
Formuliert die Neutralisationsreaktion von Schwefelsäure H<sub>2</sub>SO<sub>4</sub> mit Calciumhydroxid Ca(OH)<sub>2</sub> | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
== Arbeitsauftrag Chemie für den 04.05. == | |||
{{Box-spezial | |||
|Titel=<span style="color:#080">Verbesserung der Hausaufgabe</span> | |||
|Inhalt= | |||
'''Pflicht''': Sucht bei euch zu Hause drei völlig verschiedene '''Lebensmittel''', die '''sauer '''sind (mit "völlig verschieden" meine ich, dass ihr nicht so etwas findet wie "Äpfel" und "Birnen"). <br> | |||
'''Freiwillig:''' Versucht zu recherchieren, welches Molekül für den sauren Geschmack des Lebensmittels verantwortlich ist! | |||
* z.B.: Essig - Essigsäure (CH<sub>3</sub>-COOH) | |||
* z.B.: Zitronen (allgemein Früchte) - Zitronensäure (C<sub>6</sub>H<sub>8</sub>O<sub>7</sub>) | |||
* z.B.: Joghurt (allgemein Sauermilchprodukte) - Milchsäure (C<sub>3</sub>H<sub>6</sub>O<sub>3</sub>) | |||
* z.B.: Limo (allgemein sprudelnde Getränke) - Kohlensäure (H<sub>2</sub>CO<sub>3</sub>) | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Die "Gegenspieler" der Säuren'''</span> | |||
|Inhalt= | |||
In der letzten Einheit habt ihr gesehen, dass es Moleküle mit einer '''polaren Atombindung''' zwischen einem elektronegativen Atom und einem Wasserstoff-Atom gibt, die '''heterolytisch ein Proton abspalten''' können. Hier noch einmal verschiedene Darstellungsformen am Beispiel von Hydrogenchlorid (HCl).<br> | |||
[[Datei:SäBa2_Heterolyse_divDarstellungen.jpg|600px]]<br> | |||
<br> | |||
<br> | |||
Moleküle, bei denen eine derartige Reaktion möglich ist, nennt man '''Säuren'''. Typische '''Eigenschaften '''von Säuren sind z.B. der '''"saure Geschmack"''' oder '''"greifen unedle Metalle an"'''. Diese Eigenschaften sind auf das abspaltbare Proton zurückzuführen.<br> | |||
Sicher können sich diejenigen, die Chemie schon länger in der Schule hatten erinnern, dass es zu Säuren einen '''"Gegenspieler"''' gibt. Wie heißen diese Gegenspieler? | |||
{{Lösung versteckt| | |||
Basen oder Laugen (als Lauge bezeichnet man in der Regel eine wässrige Lösung einer Base) | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
Diese Gegenspieler sind in der Lage, die saure Wirkung von Säuren zu neutralisieren, also aufzuheben. Dazu gleich ein Versuch. Vorher noch etwas Theorie: Wenn die saure Wirkung einer Säure darauf beruht, dass die Säure-Teilchen ein Proton abgeben, welche Fähigkeit muss dann ein solches Gegenspieler-Teilchen besitzen, wenn es diese Wirkung aufzuheben vermag? | |||
{{Lösung versteckt| | |||
Es muss in der Lage sein, ein Proton aufzunehmen | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Beispiel'''</span> | |||
|Inhalt= | |||
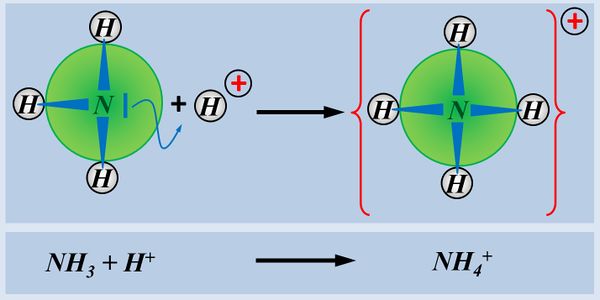
Ein einfaches Molekül, dass in der Lage ist, ein Proton aufzunehmen ist NH<sub>3</sub> (Ammoniak). Der Vorgang ist hier dargestellt. Beschreibt die Abbildung mit Worten und unter Verwendung von Fachbegriffen:<br> | |||
[[Datei:SäBa2_NH3_AufnahmeProton.jpg|600px]]<br> | |||
<br> | |||
{{Lösung versteckt| | |||
Das Ammoniak-Molekül NH<sub>3</sub> stellt sein freies Elektronen-Paar für eine Atombindung mit einem Proton zur Verfügung | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
Was ist der Unterschied zwischen dieser neu gebildeten Atombindung im Vergleich zu einer "normalen" Atombindung, wie ihr sie früher kennengelernt habt? | |||
<br> | |||
{{Lösung versteckt| | |||
Bei der Bildung einer Atombindung sind wir in den vorangegangenen Einheiten davon ausgegangen, dass jeder Partner ein Elektron zur Verfügung stellt. Hier stammen aber beide Elektronen der Atombindung nur vom Stickstoff-Atom. Das Proton hat kein Elektron zur Bindung beigetragen. | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Versuch'''</span> | |||
|Inhalt= | |||
Ein freiwilliger Versuch. '''Ihr benötigt dazu:''' | |||
* Zitrone(nsaft) | |||
* Bullrichsalz (Tabletten oder Pulver), falls nicht verfügbar ist auch Backpulver möglich. | |||
* 2 kleine Gläschen (z.B. Schnapsgläser) | |||
<br> | |||
'''Durchführung''': | |||
* Füllt die zwei Schnapsgläser zur Hälfte mit Leitungswasser. In ein Glas gebt ihr eine Tablette Bullrich-Salz (oder einen halben Teelöffel Bullrich-Salz-Pulver oder einen halben Teelöffel Backpulver. | |||
* Anschließend tropft ihr in beide Gläschen die gleiche Menge Zitronensaft (ich habe es mit jeweils 50 Tropfen Z.-Saft ausprobiert) und rührt ca. 1 Minute lang um. | |||
* Probiert von jeder Lösung indem ihr euren Finger eintaucht und ihn ableckt. (Falls ihr Backpulver verwendet habt, dürft ihr das nur '''einmal''' machen, Backpulver kann im Magen zur Bildung großer Mengen Gas führen.) | |||
<br> | |||
Beschreibt das '''Ergebnis''' in Form eurer Geschmacks-Empfindung | |||
{{Lösung versteckt| | |||
Die Lösung mit Bullrich-Salz / Backpulver sollte deutlich weniger sauer schmecken. Es kommt aber ein bisschen auf die Zitrone an. Die muss sehr sauer sein, damit der Versuch gut klappt. <br> | |||
Nur kurz zur Erklärung: Bullrichsalz enthält Natriumhydrogencarbonat. In Wasser gelöst entstehen Hydrogencarbonat-Ionen. Diese sind in der Lage Protonen aufzunehmen. Sie fungieren also als Base.<br> | |||
Die sauere Wirkung von Zitronensaft beruht auf der Zitronensäure, die ein (bzw. auch mehrere) Proton(en) abgeben kann. Nachdem diese jedoch von den Hydrogencarbonat-Ionen "abgefangen" werden, entsteht auf der Zunge kein sauerer Eindruck. | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#080">Hausaufgabe</span> | |||
|Inhalt= | |||
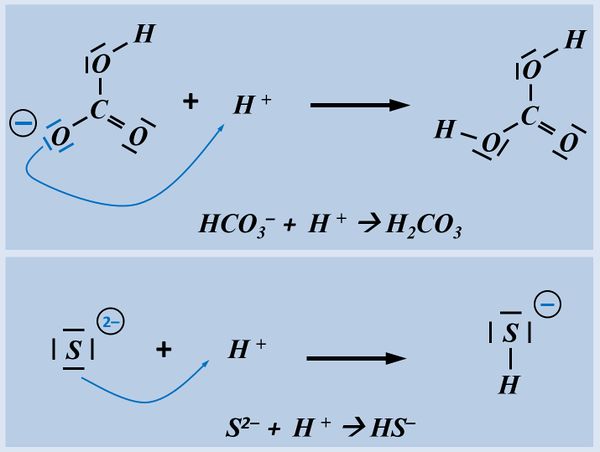
Formuliert die Aufnahme '''eines Protons''' auf Teilchen-Ebene von folgenden Basen: | |||
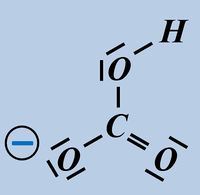
* Hydrogencarbonat-Ion | |||
* Sulfid-Ion | |||
[[Datei:SäBa2_HCO3minus_VSF.jpg|200px]] [[Datei:SäBa2_S2minus_VSF.jpg|200px]]<br> | |||
Bitte wirklich erst auf "Lösung" klicken, wenn ihr diesen chemischen Vorgang auf ein Stück Papier gezeichnet habt! | |||
{{Lösung versteckt| | |||
Hast Du wirklich die Lösung schon gezeichnet? | |||
{{Lösung versteckt| | |||
[[Datei:SäBa2_HA_ML.jpg|600px]]<br> | |||
Beim Hydrogencarbonat-Ion könnte es sein, dass ihr ein anderes freies Elektronenpaar für die Bindung zum Proton verwendet habt. Das ist aber falsch! Das Proton wird immer über eines der drei freie Elektronenpaare gebunden, die am Sauerstoff mit der negativen Ladung sitzen (im Bild blau markiert). Schon allein aufgrund der elektrischen Ladung dort, wird das positiv geladene Proton dort hin gezogen.<br> | |||
Beim Sulfid-Ion ist egal, welches Elektronenpaar verwendet wird, das Ergebnis ist faktisch immer das selbe. | |||
|Ja!|Lösung ausblenden}} | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
<br> | |||
== Arbeitsauftrag 27.04. == | |||
Für diesen Arbeitsauftrag solltet ihr ca. 30 Minuten benötigen.<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Säure-Base-Reaktionen'''</span> | |||
|Inhalt= | |||
Normalerweise würde ich das Kapitel "Säure-Base-Reaktion" sehr ausführlich behandeln. Ich beschränke mich während des Home-Schoolings auf absolute Grundlagen.<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Einstieg/Wiederholung'''</span> | |||
|Inhalt= | |||
Versucht im folgenden Bild '''möglichst genau''' zu beschreiben, was die eingekringelten Symbole bedeuten sollen. (In beiden Fällen wird das gleiche symbolisiert, es sind nur unterschiedliche Varianten.) In eurer Beschreibung sollte der Begriff "Elektronegativität (EN)" vorkommen. <br> | |||
[[Datei:SäBa1_polAtombdg_Darstellung.jpg|400px]]<br> | |||
Am besten macht ihr das wirklich schriftlich, damit ihr eure Lösung mit der hier angegebenen nachträglich gut überprüfen könnt! | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Lösung versteckt| | |||
Die eingekreisten Symbole stehen für eine "polare Atombindung".<br> | |||
Beide Begriffe, '''polar '''und '''Atombindung''', sollte man nun erklären. <br> | |||
Eine '''Atombindung '''entsteht, wenn zwei Atome jeweils ein Elektron zur Verfügung stellen und dieses Elektronenpaar sich zwischen den beiden Atomkernen aufhalten kann und dadurch zu einer Anziehung der beiden Partner führt. <br> | |||
'''Polar '''sind Atombindungen dann, wenn einer der beiden Bindungspartner in der Lage ist, das bindende Elektronenpaar stärker zu sich zu ziehen. Die beiden Elektronen haben dann eine hohe Aufenthaltswahrscheinlichkeit nicht genau in der Mitte zwischen den Atomkernen sondern bei dem Bindungspartner, der die höhere Elektronegativität (EN) hat. Der Keil, bzw. der Pfeil zeigen diese Verschiebung des Elektronenpaars hin zum elektronegativeren Partner an. | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Trennung einer polaren Atombindung'''</span> | |||
|Inhalt= | |||
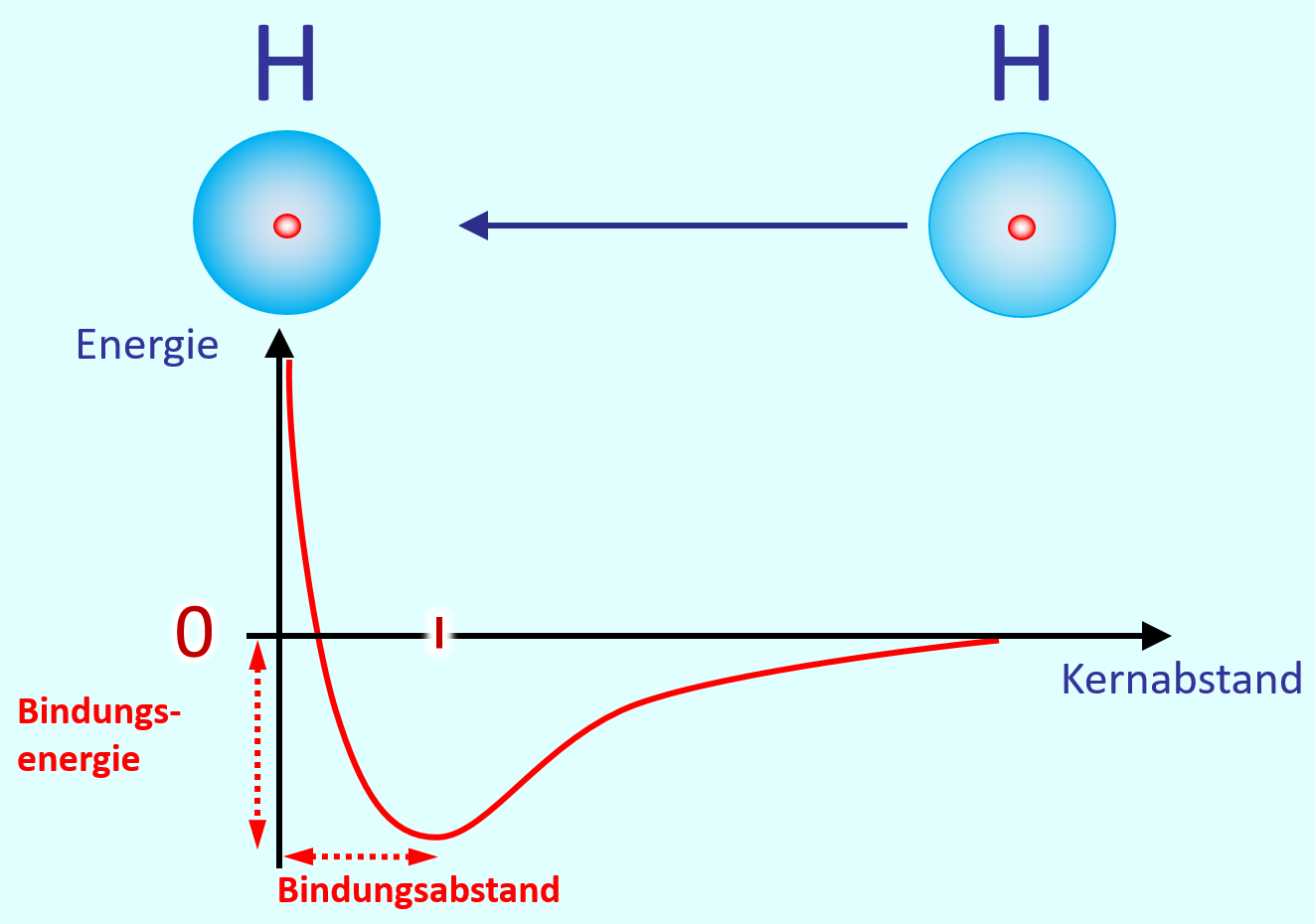
Grundsätzlich bildet sich ein Molekül aus zwei Atomen ja deswegen, weil der durch die Atombindung erreichte Zustand energetisch günstiger ist, als wenn die beiden Atome alleine bleiben würden. Wir haben das schon einmal anhand eines '''Energie-Abstands-Diagramms''' für die Bildung von H<sub>2</sub> aus 2 H dargestellt. Skizziert dieses Diagramm zur Erinnerung noch einmal: | |||
* Was muss an den Achsen stehen? | |||
* Wie ist der Verlauf? | |||
* Welche Werte könnte man aus diesem Diagramm ablesen, wenn auf den Achsen welche angegeben wären? | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Lösung versteckt| | |||
[[Datei:SäBa1_Atombdg_EAbstandsDiagr.jpg]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
{{Box-spezial | |||
|Titel= | |||
|Inhalt= | |||
Zwei Wasserstoff-Atome würden sich bei Raumtemperatur daher nicht spontan voneinander trennen. Die Atombindung ist zu stark. Bei '''polaren Atombindungen''' gibt es Situationen, in denen das anders ausschaut. Vor allem, wenn der eine Bindungspartner Wasserstoff ist. Bleiben wir bei dem oben dargestellten Molekül "Hydrogenchlorid" (HCl). Hier lassen sich die beiden Partner sehr leicht voneinander trennen. Warum? <br> | |||
Bevor diese Frage beantwortet wird vorher wieder etwas zum Auffrischen: | |||
* Wie viele Elektronen besitzt ein einzelnes Chlor-Atom insgesamt? | |||
* Wie viele davon sind Valenzelektronen? | |||
* Was muss passieren, damit dieses Chlor-Atom Edelgaskonfiguration erreicht? | |||
* Wie viele Elektronen besitzt ein einzelnes Wasserstoff-Atom insgesamt? | |||
* Wie viele davon sind Valenzelektronen? | |||
* Was muss passieren, damit Wasserstoff-Atom Edelgaskonfiguration erreicht? | |||
* Wirklich? Keine zweite Möglichkeit? | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Lösung versteckt| | |||
* Ein Chlor-Atom besitzt insgesamt 17 Elektronen | |||
* Sieben davon sitzen auf der äußersten Schale, sind also Valenzelektronen | |||
* Chlor muss ein Elektron aufnehmen | |||
* Ein Wasserstoff-Atom besitzt ein Elektron | |||
* ...''sehr witzig''... | |||
* Es muss eins aufnehmen, um die Edelgas-Konfiguration von Helium zu erreichen (Zwei Elektronen auf der innersten Schale, die damit voll besetzt ist und einen sehr energiearmen Zustand darstellt) | |||
* ''Das haben wir noch nicht besprochen'': Wasserstoff könnte das eine Elektron auch abgeben. Dann hat es überhaupt keins mehr. Vom Wasserstoffatom bliebe dann nur das eine Proton im Kern übrig. Das ist zwar keine klassische Edelgaskonfiguration, aber dennoch auch ein sehr energiearmer Zustand. | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
{{Box-spezial | |||
|Titel= | |||
|Inhalt= | |||
Die folgende Aussage ist "anthropomorph". Das bedeutet, man tut so, als wären die betrachteten Teilchen Lebewesen/Menschen mit Gefühlen und Bedürfnissen. Das ist natürlich nicht so! Solche Aussagen sind aber oft sehr leicht verständlich für Schülerinnen und Schüler. Ich werde die Aussage erst später ''fachwissenschaftlich'' umformulieren: <br> | |||
O.k., schauen wir uns die Situation mal an: Wir haben zwei Atome, ein Wasserstoff-Atom und ein Chlor-Atom. Beide teilen sich ein Elektronenpaar und bilden daher ein Molekül. Das Chlor-Atom ist unglaublich scharf auf das Elektronenpaar. Wenn es beide Elektronen haben könnte, hätte es Edelgaskonfiguration. Das Wasserstoff-Atom könnte mit beiden Elektronen zwar auch etwas anfangen, ist aber auch glücklich, wenn es überhaupt kein Elektron mehr hat.<br> | |||
WAS WIRD WOHL PASSIEREN? <br> | |||
Wer keine Ahnung hat, was das soll, vielleicht noch ein anderes Beispiel: Ihr habt ein kleines Geschwister. Das hat zum Geburtstag ein Playmobil-Pferd geschenkt bekommen. Ihr habt den passenden Playmobil-Cowboy dazu, den ihr irgendwie ganz witzig findet. Euer kleines Geschwister kommt permanent zu euch ins Zimmer und will mit euch und eurem Playmobil-Cowboy spielen. Eine Zeit lang macht euch das auch Spaß und ihr macht mit. Aber plötzlich klingelt euer Handy und euer... bester Freund/beste Freundin ist dran. WAS MACHT IHR? - Vermutlich: Ihr schenkt euren Playmobil-Cowboy eurem Geschwister und schickt ihn aus dem Zimmer. Übertragt das jetzt auf die Atome! | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Lösung versteckt| | |||
Das bindende Elektronenpaar (Playmobil-Pferd + Playmobil-Cowboy) wird komplett auf das Chlor-Atom (euer Geschwister) übertragen. Es entsteht ein '''positiv geladenes Wasserstoff-Teilchen''' (vorher: ein positiv geladenes Proton im Kern, ein negatives Elektron in der Hülle; jetzt; nur noch ein Proton) und ein '''negativ geladenes Chlor-Teilchen''' (vorher: 17 Protonen im Kern, 17 Elektronen in der Hülle; jetzt: 17 Protonen im Kern, 18 Elektronen in der Hülle.<br> | |||
[[Datei:SäBa1_heterolytBdgTrennung.jpg|400px]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
{{Box-spezial | |||
|Titel= | |||
|Inhalt= | |||
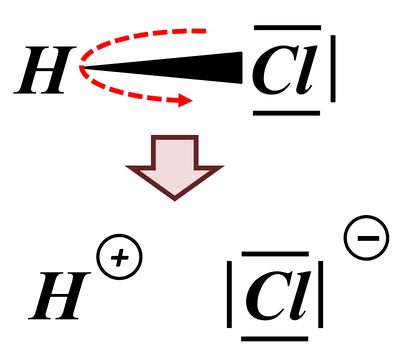
Man spricht in so einem Fall von einer '''heterolytischen Bindungstrennung'''. "Bindungstrennung" bedeutet, dass eine Bindung getrennt wird (ziemlich logisch...) und "hetero"(lytisch) bedeutet, dass die Bindung (bzw. besser: das bindende Elektronenpaar) "ungleichmäßig" aufgeteilt wird. Es gibt auch die "homolytische Bindungstrennung", bei der wird die Bindung so aufgeteilt, dass jeder Partner ein Elektron des bindenden Paares bekommt. Das ist hier aber nicht so: Das Wasserstoff-Atom bekommt gar kein, das Chlor-Atom beide. Deswegen: '''heterolytische '''Bindungstrennung.<br> | |||
Die Abspaltung eines Wasserstoffteilchens nach diesem Muster ist etwas, was viele Moleküle können (wenn ein passender Reaktionspartner zur Verfügung steht). Man zählt solche Moleküle zur Gruppe der '''"Säuren"'''. Wenn z.B. etwas '''"sauer"''' schmeckt, dann sicher deswegen, weil eine '''Säure '''enthalten ist, also ein Molekül, das durch heterolytische Bindungstrennung ein Proton (das was vom Wasserstoffteilchen nach der Abspaltung übrig bleibt) abgespalten hat.<br> | |||
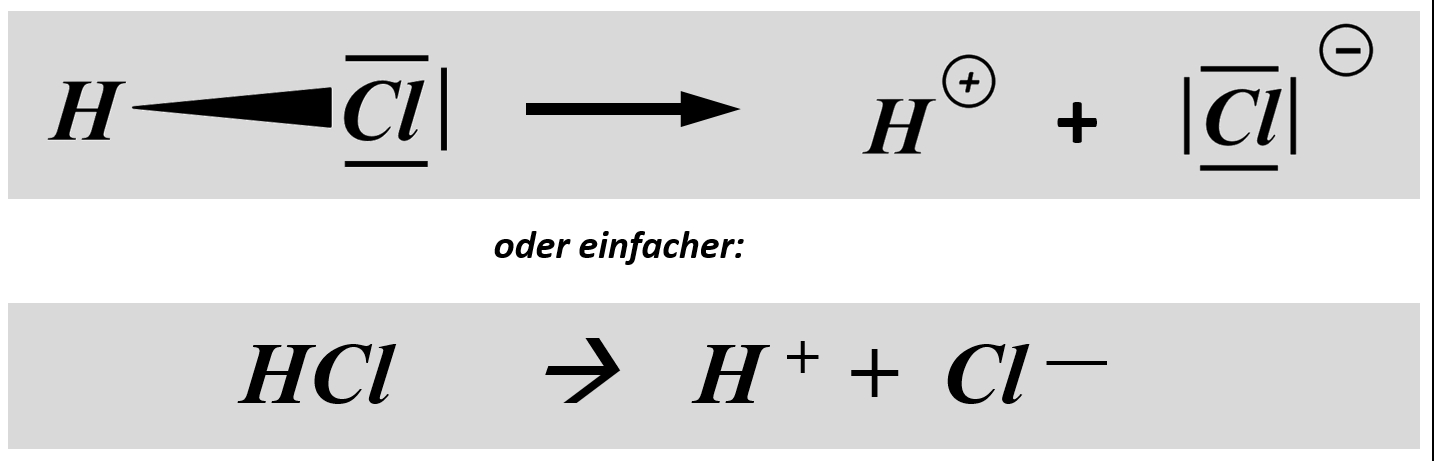
Man kann diese Abspaltung als chemische Gleichung formulieren: <br> | |||
[[Datei:SäBa1_heterolytBdgTrennung_Gleichung.jpg]]<br> | |||
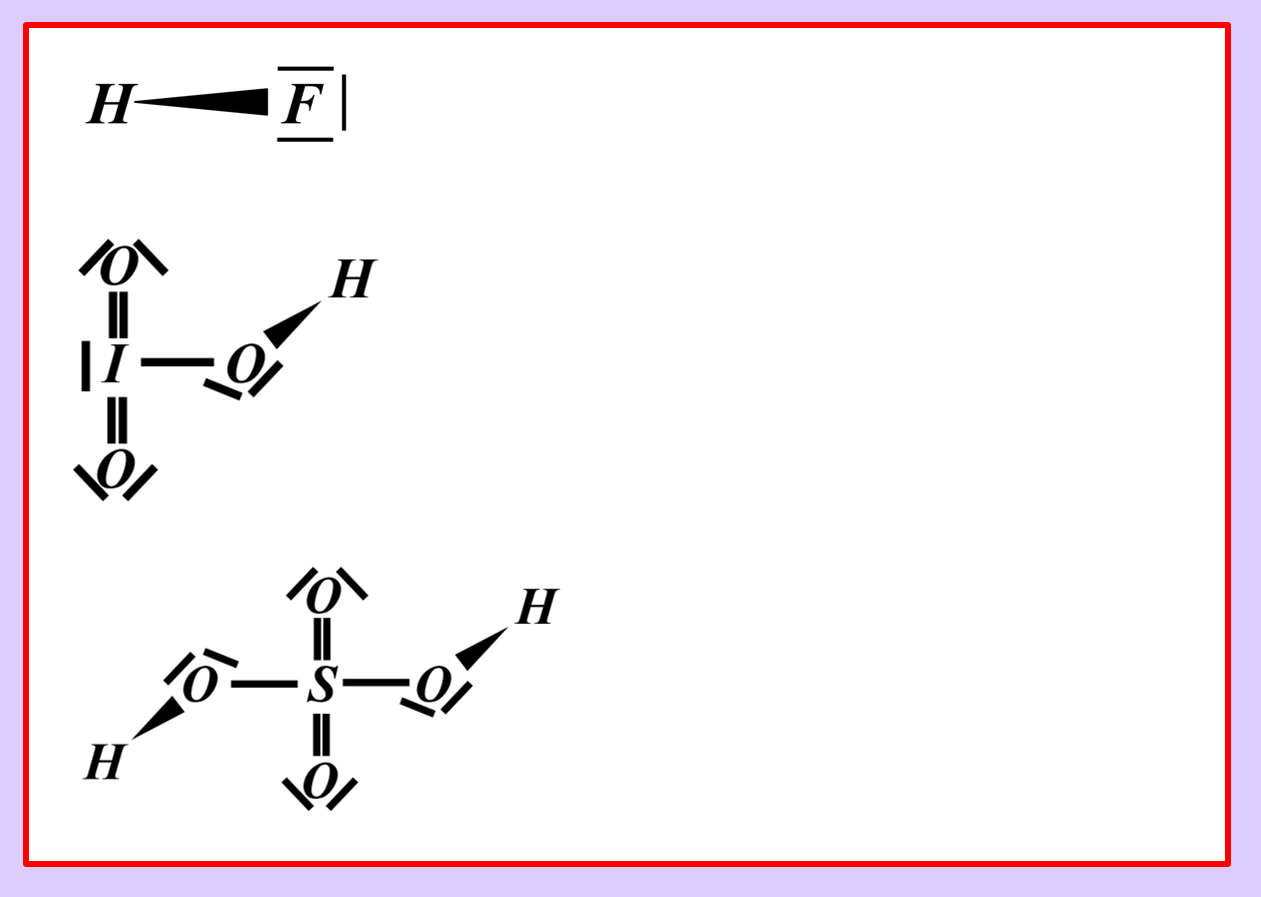
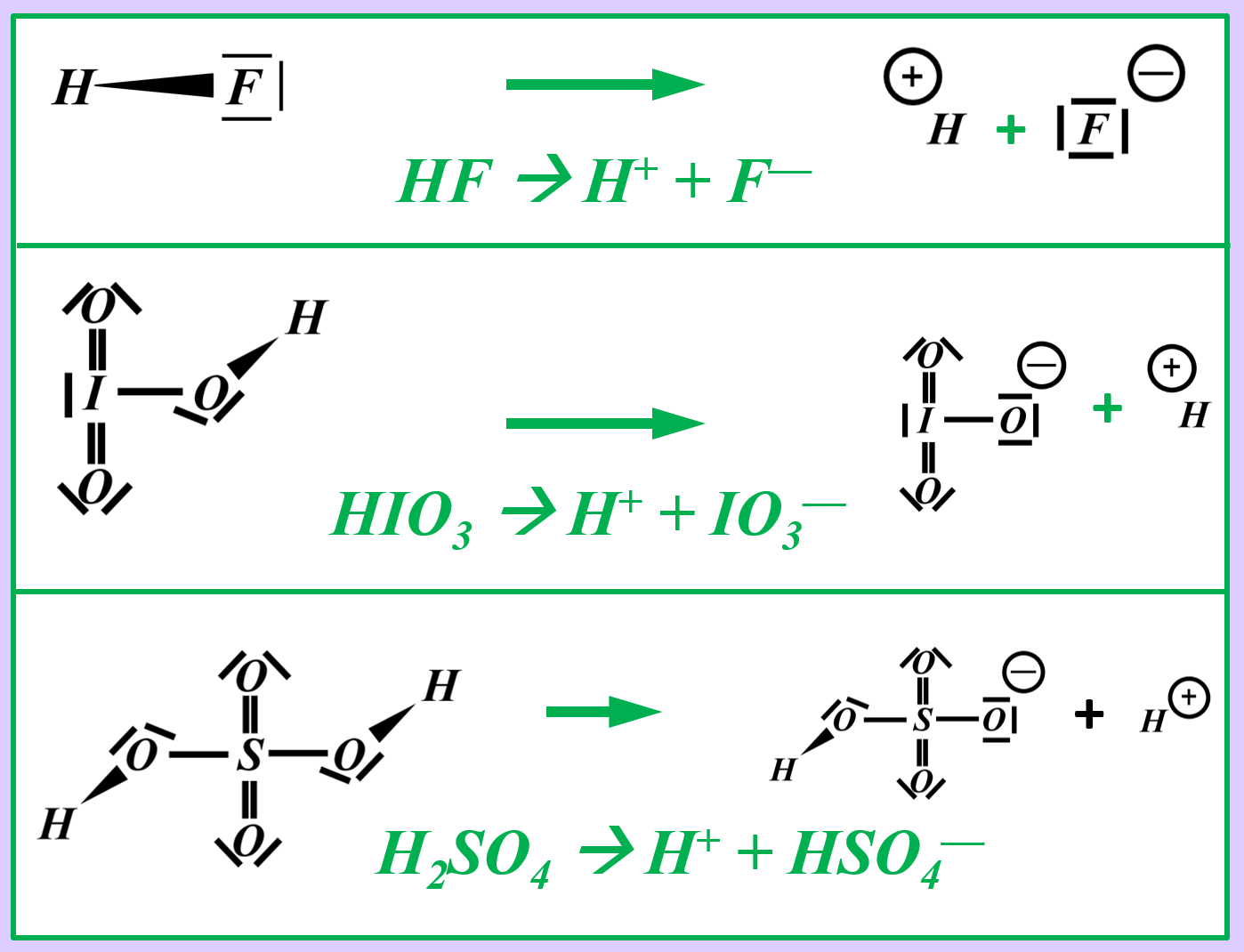
Stellt nach dem gleichen Muster die chemischen Gleichungen (beide Varianten: mit und ohne Valenzstrichformel) für die heterolytische Bindungstrennung für folgende Säure-Moleküle auf:<br> | |||
* Hydrogenfluorid (HF) | |||
* Iodsäure (HIO<sub>3</sub>) | |||
* Schwefelsäure (H<sub>2<sub>SO</sub>4</sub>) | |||
[[Datei:SäBa1_Aufgabe1_chemGl_Heterolyse.jpg]]<br> | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Lösung versteckt| | |||
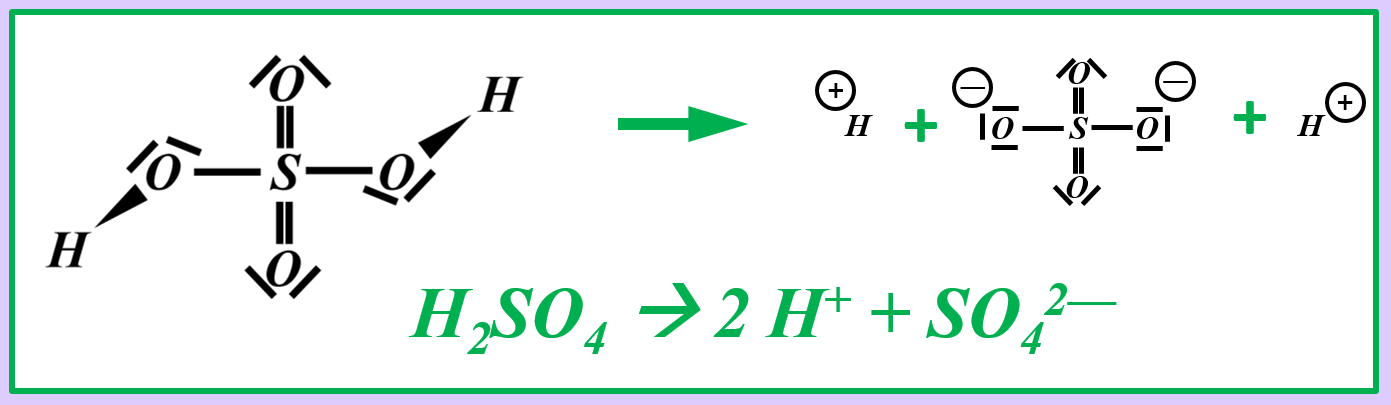
[[Datei:SäBa1_Aufgabe1_chemGl_Heterolyse_ML1.jpg]]<br> | |||
Vielleicht habt ihr bei der Schwefelsäure das andere Proton abgespalten. Das funktioniert. Es können sogar beide Wasserstoff-Teilchen gleichzeitig abgespalten werden. Stellt dafür (sofern ihr es noch nicht getan habt) die Gleichungen (mit und ohne Valenzstrichformeln) auf! | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
{{Lösung versteckt| | |||
[[Datei:SäBa1_Aufgabe1_chemGl_Heterolyse_ML2.jpg]]<br> | |||
|Lösung|Lösung ausblenden}} | |||
<br> | |||
" | {{Box-spezial | ||
|Titel=<span style="color:#080">Hausaufgabe</span> | |||
|Inhalt= | |||
Das Buch geht hier anders vor, deswegen keine Seiten im Buch lesen. Eher etwas praktisches als Hausaufgabe: <br> | |||
'''Pflicht''': Sucht bei euch zu Hause drei völlig verschiedene '''Lebensmittel''', die '''sauer '''sind (mit "völlig verschieden" meine ich, dass ihr nicht so etwas findet wie "Äpfel" und "Birnen"). <br> | |||
'''Freiwillig:''' Versucht zu recherchieren, welches Molekül für den sauren Geschmack des Lebensmittels verantwortlich ist! | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | |||
<br> | <br> | ||
== Arbeitsauftrag 20.04. == | == Arbeitsauftrag 20.04. == | ||
Aktuelle Version vom 15. Februar 2021, 06:08 Uhr
Diejenigen unter euch, die in der Oberstufe Chemie belegt haben, sollten diese Aufgaben wirklich bearbeiten. Bitte meldet mir Unklarheiten auch möglichst zeitnah zurück. Für diejenigen, die kein Chemie belegt haben, können die Aufgaben trotzdem ganz nützlich sein. Vor allem in der ersten Hälfte der elften Klasse in Biologie wird oft auf die chemischen Grundlagen bestimmter Stoffwechselreaktionen zurückgegriffen.
Arbeitsauftrag Chemie für den 27.05.
Arbeitsauftrag Chemie für den 25.05.
Arbeitsauftrag Chemie für den 20.05.
Arbeitsauftrag Chemie für den 18.05.
Arbeitsauftrag Chemie für den 11.05.
Arbeitsauftrag Chemie für den 04.05.
Arbeitsauftrag 27.04.
Für diesen Arbeitsauftrag solltet ihr ca. 30 Minuten benötigen.
Die eingekreisten Symbole stehen für eine "polare Atombindung".
Beide Begriffe, polar und Atombindung, sollte man nun erklären.
Eine Atombindung entsteht, wenn zwei Atome jeweils ein Elektron zur Verfügung stellen und dieses Elektronenpaar sich zwischen den beiden Atomkernen aufhalten kann und dadurch zu einer Anziehung der beiden Partner führt.
Polar sind Atombindungen dann, wenn einer der beiden Bindungspartner in der Lage ist, das bindende Elektronenpaar stärker zu sich zu ziehen. Die beiden Elektronen haben dann eine hohe Aufenthaltswahrscheinlichkeit nicht genau in der Mitte zwischen den Atomkernen sondern bei dem Bindungspartner, der die höhere Elektronegativität (EN) hat. Der Keil, bzw. der Pfeil zeigen diese Verschiebung des Elektronenpaars hin zum elektronegativeren Partner an.
- Ein Chlor-Atom besitzt insgesamt 17 Elektronen
- Sieben davon sitzen auf der äußersten Schale, sind also Valenzelektronen
- Chlor muss ein Elektron aufnehmen
- Ein Wasserstoff-Atom besitzt ein Elektron
- ...sehr witzig...
- Es muss eins aufnehmen, um die Edelgas-Konfiguration von Helium zu erreichen (Zwei Elektronen auf der innersten Schale, die damit voll besetzt ist und einen sehr energiearmen Zustand darstellt)
- Das haben wir noch nicht besprochen: Wasserstoff könnte das eine Elektron auch abgeben. Dann hat es überhaupt keins mehr. Vom Wasserstoffatom bliebe dann nur das eine Proton im Kern übrig. Das ist zwar keine klassische Edelgaskonfiguration, aber dennoch auch ein sehr energiearmer Zustand.
Das bindende Elektronenpaar (Playmobil-Pferd + Playmobil-Cowboy) wird komplett auf das Chlor-Atom (euer Geschwister) übertragen. Es entsteht ein positiv geladenes Wasserstoff-Teilchen (vorher: ein positiv geladenes Proton im Kern, ein negatives Elektron in der Hülle; jetzt; nur noch ein Proton) und ein negativ geladenes Chlor-Teilchen (vorher: 17 Protonen im Kern, 17 Elektronen in der Hülle; jetzt: 17 Protonen im Kern, 18 Elektronen in der Hülle.
Vielleicht habt ihr bei der Schwefelsäure das andere Proton abgespalten. Das funktioniert. Es können sogar beide Wasserstoff-Teilchen gleichzeitig abgespalten werden. Stellt dafür (sofern ihr es noch nicht getan habt) die Gleichungen (mit und ohne Valenzstrichformeln) auf!
Arbeitsauftrag 20.04.