Benutzer:Thomas Lux/Test Oberstufe: Unterschied zwischen den Versionen
Aus RMG-Wiki
(Video eingefügt) Markierung: Quelltext-Bearbeitung 2017 |
KKeine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
||
| Zeile 19: | Zeile 19: | ||
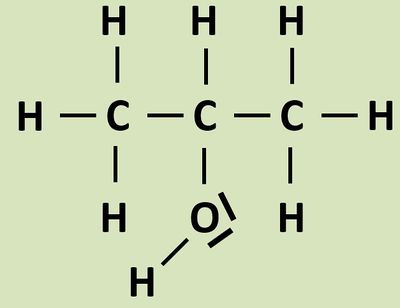
Propan-2-ol | Propan-2-ol | ||
|Lösung|Lösung ausblenden}} | |Lösung|Lösung ausblenden}} | ||
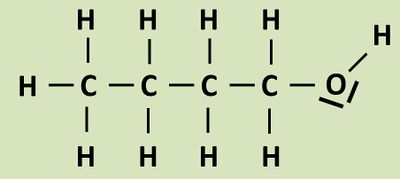
* Nenne alle bei Ethanol-Molekülen auftretenden "zwischenmolekularen Kräfte" und ordne sie nach ihrer Stärke! | * Nenne alle bei Ethanol-Molekülen auftretenden "zwischenmolekularen Kräfte" und ordne sie nach ihrer Stärke! (Das ist eine Wiederholungsaufgabe. Die geforderten Inhalte sind nur teilweise im Video oder im Buch enthalten) | ||
{{Lösung versteckt| | {{Lösung versteckt| | ||
Die stärksten "zwischenmolekularen Kräfte" wären hier: '''Wasserstoffbrückenbindungen'''. | |||
Sie können sich ausbilden zwischen Wasserstoffen, die an ein stark elektronegatives Element gebunden sind (ist hier der Fall: Das H-Atom der Hydroxgruppe) und freien Elektronenpaaren eines stark elektronegativen Elements der 2. Periode (ist hier der Fall: Das O-Atom der Hdroxgruppe hat freie Elektronenpaare und ist stark elektronegativ) | * Sie können sich ausbilden zwischen Wasserstoffen, die an ein stark elektronegatives Element gebunden sind (ist hier der Fall: Das H-Atom der Hydroxgruppe) und freien Elektronenpaaren eines stark elektronegativen Elements der 2. Periode (ist hier der Fall: Das O-Atom der Hdroxgruppe hat freie Elektronenpaare und ist stark elektronegativ) | ||
Die zweitstärksten "zwischenmolekularen Kräfte" wären hier: Die Kräfte '''zwischen den permanenten Dipolen'''.<br> | |||
Dann gibt eine Kraft, die aufritt, wenn ein '''permanenter Dipol''' in benachbarten Molekülen einen '''Dipol induziert'''.<br> | |||
Die schwächsten Kräfte sind die van-der-Waals-Kraft im engeren Sinne: Durch Fluktuationen in der Elektronenhülle entstehen '''spontane Dipole''', die im Nachbarmolekül ebenfalls kleine '''Dipole induzieren''' können. | |||
|Lösung|Lösung ausblenden}} | |Lösung|Lösung ausblenden}} | ||
Version vom 12. Januar 2021, 15:30 Uhr
Distanzunterricht Mittwoch, 13.01.