Corona-Arbeitsaufträge (Chemie) LUX
Inhaltsverzeichnis
Arbeitsauftrag Chemie1
Züchtet einen Salzkristall:
- Dokumentiert jeden der folgenden Schritte mit einem Foto, damit ihr daraus später eine schöne Anleitung am PC erstellen könnt!
- Füllt ein Glas mit heißem Wasser. Ihr braucht es nicht extra erhitzen, nehmt einfach das heißeste Wasser, was ihr aus eurer Leitung bekommen könnt.
- Gebt löffelweise Spülmaschinen-Salz dazu und rührt um. Minutenlang! (Wenn ihr kein Spülmaschinen-Salz habt, geht auch normales Speisesalz)
- Irgendwann wird sich das Salz im Glas nicht mehr auflösen. Lasst den Ansatz dann noch 5 Minuten stehen.
- Filtriert das Salzwasser durch einen Kaffee-Filter und fangt das Wasser in einem zweiten Glas auf
- Schüttet etwas von dem Filtrat in eine Untertasse (am besten eine, die nicht weiß ist) und stellt es an einen sonnigen Platz auf das Fensterbrett, wo der Ansatz bis Montag stehen bleiben kann ohne dass er stört. Er sollte nicht bewegt werden.
- Macht alle 24 Stunden ein Foto.
- Am Montag, 23.03. geht es weiter
Sofern ihr Arbeitsauftrag Chemie1 durchgeführt habt, könnt ihr nun folgende Überlegungen anstellen:
- Gibt es in eurem Haushalt noch andere "reine Salze" mit denen ihr diesen Versuch durchführen könnte. Wenn ja: Probiert es aus!
- Wenn man das Wasser vollständig verdunsten lässt, entstehen ganz zum Schluss viele kleine Kristalle, die wie ein Schleier alles überziehen.
- Wenn man das nicht möchte, kann man vorher (z.B. nach 12 Stunden) einen kleinen, sauberen Kristall aus der Lösung holen und in ein neues Gefäß mit gesättigter Salzlösung überführen. Man kann ihn auch an einem Faden in ein Glas mit der Salzlösung hängen. Im Internet gibt es dazu reichlich Anleitungen. Wenn man Glück hat, wächst nur der kleine Kristall zu einem großen heran. Versucht das!
- Man kann aus Draht z.B. einen Stern formen und diesen in ein Glas mit der Salzlösung hängen. Oder auch wieder in eine Untertasse mit der Salzlösung legen. Lässt man das Wasser komplett verdunsten, ist der Draht dann überall mit kleinen Kristallen überzogen. Manche finden das schön.
- Führt den Versuch erneut durch. Stellt das Gefäß, in dem die Kristalle wachsen sollen, an einen ungestörten Ort. Baut eine Halterung, in der ihr euer Handy / euren Fotoapparat zum Anfertigen des Fotos kurz einspannen könnt, so dass jedes Foto vom Versuch aus exakt der selben Perspektive gemacht wird. Macht alle 8 Stunden (besser alle 4 oder 2 - was nachts aber schwierig ist...) ein Foto. Aus diesen Fotos kann man später eine Zeitrafferaufnahme machen.
Arbeitsauftrag Chemie2 (verpflichtend)
Die folgende verpflichtende Unterrichtseinheit hat eine Bearbeitungszeit von ca. 45 Minuten. Ihr benötigt für die Bearbeitung: Das Schulbuch, das PSE, einen Zettel, Stift, Internetzugriff um ein yt-Video zu schauen. Und Ruhe. Bitte bearbeitet die gestellten Aufgaben tatsächlich erst selbst, bevor ihr auf die Lösung klickt!
Die Atombindung (auch: kovalente Bindung)
Das folgende yt-Video bietet einen sehr guten Einstieg in die Thematik. Tatsächlich würde ich im Unterricht nahezu genau das gleiche sagen. Zu Beginn des Videos wird auf andere Videos verwiesen, die vorausgesetzt werden. Diese Videos braucht ihr nicht zu schauen. Wir haben das bereits im Unterricht besprochen.
Zum Einstieg vielleicht eine kleine Wiederholung (ca. 5 Min.):
- Notiere, was "Valenzelektronen" sind!
Das sind die Elektronen, die sich bei Atomen eines bestimmten Elements auf der äußersten Schale befinden.
- Bestimme die Anzahl der Valenzelektronen (VE) der Atome folgender Elemente mit Hilfe des PSE: Calcium, Lithium, Iod!
Ca: 2 VE, Li: 1 VE, I: 7 VE
- Erkläre, wie Du diese Anzahl bestimmt hast!
Die Anzahl der VE entspricht der Hauptgruppen-Nr. im PSE.
- Bestimme die chemische Formel des Salzes Berylliumbromid!
Beryllium besitzt 2 VE. Um Edelgaskonfiguration zu erreichen, muss es diese beiden abgeben. Es entstehen Be2+-Ionen. Brom besitzt 7 VE. Um Edelgaskonfiguration zu erreichen muss es ein Elektron aufnehmen. Es entstehen Br--Ionen. Damit ein neutrales (nicht geladenes) Salz entsteht und keine Elektronen verloren gehen oder übrig bleiben, müssen immer zwei Bromid-Atome mit einem Beryllium-Atom reagieren. Die Formel des entstehenden Salzes lautet dann BeBr2
Das genügt als Wiederholung. Jetzt zum yt-Video (10:06 min.): Hier klicken
Testet, ob ihr die Inhalte des Videos wiedergeben könnt:
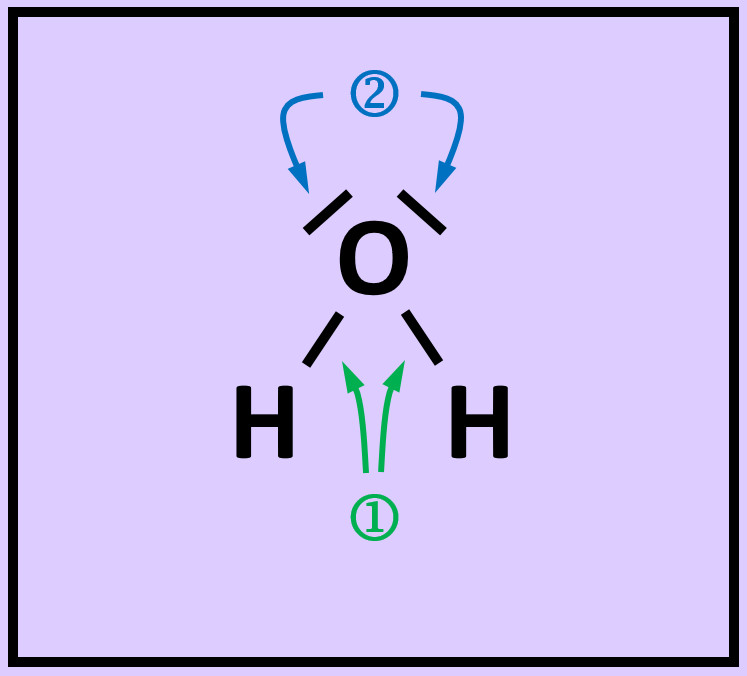
- Das folgende Bild zeigt die Valenzstrichformel des Wassermoleküls. Was bedeuten die mit unterschiedlichen Ziffern markierten Striche?
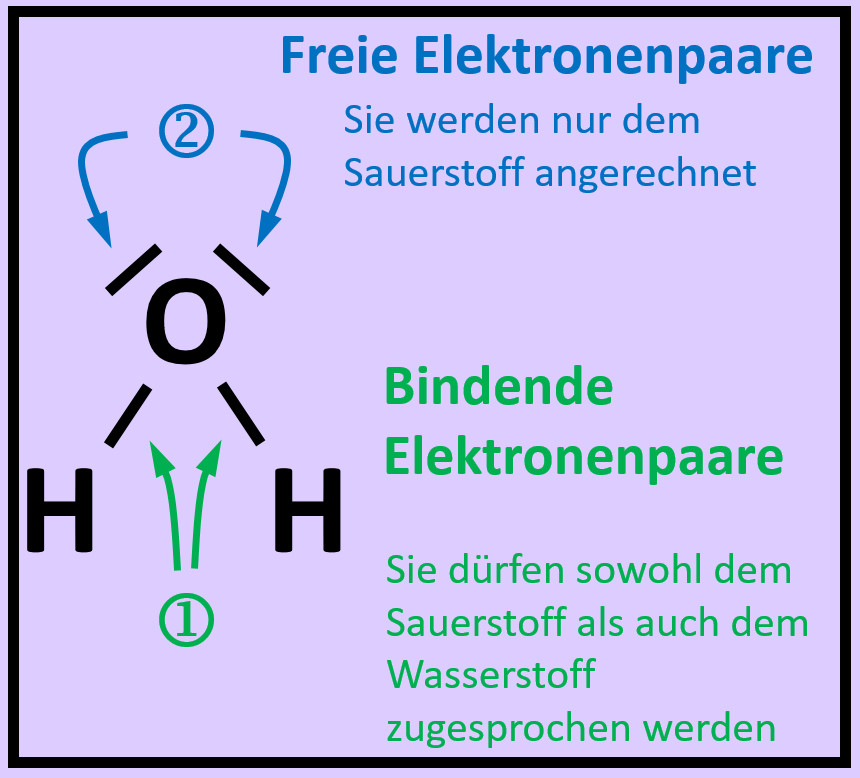
Freie Elektronenpaare stammen nur von dem Atom, das sie umgeben. Bei den bindenden Elektronenpaaren stammt ein Elektron vom einen Partner (hier: Sauerstoff) und das andere Elektron vom anderen Partner (hier: Wasserstoff)
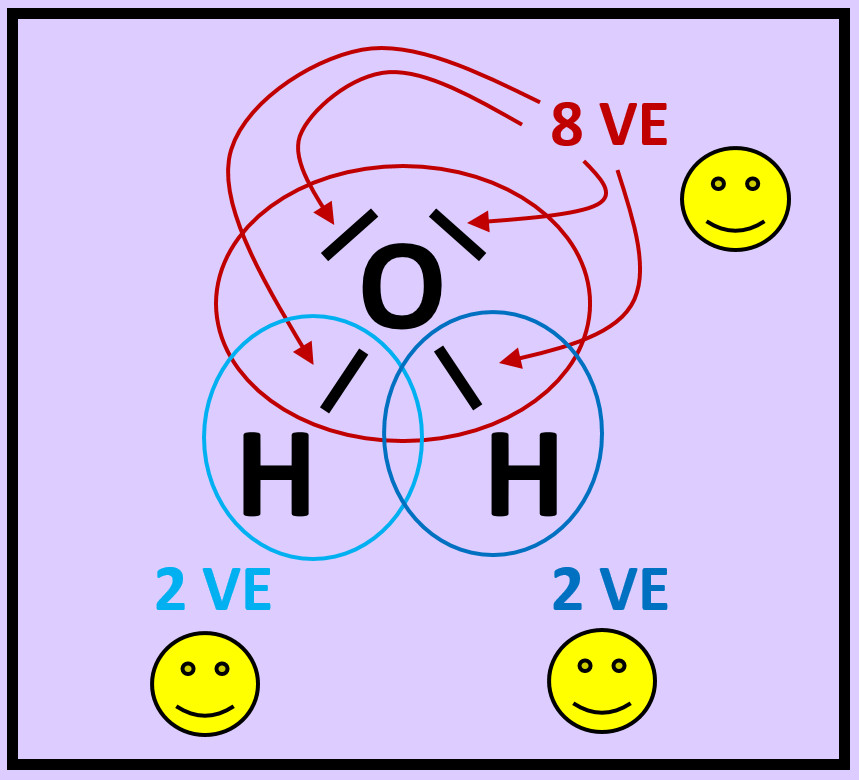
- Zeichnet das Wassermolekül ab. Kreist nun jedes Atom ein. Achtet dabei darauf, dass im Kreis alle Elektronen (freie Elektronenpaare und bindende Elektronenpaare) enthalten sind, die dem Atom zugerechnet werden können!
- Zählt nun die Elektronen, die ihr jedem Atom zugeordnet habt!
- Entscheidet, ob durch diese Anordnung Edelgaskonfiguration erreicht wurde!
- Warum kann man beim Wasserstoff von Edelgaskonfiguration sprechen, obwohl ihm nur zwei Elektronen zugesprochen werden?
Die beiden Elektronen sitzen auf der innersten Schale, der K-Schale. Damit ist diese voll besetzt. Dies entspricht der Konfiguration von Helium und damit einem Edelgas.
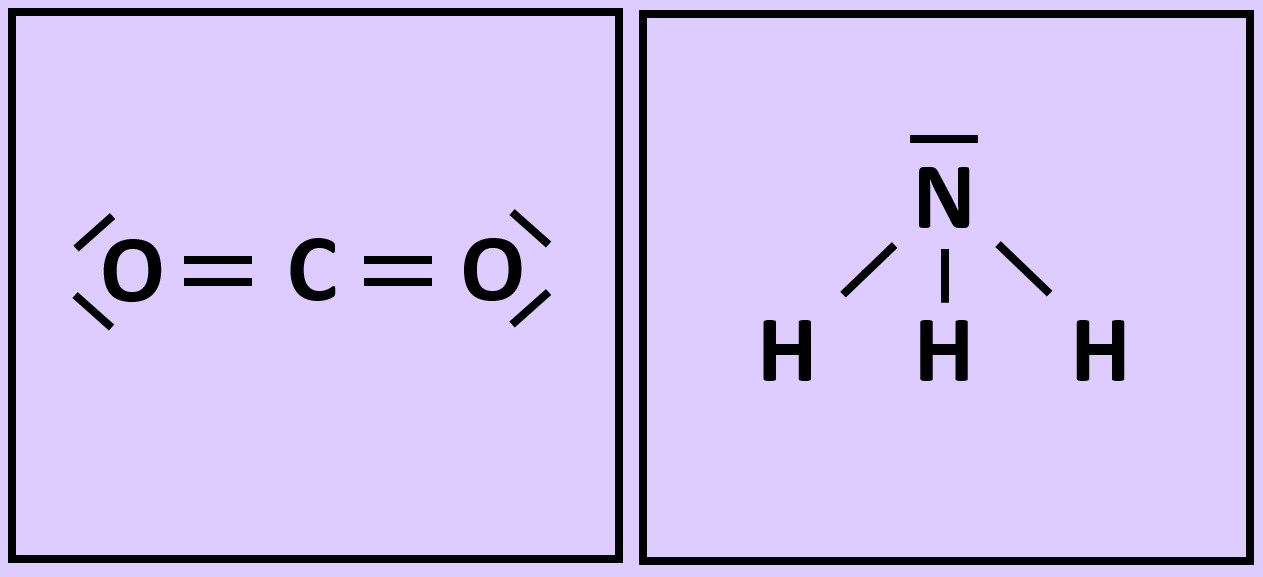
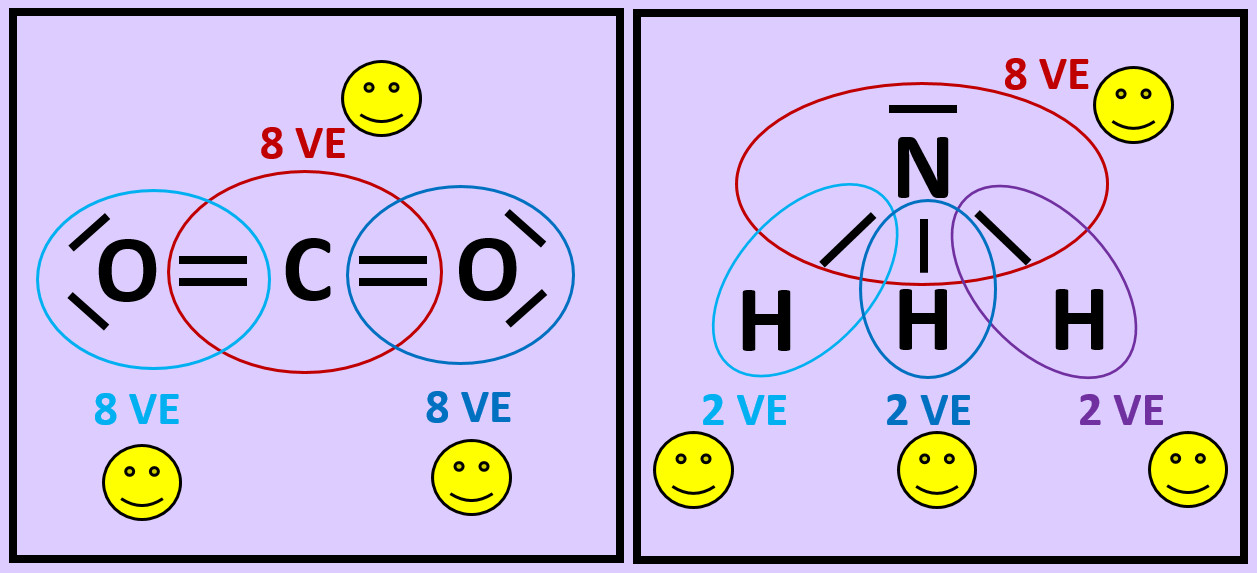
- Wiederholt die vorangegangenen Schritte (Einkreisen der Atome; Zählen der Elektronen; Entscheiden, ob Edelgaskonfiguration vorliegt) für die Moleküle "Kohlenstoffdioxid" (CO2) und "Ammoniak" (NH3)
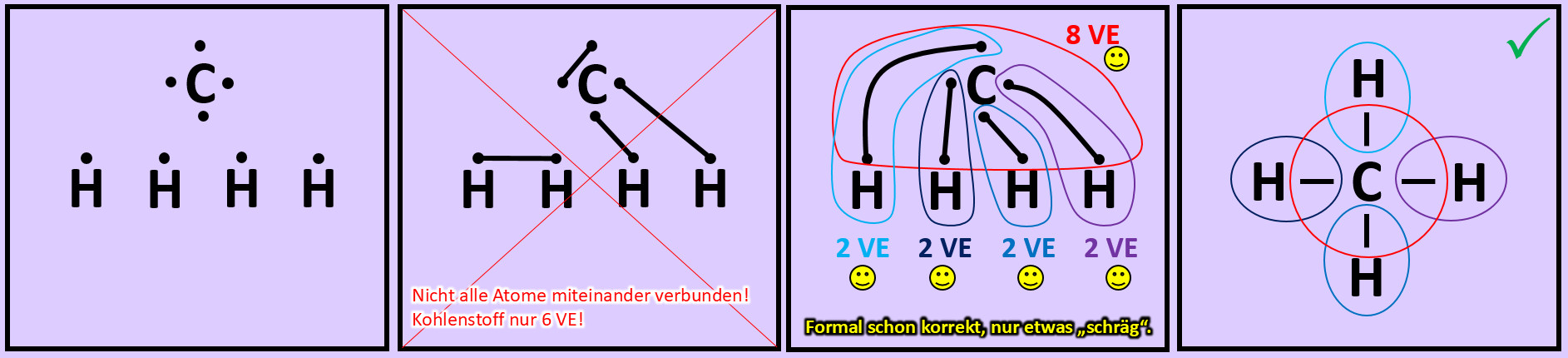
Versucht nun mit Hilfe der Valenzstrichformel selbst ein Molekül zu zeichnen, das ihr noch nicht im Video gesehen habt: "Methan" (CH4). Geht wie folgt vor:
- Zeichnet die Elementsymbole aller fünf Atome auf das Papier. Tipp: Wählt eine möglichst symmetrische Anordnung.
- Zeichnet nun um jeden Atom die richtige Anzahl an Valenzelektronen.
- Versucht nun die Punkte so zu verbinden, dass alle Atome miteinander zusammenhängen und gleichzeitig Edelgaskonfiguration erreicht wird.
- Hinweis: Wenn man die zwei Valenzelektronen von zwei Wasserstoffen miteinander verbindet, dann besitzen zwar diese beiden Edelgaskonfiguration können aber keine weitere Bindung mehr eingehen. Sie können dann mit den restlichen Atomen nicht mehr verknüpft werden. Man muss also nach einer anderen Lösung suchen...
In eurem Buch ist auf der Seite 113 ist ein Verfahren beschrieben, mit dem man die Valenzstrichformeln "berechnen" kann. Ihr dürft das in Zukunft gerne so durchführen. Wenn man etwas übt, dann klappt es aber nach einiger Zeit auch ohne dieses Verfahren. Lest dieses Verfahren jetzt noch nicht, sondern erst als Hausaufgabe.
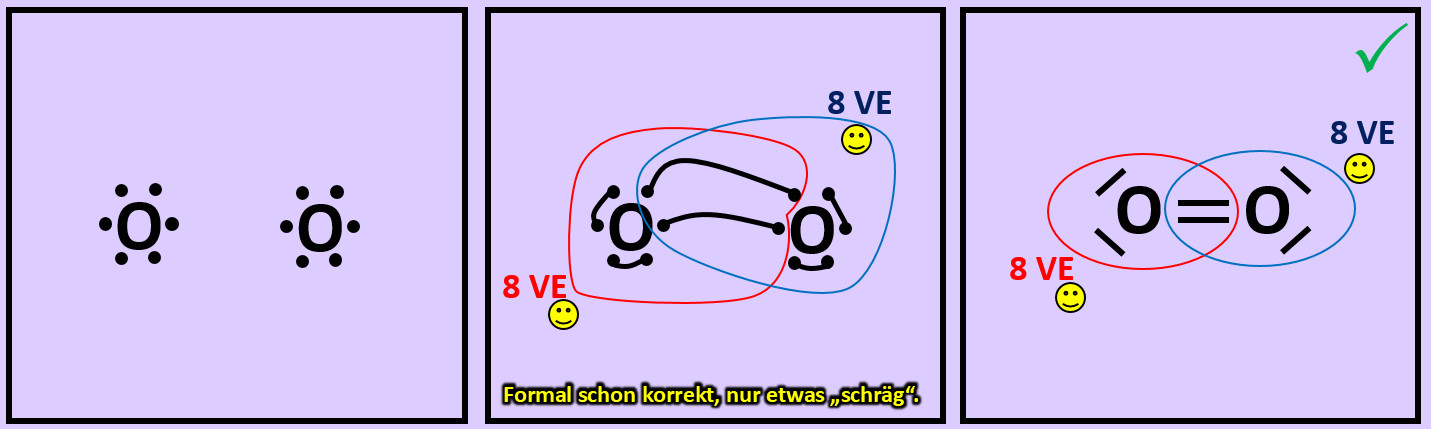
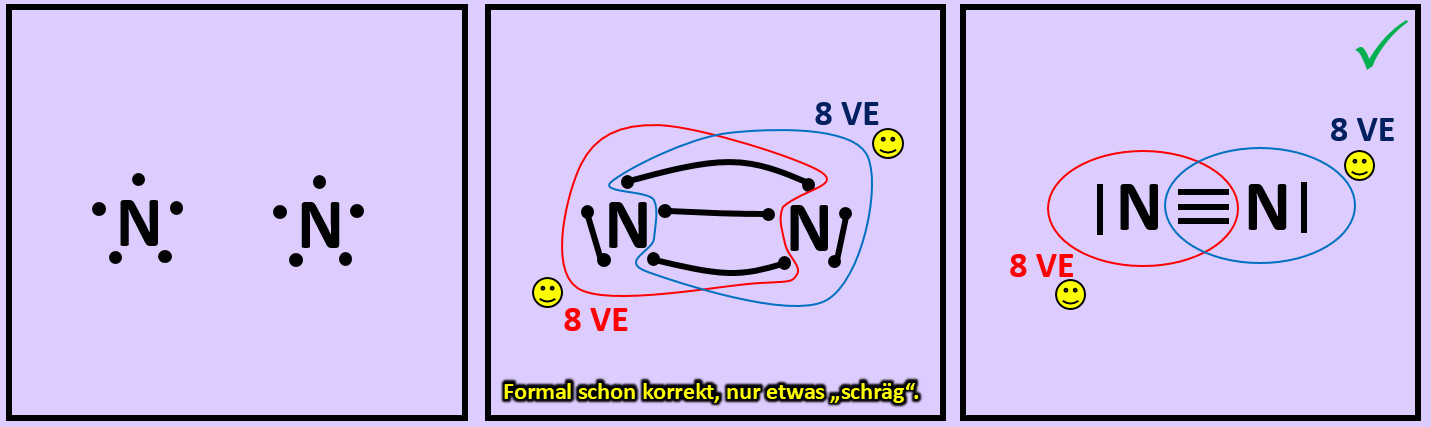
- Versucht erst noch zwei weitere Moleküle mit Hilfe der Valenzstrichformeln darzustellen: "Sauerstoff" (O2) und "Stickstoff" (N2)
- Beim Sauerstoffmolekül sind an der Bindung zwischen den beiden Atomen zwei Elektronenpaare, beim Stickstoffmolekül drei beteiligt. Diese Formen von Bindungen haben eigene Namen. Wie nennt man diese Bindungen?
Beim Sauerstoffmolekül: Doppelbindung, beim Stickstoffmolekül: Dreifachbindung.
Hausaufgabe: Lest im Buch folgende Abschnitte: S. 107 "Das Konzept der Elektronenpaarbindung", S. 108 komplett, S. 109 "Die Molekülformel". (Hinweis: Der Begriff "stöchiometrische Wertigkeit" spielt im meinen Unterricht keine große Rolle.) Bearbeitet die Aufgaben 1 + 3 auf S. 107 und stellt die Valenzstrichformel für Wasserstoffperoxid (H2O2) auf (schwierig).
Arbeitsauftrag Chemie3 (verpflichtend)
Die folgende verpflichtende Unterrichtseinheit hat eine Bearbeitungszeit von ca. 45 Minuten. Ihr benötigt für die Bearbeitung: Das Schulbuch, das PSE, einen Zettel und einen Stift. Und Ruhe. Voraussetzung für die Bearbeitung ist, dass ihr Arbeitsauftrag Chemie2 erledigt habt (vom Mo, 23.03.). Am Ende erhaltet ihr einen Hefteintrag sowohl für die Einheit Chemie2 als auch Chemie3. Den könnt ihr abschreiben (bitte nur im Notfall) oder ausdrucken und einkleben.
Bitte klickt erst auf "Lösung", wenn ihr die Aufgabe wirklich versucht habt zu lösen.
Verbesserung der Hausaufgabe
- Buch S. 107, A1
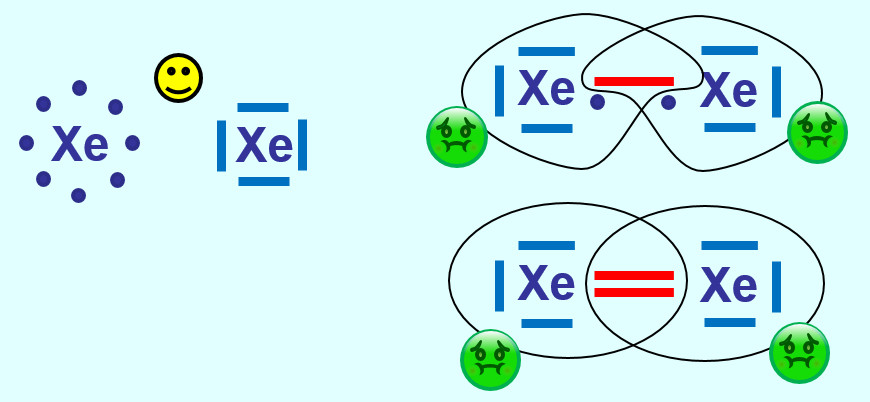
Xenon hat bereits Edelgaskonfiguration (8 VE auf der äußersten Schale). Durch eine (oder mehr) Atombindung(en) mit einem weiteren Xenon-Atom würde dieser energiearme Zustand zerstört werden. Daher kommen alle Edelgase einatomige Gase vor, im Gegensatz zu den anderen elementaren Gasen (wie z.B. Sauerstoff, Stickstoff, Wasserstoff...)
- Buch S. 107, A3

Ein Natrium-Atom könnte mit seinem einen Valenzelektron lediglich eine Atombindung aufbauen. Dadurch käme eine Konfiguration zustanden, bei der dem Atom zwei Elektronen zugeordnet werden können. Das ist weit entfernt von einer Edelgaskonfiguration und daher auch nicht stabil.
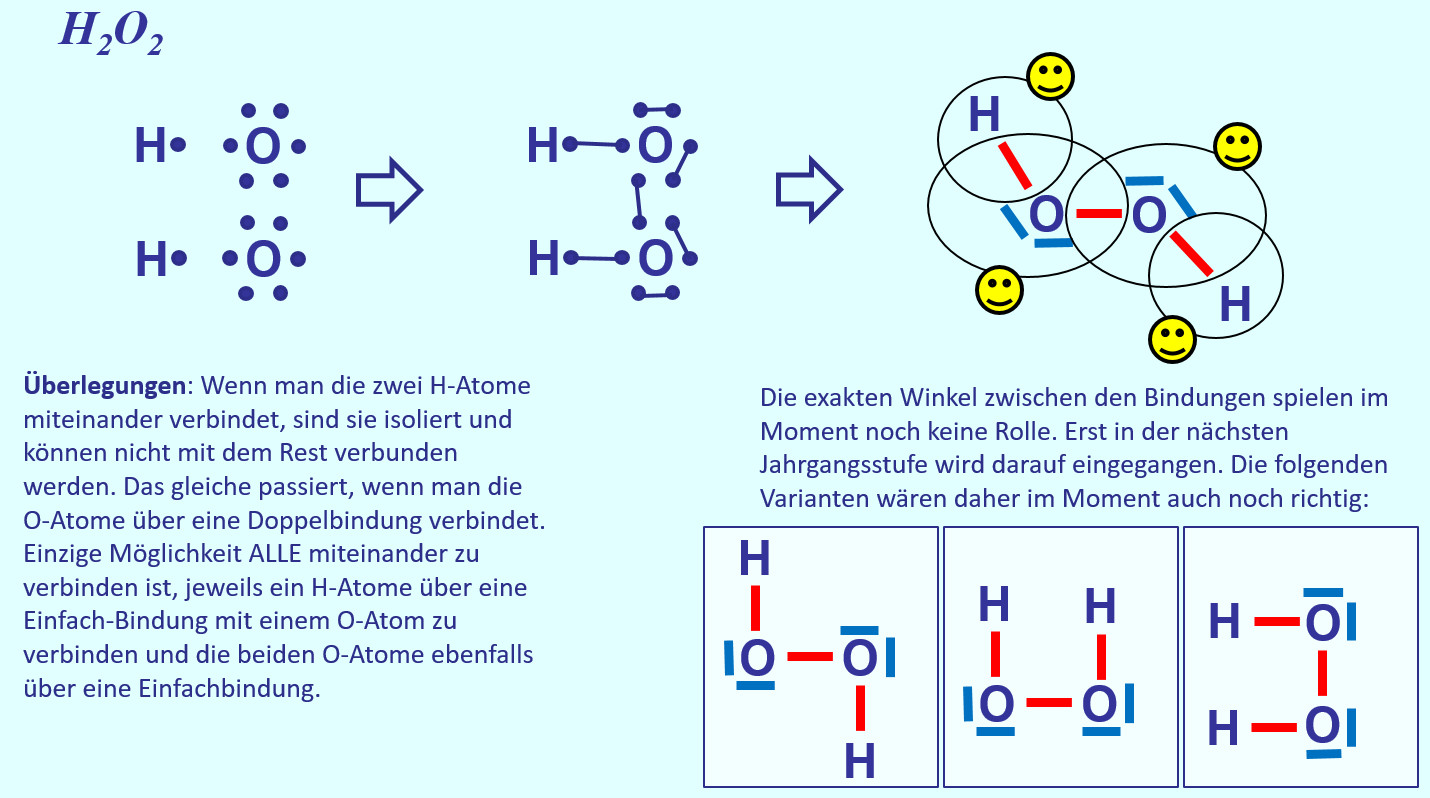
- Zeichne die Valenzstrichformel für Wasserstoffperoxid (H2O2)
Neu: Unterschiede zwischen Salzen und Molekülen
Bevor wir uns einige Spezialfälle beim Aufstellen von Valenzstrichformeln anschauen, soll hier zunächst noch einmal der Unterschied zwischen Salzen und Molekülen etwas genauer beleuchtet werden: Die chemischen Formeln CaF2 und CO2 sehen sich auf den ersten Blick recht ähnlich: Beide enthalten drei Atome, eines davon kommt doppelt vor. Auf Teilchen-Ebene betrachtet bedeuten sie jedoch etwas völlig anderes.
Zunächst zum Calciumfluorid (CaF2): Es gibt kein einzelnes CaF2-Teilchen. CaF2 ist ein Salz und besteht aus sehr vielen Ca2+- und sehr vielen F--Ionen. Alle ziehen aufgrund der unterschiedlichen Ladungen an ihren entgegen gesetzt geladenen Nachbarn, in alle Richtungen. Es entstehen riesige Gebilde, die Salzkristalle. Insgesamt ist das Verhältnis der vorliegenden Ionen in einem solchen Salzkristall aber immer 1 : 2. Nur so können sich die Ladungen exakt neutralisieren und es entsteht ein ungeladener Stoff (wären Salze geladen, würde man z.B. beim Berühren eine elektrischen Schlag bekommen). Das folgende Bild zeigt den Ausschnitt aus einem CaF2-Kristall. Weiß dargestellt sind die Ca2+-Ionen, die F--Ionen grün. Man kann erkennen, dass Calcium-Ionen jeweils von acht Fluorid-Ionen als direkte Nachbarn umgeben sind (der graue Würfel links in der Abbildung), während Fluorid-Ionen jeweils nur von vier Calcium-Ionen als direkte Nachbarn umgeben sind (die graue pyramidenähnliche Figur rechts in der Abbildung). Pro Fluorid-Ion sind also doppelt so viele Calcium-Ionen vorhanden.

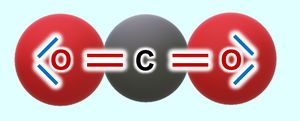
Nun zum Kohlenstoffdioxid (CO2): Hier gibt es tatsächlich einzelne CO2Teilchen. Jeweils eine Doppelbindung verbindet genau ein Sauerstoffatom mit dem zentralen Kohlenstoffatom. Diese drei Atome bilden eine Einheit, eben das Molekül. Mit anderen Teilchen tritt zunächst keine Wechselwirkung auf (später werden wir sehen, dass dies nicht korrekt ist, für den Moment bleiben wir aber bei dieser Annahme).
Woran erkennt man nun, ob ein Salz oder ein Molekül vorliegt? Im Moment ist auch das noch recht einfach: Salze liegen vor, wenn es sich um eine Verbindung aus einem Metall und einem Nichtmetall handelt. Moleküle liegen vor, wenn es sich um eine Verbindung aus Nichtmetallen untereinander handelt.
- Entscheidet, ob es sich bei den folgenden Verbindungen um ein Salz oder einen molekularen Stoff handelt (Im PSE in eurem Buch auf der letzten Seite kann man erkennen, ob ein Element zu den Metallen oder Nichtmetallen gezählt wird): NO2, K2O, Al2O3, N2O3
- NO2: Stickstoff(N) und Sauerstoff (O) sind Nichtmetalle, das bedeutet: NO2 ist ein molekularer Stoff
- K2O: Kalium (K) ist ein Metall, Sauerstoff (O) ein Nichtmetall, das bedeutet: K2O ist ein Salz
- Al2S3: Aluminium (Al) ist ein Metall, Schwefel (S) ein Nichtmetall, das bedeutet: Al2S3 ist ein Salz
- SO3: Schwefel (S) und Sauerstoff (O) sind Nichtmetalle, das bedeutet: SO3 ist ein molekularer Stoff
Zurück zu den Valenzstrichformeln für Moleküle:
In der letzten Unterrichtseinheit habt ihr gesehen, wie man die Valenzstrichformel für Moleküle aufstellt. In eurem Buch ist ein mathematisches Verfahren dazu beschrieben. Ich persönlich finde es etwas umständlich und glaube, das man auch ohne dieses Verfahren auskommt. Einfach indem man sich ein paar sinnvolle Gedanken macht und etwas herumprobiert. Ihr dürft aber gerne das mathematische Verfahren anwenden.
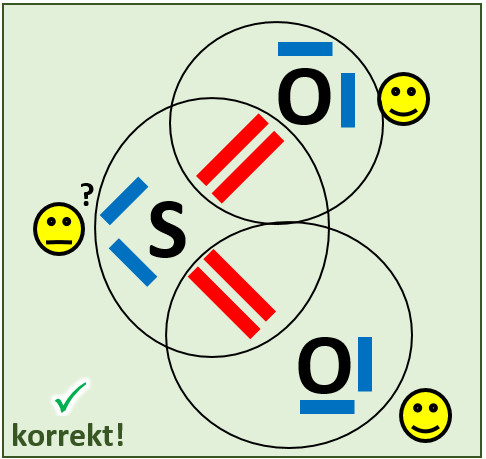
- Versucht nun eine Valenzstrichformel für das Molekül Schwefeldioxid (SO2) aufzustellen!
Wenn ihr etwas Geduld aufgebracht habt, kommt ihr vielleicht zu der folgenden Lösung:
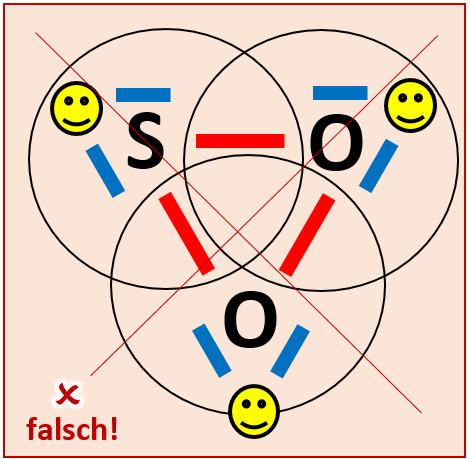
Obwohl hier alle drei Atome Edelgaskonfiguration aufweisen würden, bildet sich dieses Molekül nicht! Diese Lösung ist daher leider falsch. Aber woran liegt das?
Das Problem ist die Geometrie. Ein Effekt, den ich euch im Moment nicht näher erläutern kann, führt dazu, dass Dreiecks- und Vierecks-Verbindungen so gut wie nie stabil sind und sich daher auch (fast) nicht bilden. Die oben abgebildete Variante eines SO2-Moleküls wäre eine Dreiecks-Verbindung.
Wenn ihr weiter versucht, eine Lösung zu finden, werdet ihr vermutlich verzweifeln. Es fehlt euch nämlich noch eine wichtige Zusatzinformation. Zunächst zeige ich euch aber die richtige Strukturformel. Klickt auf "Anzeigen", schaut euch das Molekül an und erklärt, warum diese Variante nach eurem bisherigen Wissenstand falsch sein sollte:
Dem Schwefel-Atom werden in dieser Anordnung zehn Valenzelektronen zugeordnet. Das ist kein Edelgaszustand.
Dennoch ist dieser Zustand stabiler als die Dreiecksverbindung. Man darf allerdings nicht jedem Atom in Molekülen mehr als acht Valenzelektronen zuordnen! Das ist nur möglich, wenn es sich um Elemente der 3. Periode oder noch höher handelt. Für Elemente der 2. Periode gilt die Oktettregel streng (ohne Ausnahme):
Atome besitzen in Verbindungen oft eine Elektronenkonfiguration, bei der auf der äußersten Schale acht Elektronen sitzen.
Nachdem Schwefel ein Element der 3. Periode ist, kann im SO2 das Oktett (also 8 VE) überschritten werden.
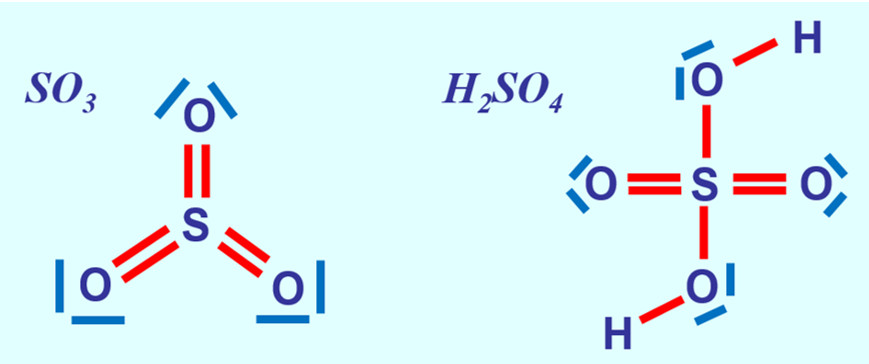
- Wendet dieses neue Wissen jetzt an und stellt die Valenzstrichformeln für Schwefeltrioxid SO3 (leicht) und Schwefelsäure H2SO4 (schwer) auf!
Ihr könnt euch nun die Hefteinträge für die letzten beiden Einheiten herunterladen:
Hier findet ihr noch ein Übungsblatt mit vielen Molekülen, zu denen ihr die Valenzstrichformeln aufstellen könnt. Meine Empfehlung: Macht ab heute jeden Tag als Hausaufgabe drei von der linken und zwei von der rechten Seite. Übung macht den Meister!
Arbeitsauftrag Chemie4
- noch nicht hochgeladen -