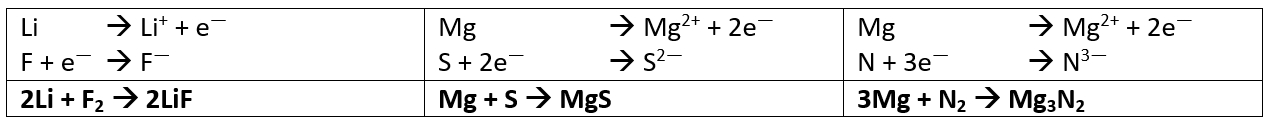9e 2020 21/Chemie
Termine
Schulaufgabe am 07.12.2020 (für Gruppe B)
Schulaufgabe am 08.12.2020 (für Gruppe A)
Prüfungsstoff: Neben Grundwissen, den Hefteinträgen und den Versuchsprotokollen eignen sich folgende Seite im Buch (Galvani Chemie 2) als Vorbereitung für die Schulaufgabe (chronologisch sortiert):
- S. 20 - 21 Unterschied zwischen qualitativen und quantitativen Nachweisen
- S. 22 - 24 Nachweismethoden
- S. 25 - 26 Die Spektralanalyse
- S. 92 - 93 Fällungsreaktionen
- S. 54 - 55 Das Orbitalmodell (Die Inhalte dieser Seite werden nicht direkt in der Schulaufgabe abgefragt, aber zum Verständnis der nächsten Seiten sind sie meiner Meinung schon relevant.
- S. 56 - 57 Der räumliche Bau von Molekülen
- S. 63 - 64 Die polare Atombindung (ohne den letzten Absatz "Polarität und Dissoziationsenergie")
- S. 65 Dipole
- (S. 72 - 73 Zwischenmolekulare Kräfte - Wiederholung)
- S. 76 - 77 Van-der-Waals-Kräfte
- S. 74 - 75 Wasserstoffbrückenbindungen
- S. 78 Einfluss zwischenmolekularer Kräfte auf Stoffeigenschaften
Versuchsprotokolle
Eine Musterlösung für das Versuchsprotokoll zur Übung vom 08.10. "Flammenfärbung von Na- und K-Salzen":
- Zum Herunterladen: Hier klicken
Eine Musterlösung für das Versuchsprotokoll zur Übung vom 22.10. "Nachweis von ausgewählten Halogenid-Ionen":
- Zum Herunterladen: Hier klicken
Grundwissen
Text
Magnesium ist ein sehr reaktives Metall und wird an Schulen häufig in Form von langen Bändern verwendet. Sobald man ein Ende eines solchen Magnesium-Bandes kurz erhitzt, beginnt es mit dem Sauerstoff aus der Luft zu reagieren. Dabei entsteht sehr viel Hitze und Licht. Früher hat man daher Magnesium als „Blitzlicht-Pulver“ eingesetzt. Einmal gestartet, endet die Reaktion erst, wenn das gesamte Magnesium-Band „verbrannt“ ist. Übrig bleibt ein weißer Feststoff: Magnesiumoxid (MgO).
Aufgaben
- Stelle die chemische Reaktionsgleichung für den beschriebenen Prozess auf!
- Ordne diese chemische Reaktion verschiedenen Gruppen zu: Beachte bei der einen Zuordnung den Energieumsatz und bei der anderen Zuordnung die Anzahl der Pro- und Edukte!
- Zeichne das vollständig beschriftete Energie-Zeit-Diagramm dieser Reaktion!
Text + Grafik
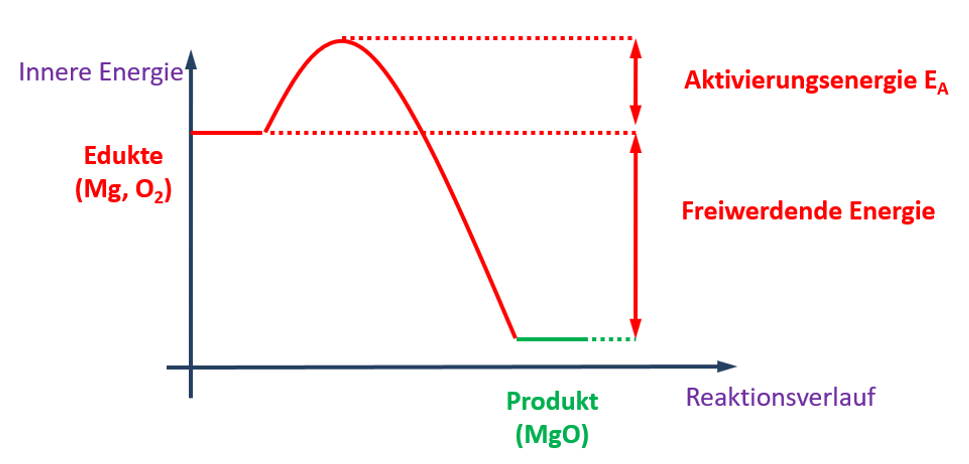
Die folgende Grafik enthält viele Informationen. Leite aus dieser Grafik die folgenden Punkte ab:
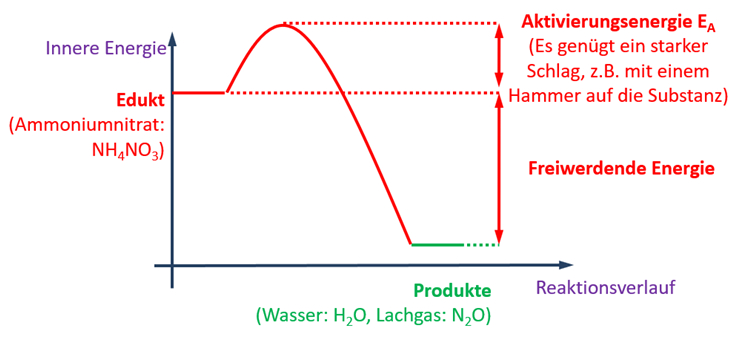
Aufgaben
- Beschreibe mit einem schönen, deutschen Satz die ablaufende Reaktion!
- Stelle die vollständig ausgeglichene Reaktionsgleichung auf!
- Ordne die dargestellte Reaktion zwei Gruppen zu. Betrachte bei der ersten Zuordnung die an der Reaktion beteiligte Energie, bei der der zweiten Zuordnung die Anzahl der vorhandenen Pro- und Edukte!
Atombau
- Bestimme mit Hilfe des PSE die Anzahl an Protonen, Neutronen, Elektronen und Valenzelektronen in einem Atom von Aluminium, Arsen und Antimon!
- Finde in den Hauptgruppen des PSE das Element, bei dem ein Atome zwei Valenzelektronen und 50 Neutronen besitzt!
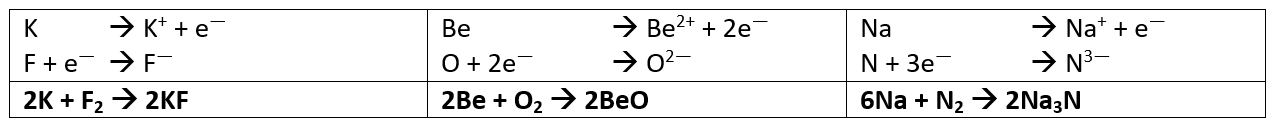
Salzgleichungen
- Stelle die chemischen Gleichungen zur Bildung der folgenden Salze aus den Elementen auf: Kaliumfluorid (aus Kalium und Fluor), Berylliumoxid (aus Beryllium und Sauerstoff) und Natriumnitrid (aus Natrium und Stickstoff)
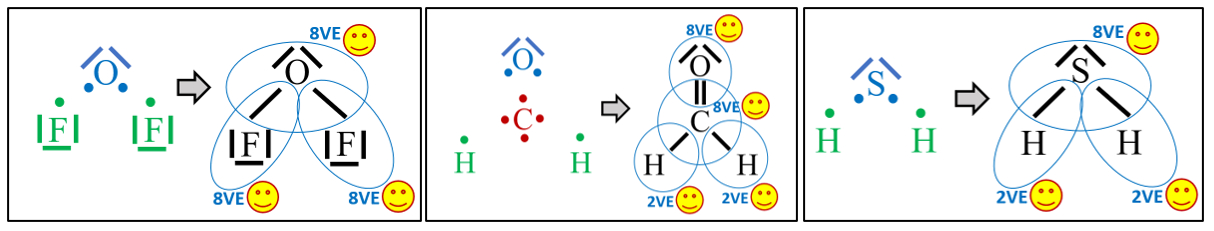
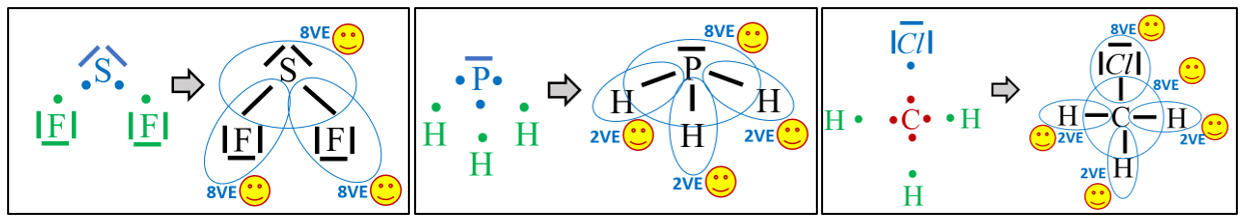
Moleküle
- Zeichne die Valenzstrichformel der folgenden Moleküle: Sauerstoffdifluorid (OF2), Formaldehyd (CH2O) und Schwefelwasserstoff (H2S)
Atombau
- Bestimme mit Hilfe des PSE die Anzahl an Protonen, Neutronen, Elektronen und Valenzelektronen in einem Atom von Bor, Brom und Barium!
- Finde in den Hauptgruppen des PSE das Element, bei dem ein Atome drei Valenzelektronen und 14 Neutronen besitzt!
Salzgleichungen
- Stelle die chemischen Gleichungen zur Bildung der folgenden Salze aus den Elementen auf: Lithiumfluorid (aus Lithium und Fluor), Magnesiumsulfid (aus Magnesium und Schwefel) und Magnesiumnitrid (aus Magnesium und Stickstoff)
Moleküle
- Zeichne die Valenzstrichformel der folgenden Moleküle: Schwefeldifluorid (SF2), Phosphan (PH3) und Chlormethan (CH3Cl)