Corona-Arbeitsaufträge (Chemie) LUX: Unterschied zwischen den Versionen
Aus RMG-Wiki
KKeine Bearbeitungszusammenfassung Markierung: 2017-Quelltext-Bearbeitung |
(AA C5 hierhin verschoben) Markierung: 2017-Quelltext-Bearbeitung |
||
| Zeile 240: | Zeile 240: | ||
}} | }} | ||
== Arbeitsauftrag Chemie4 == | == Arbeitsauftrag Chemie4 (verpflichtend) == | ||
* Die folgende verpflichtende Unterrichtseinheit hat eine Bearbeitungszeit von ca. 45 Minuten. | |||
* Ihr benötigt für die Bearbeitung: Das Schulbuch, das PSE, einen Zettel, Stift, Internetzugriff um ein Video zu schauen. Und Ruhe. | |||
* Bitte bearbeitet die gestellten Aufgaben tatsächlich erst selbst, bevor ihr auf die Lösung klickt!</span><br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Das Energie-Abstands-Diagramm'''</span> | |||
|Inhalt= | |||
Ihr habt sicher im Buch gesehen, dass ich einen Abschnitt im Buch zum Kapitel Atombindung ausgelassen habe: Das Diagramm auf der S. 106. Dieses Diagramm soll heute besprochen werden. Ihr braucht das Diagramm jetzt noch nicht anschauen, zunächst möchte ich euch sagen, welche Fragen dieses Diagramm beantworten kann: | |||
* Untersucht man ein Wasserstoff-Molekül (H<sub>2</sub>) genauer, stellt man fest, dass sich die beiden Atomkerne in einem ganz bestimmten Abstand zueinander aufhalten. Dieser Abstand wird '''Bindungsabstand '''genannt. Er ist bei allen Wasserstoffmolekülen gleich. Warum? - Das ist eine Frage, auf die das Diagramm eine Antwort geben kann. | |||
* Wasserstoff kommt immer als "Pärchen" vor, also als Molekül (H<sub>2</sub>). Ihr habt in der letzten Einheit gelernt, dass durch das Teilen von Elektronen über eine '''Atombindung '''Edelgaszustand erreicht werden kann. Man kann mit sehr viel Aufwand die beiden Wasserstoff-Atome eines Moleküls schon voneinander trennen. Aber sie finden sich sofort wieder zum Molekül zusammen. Dabei wird eine große Menge Energie frei, die '''Bindungsenergie'''. Das Diagramm im Buch kann auch erklären, warum das so ist. | |||
<br><br> | |||
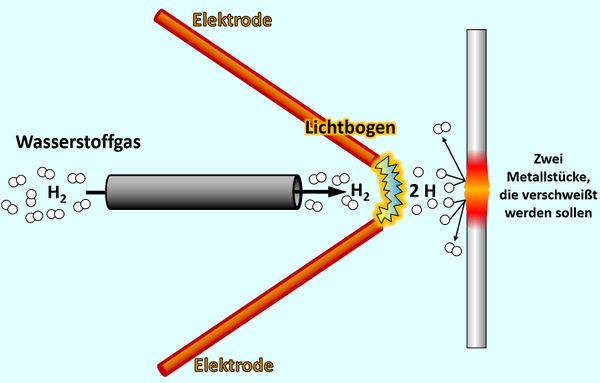
Beginnen wir mit dem letzten Punkt: Die folgende Abbildung zeigt schematisch eine Langmuir-Fackel, benannt nach einem US-amerikanischen Physiker und Chemiker, der diese Apparatur 1924 entwickelte. Man kann damit metallische Werkstücke verschweißen. Beschreibe diese Grafik: Mache Dir Stichpunkte auf einem Zettel. <br> | |||
[[Datei:A4_E_Abstandsdiagramm_LangmuirFackel.jpg|600px]]<br> | |||
{{Lösung versteckt| | |||
Über ein Röhrchen strömt Wassserstoff-Gas (besteht aus H<sub>2</sub>-Molekülen) zwischen zwei Elektroden hindurch. Von der einen zur anderen Elektrode spannt sich ein Lichtbogen (der wird durch eine sehr hohe Spannung erzeugt, die man an den Elektroden anlegt). Beim Durchtritt durch den Lichtbogen werden die Wasserstoff-'''Moleküle''' in einzelne Wasserstoff-'''Atome''' gespalten. Diese prasseln auf zwei metallische Werkstücke, die verschweißt werden sollen. Beim Auftreffen verbinden sich jeweils zwei Wasserstoff-'''Atome '''wieder zu einem Wasserstoff-'''Molekül'''. Dabei werden große Energiemengen frei, welche die metallischen Werkstücke so stark erhitzen, dass sie miteinander verschmelzen. | |||
|Lösung 1|Lösung ausblenden}} | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#070">'''optional (freiwillig) '''</span> | |||
|Inhalt= | |||
Je nachdem, ob ein Familienmitglied gerade Zeit hat oder nicht, kannst Du folgendes probieren: Gehe mit Deinem Zettel zu einem Familienmitglied. Erkläre ihm, wie eine Langmuir-Fackel funktioniert. Lass das Familienmitglied die Langmuir-Fackel nach Deinen Anweisungen zeichnen. Vergleicht dann die Zeichnung mit der Skizze hier. <br> | |||
Das geht auch "fernmündlich": Ruft jemanden an, der nach euren Anweisungen am Telefon die Skizze anfertigt. Anschließend soll euch derjenige ein Foto von seiner Zeichnung schicken. | |||
|Farbe= #070 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFC | |||
|Hintergrund= #DFC | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Das Diagramm'''</span> | |||
|Inhalt= | |||
Was für euch an dieser Langmuir-Fackel wichtig ist, sind die Prozesse '''nach '''dem Lichtbogen: Zwei Wasserstoff-'''Atome verbinden sich '''wieder zu einem Wasserstoff-'''Molekül'''. Dabei werden große '''Energiemengen frei'''. <br> | |||
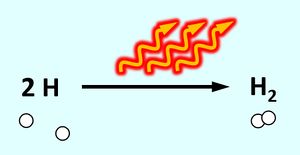
Es handelt sich um eine '''exotherme Reaktion''': Das "System" aus zwei Wasserstoff-Atomen enthält viel Energie, wenn sich beide zu einem Wasserstoff-Molekül vereinigen enthält dieses "System" weniger Energie. Die Energiedifferenz wird in diesem Beispiel als Wärme frei und erhitzt die metallischen Werkstücke. Als chemische Gleichung könnte man das z.B. so darstellen:<br> | |||
[[Datei:A4_E_Abstandsdiagramm_RGl_2HzuH2.jpg|300px]]<br> | |||
<br> | |||
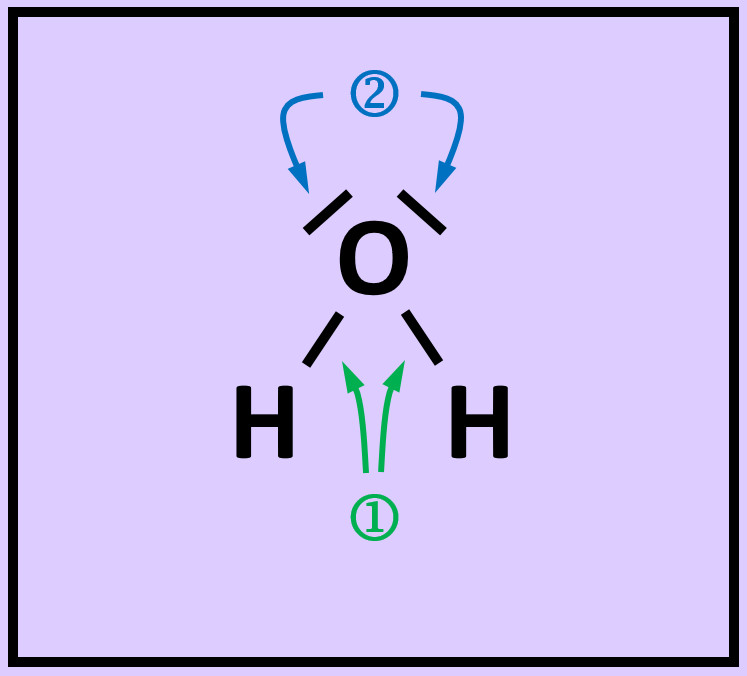
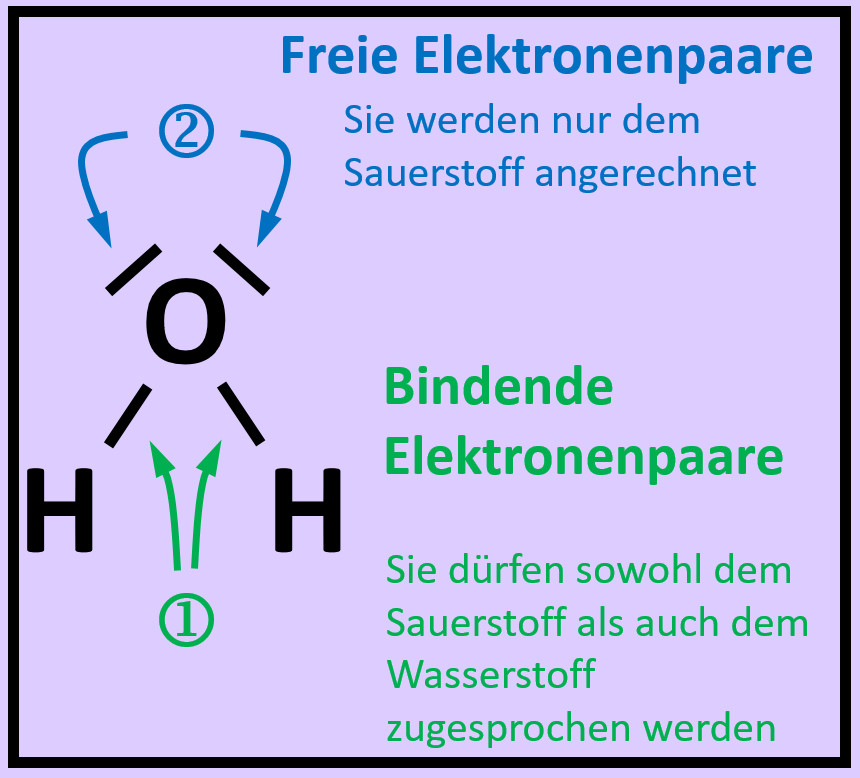
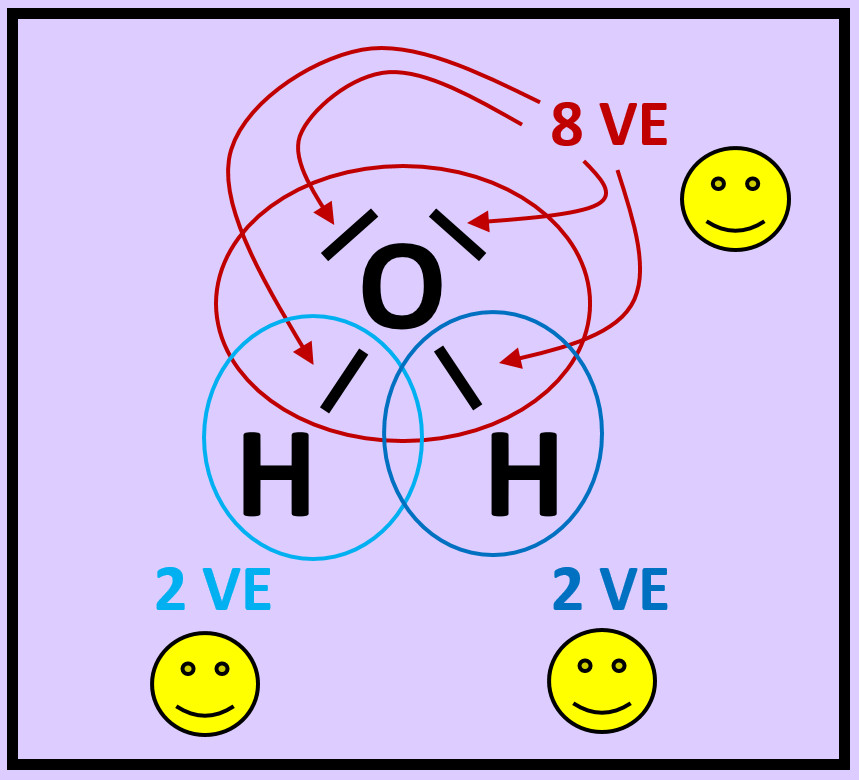
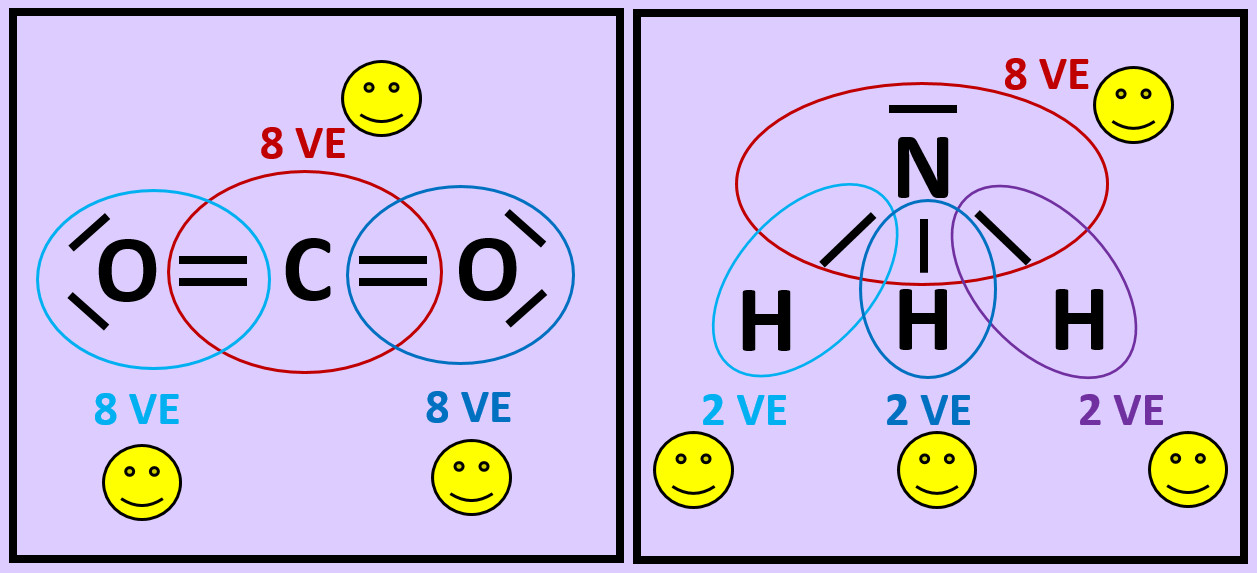
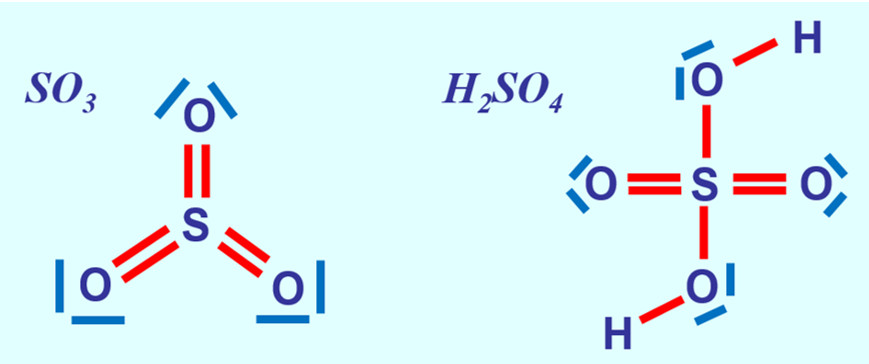
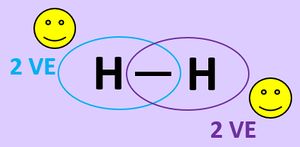
Es ist für zwei Wasserstoff-Atome also energetisch günstiger, wenn sie als Molekül vorkommen. In der letzten Stunde haben wir das auch anschaulich begründet: Durch das '''Teilen von Elektronen''' über die '''Atombindung''' können jedem Wasserstoff-Atom zwei Valenzelektronen zugeordnet werden, was einer Edelgaskonfiguration entspricht.<br> | |||
[[Datei:A4_E_Abstandsdiagramm_2_Valenzstrich.jpg|300px]]<br> | |||
<br> | |||
Die Grafik in eurem Buch versucht diese Bindung noch etwas genauer zu erklären.<br> | |||
* Lest jetzt im Buch auf den S. 106 - 107 die Abschnitte mit den Überschriften "Nichtmetalle reagieren miteinander", "Warum ist das Wasserstoffmolekül so stabil" und "Das bindende Elektronenpaar" | |||
* Versucht die Grafik (S. 106) zu interpretieren (1. Die Grafik zeigt... in Abhängigkeit von..., 2. Verlauf beschreiben, 3. Verlauf erklären) | |||
Ich glaube, dass anhand des Textes die Grafik schwierig zu verstehen ist. Vielleicht täusche ich mich aber auch. Falls ihr die Grafik nicht interpretieren könnt, hier ein Hilfsvideo: | |||
* Das Video ist mit Absicht ohne Ton. | |||
* Am oberen Bildrand wird immer erst ein Text eingeblendet, nach kurzer Verzögerung erfolgt (meist) eine Animation. | |||
* Wenn es euch zu schnell geht, dann drückt immer wenn sich der Text ändert kurz auf Pause, lest den Text in Ruhe und schaut euch dann die Animation an. | |||
<br> | |||
[[Datei:Atombdg_E_Abstands_Diagramm.mp4|600px]] <br> | |||
Jetzt sollte die Interpretation besser klappen, also los: | |||
* Die Grafik zeigt... in Abhängigkeit von... | |||
* Beschreibung des Verlaufs | |||
* Erklärung | |||
{{Lösung versteckt| | |||
* Die Grafik zeigt den Energiegehalt von zwei Wasserstoffatomen, die sich annähern in Abhängigkeit vom Abstand der Atomkerne. | |||
* Sind die beiden Kerne sehr weit voneinander entfernt, ist die Energie dieses Systems 0. Nähern sich die Atomkerne an, nimmt die Energie des Systems ab, bis zu einem Minimum. Nähert man die Kerne noch näher an, steigt der Energiegehalt des Systems sehr rasch an. | |||
* Begründung: Durch die Annäherung der Atome aneinander können die Elektronenhüllen sich immer besser überlappen. Das Teilen der Elektronen wird dadurch immer einfacher, das erklärt die Abnahme der Energie des Systems bis zu einem bestimmten Punkt. Nähert man die Atome noch näher an, beginnt nun die Abstoßung der positiv geladenen Kerne relevant zu werden und man muss Energie in das System hineinstecken. Der Kern-Abstand an dem der Energiegehalt des Systems am niedrigsten ist, nennt man '''Bindungsabstand''', die Energiedifferenz zwischen diesem Punkt und der "0-Linie" nennt man '''Bindungsenergie'''. | |||
|Lösung 2|Lösung ausblenden}} | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#070">'''optional (freiwillig) '''</span> | |||
|Inhalt= | |||
Wie oben: Je nachdem, ob ein Familienmitglied gerade Zeit hat oder nicht, kannst Du folgendes probieren: Gehe mit Deiner schriftlichen Lösung zu einem Familienmitglied. Beschreibe ihm die Grafik anhand Deiner Notizen, nach denen es die Grafik nachzeichnen soll. Vergleicht dann die Zeichnung mit der Grafik im Buch. <br> | |||
Das geht auch "fernmündlich": Ruft jemanden an, der nach euren Anweisungen am Telefon die Grafik anfertigt. Anschließend soll euch derjenige ein Foto von seiner Zeichnung schicken. | |||
|Farbe= #070 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFC | |||
|Hintergrund= #DFC | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#607">'''Aufgabe'''</span> | |||
|Inhalt= | |||
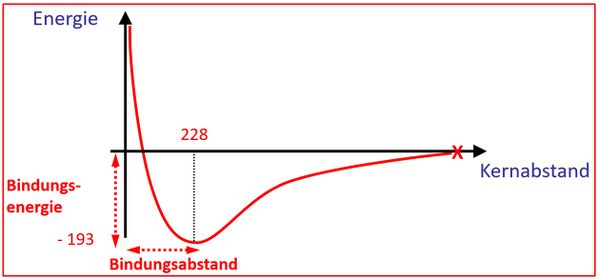
* Bei einem Brom-Molekül (Br<sub>2</sub>) beträgt der Bindungsabstand 228''pm'' (Pikometer) und die Bindungsenergie beträgt 193''kJ/mol'' (Kilojoule pro Mol). Zeichne ein vollständig beschriftetes Energie-Abstands-Diagramm für die theoretische Annäherung zweier Brom-Atome aneinander! Achte darauf, dass sich auch die eingangs genannten Werte in der Zeichnung wiederfinden! | |||
{{Lösung versteckt| | |||
[[Datei:A4_E_Abstandsdiagramm_A1_ML.jpg|600px]] | |||
|Lösung 3|Lösung ausblenden}} | |||
|Farbe= #607 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DCF | |||
|Hintergrund= #DCF | |||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#070">'''Hausaufgabe '''</span> | |||
|Inhalt= | |||
Als Hausaufgabe bearbeitet ihr bitte S. 107 A4. Die Lösung wird erst am Mittwoch hochgeladen. | |||
|Farbe= #070 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFC | |||
|Hintergrund= #DFC | |||
}} | |||
<br> | |||
== Arbeitsauftrag Chemie5 (verpflichtend) == | |||
''- noch nicht hochgeladen - '' | ''- noch nicht hochgeladen - '' | ||
Version vom 29. März 2020, 18:32 Uhr
Arbeitsauftrag Chemie1
Arbeitsauftrag Chemie2 (verpflichtend)
Arbeitsauftrag Chemie3 (verpflichtend)
Arbeitsauftrag Chemie4 (verpflichtend)
- Die folgende verpflichtende Unterrichtseinheit hat eine Bearbeitungszeit von ca. 45 Minuten.
- Ihr benötigt für die Bearbeitung: Das Schulbuch, das PSE, einen Zettel, Stift, Internetzugriff um ein Video zu schauen. Und Ruhe.
- Bitte bearbeitet die gestellten Aufgaben tatsächlich erst selbst, bevor ihr auf die Lösung klickt!
Arbeitsauftrag Chemie5 (verpflichtend)
- noch nicht hochgeladen -