Benutzer:Thomas Lux/Test Q11-Struktur: Unterschied zwischen den Versionen
KKeine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
KKeine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
||
| Zeile 301: | Zeile 301: | ||
|Rahmenfarbe= #DCF | |Rahmenfarbe= #DCF | ||
|Hintergrund= #DCF | |Hintergrund= #DCF | ||
}} | |||
<br> | |||
{{Box-spezial | |||
|Titel=<span style="color:#080">Das war es für heute</span> | |||
|Inhalt= | |||
Am Mittwoch gibt es eine Zusammenfassung von allem, was wir in diesem Schuljahr gemacht haben. | |||
<br> | |||
|Farbe= #080 | |||
|Rahmen= 0 | |||
|Rahmenfarbe= #DFB | |||
|Hintergrund= #DFB | |||
}} | }} | ||
<br> | <br> | ||
Version vom 1. Mai 2020, 17:11 Uhr
Hier im Schulwiki findet jede Klasse auf der jeweiligen Klassenseite alle Arbeitsaufträge, die erledigt werden sollten. Die Stunden orientieren sich am Stundenplan der Klasse.
Stöbern in anderen Klassen ist erlaubt!
Um in den Ferien keine Langeweile aufkommen zu lassen gibt es für alle Klassen eine
- Ideenbörse für Kollegen
- Tipps und Tricks zum Arbeiten im Wiki
- Basismodule]
- Digitale Didaktik
- Fortbildungskonzept
- Mitdenken! Mitreden! Mitgestalten!
- Pädagogischer Tag Kollaboration
- Bildung für nachhaltige Entwicklung
Unterstufe
- 5a - 5b - 5c - 5d - 5e - 5f - M5 - E5 - Eth5
- 6a - 6b - 6c - 6d - 6e - E6
- 7a - 7b - 7c - 7d
Mittelstufe
- 8a - 8b - 8c - 8d - 8e - E8
- 9a - 9b - 9c - 9d - WR9
- 10a - 10b - 10c - 10d - 10e - M10 - WR10
Q11-Kurse
- Astronomie (Link Ast): AST1
- Bio: 1b1 - 1b2 - 1b3 - 1b4 - 1b5
- Chemie: 1c1 - 1c2
- Deutsch: 1d1 - 1d2 - 1d3 - 1d4 - 1d5 - 1d6 - 1d7
- Englisch:
- Englisch Konversation:
- Ethik:
- Evangelische Religionslehre:
- Französisch:
- Geschichte:
- Geographie:
- Informatik:
- Katholische Religionslehre:
- Kunst:
- Latein:
- Mathematik:
- Musik:
- Physik:
- Rhetorik:
- Sozialkunde:
- Sport:
- Spanisch (spätbeginnend):
- Sport-Theorie:
- Wirtschaft:
Q12-Kurse
- Bio: 1b1 - 1b2 - 1b3 - 1b4 - 1b5
- Chemie: 1c1 - 1c2
- Deutsch: 1d1 - 1d2 - 1d3 - 1d4 - 1d5 - 1d6 - 1d7
- Englisch:
- Ethik:
- Evangelische Religionslehre:
- Französisch:
- Geschichte:
- Geographie:
- Informatik:
- Katholische Religionslehre:
- Kunst:
- Latein:
- Mathematik:
- Musik:
- Physik:
- Astrophysik:
- Sozialkunde:
- Sport:
- Spanisch (spätbeginnend):
- Sport-Theorie:
- Wirtschaft:
W-Seminare Q11 + Q12
Q11
- 1W01: Klassiker der dt. Literatur (D)
- 1W02: Klassiker der engl. Literatur (E)
- 1W03: Klassiker der franz. Literatur (F)
- 1W04: Klassiker der biologischen Literatur (B)
- 1W05: Klassiker der chemischen Literatur (C)
- 1W06: Klassiker der mathematischen Literatur (M)
- 1W07: Klassiker der geschichtlichen Literatur (G)
- 1W08: Klassiker der sportlichen Literatur (Spo)
- 1W09: Klassiker der musikalischen Literatur (Mu)
- 1W10: Klassiker der künstlerischen Literatur (Ku)
- 1W11: Klassiker aller Klassiker (K)
Q12
- 2W01: Klassiker der dt. Literatur (D)
- 2W02: Klassiker der engl. Literatur (E)
- 2W03: Klassiker der franz. Literatur (F)
- 2W04: Klassiker der biologischen Literatur (B)
- 2W05: Klassiker der chemischen Literatur (C)
- 2W06: Klassiker der mathematischen Literatur (M)
- 2W07: Klassiker der geschichtlichen Literatur (G)
- 2W08: Klassiker der sportlichen Literatur (Spo)
- 2W09: Klassiker der musikalischen Literatur (Mu)
- 2W10: Klassiker der künstlerischen Literatur (Ku)
- 2W11: Klassiker aller Klassiker (K)
P-Seminare Q11 + Q12
Q11
- 1P01: Klassiker der dt. Literatur (D)
- 1P02: Klassiker der engl. Literatur (E)
- 1P03: Klassiker der franz. Literatur (F)
- 1P04: Klassiker der biologischen Literatur (B)
- 1P05: Klassiker der chemischen Literatur (C)
- 1P06: Klassiker der mathematischen Literatur (M)
- 1P07: Klassiker der geschichtlichen Literatur (G)
- 1P08: Klassiker der sportlichen Literatur (Spo)
- 1P09: Klassiker der musikalischen Literatur (Mu)
- 1P10: Klassiker der künstlerischen Literatur (Ku)
- 1P11: Klassiker aller Klassiker (K)
Q12
- 2P01: Klassiker der dt. Literatur (D)
- 2P02: Klassiker der engl. Literatur (E)
- 2P03: Klassiker der franz. Literatur (F)
- 2P04: Klassiker der biologischen Literatur (B)
- 2P05: Klassiker der chemischen Literatur (C)
- 2P06: Klassiker der mathematischen Literatur (M)
- 2P07: Klassiker der geschichtlichen Literatur (G)
- 2P08: Klassiker der sportlichen Literatur (Spo)
- 2P09: Klassiker der musikalischen Literatur (Mu)
- 2P10: Klassiker der künstlerischen Literatur (Ku)
- 2P11: Klassiker aller Klassiker (K)
neuer Test
Kann man in einer "Lösung versteckt"-Box eine "Lösung versteckt"-Box integrieren?
Bist Du wirklich fertig mit der Lösung? Hast Du wirklich drei schön gezeichnete Skizzen vor Dir liegen?
Also gut, ich will Dir mal glauben. Dann hier die Lösung:
Arbeitsauftrag Chemie10
In der letzten Einheit habt ihr die Metallbindung kennengelernt und ein Video geschaut. Zunächst zur Wiederholung: Beschreibt mit Worten, warum ein Metall bei Raumtemperatur in der Regel ein Feststoff ist, was die Metall-Atome also zusammenhält!
In eurer Beschreibung sollten folgenden Fachbegriffe auftauchen:
- dichteste Kugelpackung
- positiv geladene Atomrümpfe
- negativ geladenes Elektronengas
Die Begriffe sollten in "schöne", zusammenhängende Sätze eingebettet sein. Vor allem sollte klar werden, dass die Anziehungskräfte der am aufbau beteiligten Teilchen durch die unterschiedlichen Ladungen zustande kommen. Und, dass diese starken Anziehungskräfte für den Aggregatszustand (fest) verantwortlich sind
Eine Möglichkeit, zu testen, ob eure Antwort gut war: Lest Sie z. B. euren Eltern vor. Wenn Sie euch sagen, dass es gut war, dann entweder weil es wirklich gut war, oder weil sie euch einfach lieb haben oder beides. (Ich gehe davon aus, dass euch eure Eltern immer lieb haben, aber das sollte nicht der Grund dafür sein, zu sagen, eure Antwort auf die Frage war gut.) Wenn ihr euch nicht sicher seid, schickt mir eure Lösung über den Schulmanager. Von mir bekommt ihr ein rein fachliches Feedback.
Im Video wurde bereits gezeigt, dass viele typischen Eigenschaften von Metallen (elektrische Leitfähigkeit, Wärmeleitfähigkeit, Verformbarkeit) mit dem Aufbau zusammenhängen. In eurem Buch sind diese Zusammenhänge etwas ausführlicher und relativ gut erklärt. Ihr habt zwei Möglichkeiten:
- Lest im Buch S. 128 - 129 (Abs. 1, 2 u. 3)
- Schaut noch einmal das Video (ich empfehle aber das Buch - im Video kommt dieser Aspekt etwas kurz)
Schließt jetzt das Buch und legt es weg! - Zeichnet dann aussagekräftige Skizzen, welche die folgenden Eigenschaften von Metallen gut verdeutlichen (möglichst kein Text, höchstens Beschriftungen)!
- elektrische Leitfähigkeit
- Wärmeleitfähigkeit
- Verformbarkeit
Klickt bitte wirklich erst auf "Lösung" wenn ihr für jede Eigenschaft mindestens eine schöne Skizze habt!
Hast Du wirklich mind. 3 Skizzen vor Dir liegen???
Ein freiwilliger Versuch. Ihr benötigt dazu:
- heißes Wasser
- einen Metall-Löffel
- einen Holz- oder Plastiklöffel (es muss kein Löffel sein, irgendein länglicher Gegenstand ist o.k. er sollte nur ungefähr genauso groß wie der Metall-Löffel sein)
Durchführung:
- Bringt in einem kleinen Topf Wasser zum Kochen (solltet ihr das noch nie gemacht haben, fragt einen Erwachsenen, er euch hilft)
- Wenn das Wasser kocht, reduziert die Hitze des Herdes stark. Das Wasser soll nicht stark sprudeln sondern nur leicht vor sich hin köcheln.
- Nehmt den Metall-Löffel mit der rechte und den Plastik-/Holzlöffel mit der linken Hand gleichzeitig zwischen Daumen und Zeigefinger.
- Taucht beide Löffel gleichzeitig in das heiße Wasser. Sobald ein Löffel zu heiß wird, lasst los!
Beschreibt das Ergebnis und liefert eine Erklärung.
Wenn ihr nicht zu den Menschen gehört, bei denen das Schmerz-Empfinden gestört ist, dann solltet ihr den Metall-Löffel deutlich früher losgelassen haben.
Begründung: Metalle sind sehr gute Wärmeleiter. Ein heißer Gegenstand auf Teilchen-Ebene betrachtet bedeutet nichts anderes als schnell hin und her schwingende Teilchen. Im Metall sind frei bewegliche Elektronen vorhanden, die sehr leicht Schwingnen aufnehmen und weitergeben können. Auch die positiv geladenen Atomrümpfe sind nicht sehr starr an ihren Platz gebunden und können gut schwingen.
Entlang des Metall-Löffels breitet sich die Hitze des kochenden Wassers also viel schneller aus, als im Holz oder Plastik.
Am Mittwoch gibt es eine Zusammenfassung von allem, was wir in diesem Schuljahr gemacht haben.
Arbeitsauftrag für den 04.05.
Pflicht: Sucht bei euch zu Hause drei völlig verschiedene Lebensmittel, die sauer sind (mit "völlig verschieden" meine ich, dass ihr nicht so etwas findet wie "Äpfel" und "Birnen").
Freiwillig: Versucht zu recherchieren, welches Molekül für den sauren Geschmack des Lebensmittels verantwortlich ist!
- z.B.: Essig - Essigsäure (CH3-COOH)
- z.B.: Zitronen (allgemein Früchte) - Zitronensäure (C6H8O7)
- z.B.: Joghurt (allgemein Sauermilchprodukte) - Milchsäure (C3H6O3)
- z.B.: Limo (allgemein sprudelnde Getränke) - Kohlensäure (H2CO3)
In der letzten Einheit habt ihr gesehen, dass es Moleküle mit einer polaren Atombindung zwischen einem elektronegativen Atom und einem Wasserstoff-Atom gibt, die heterolytisch ein Proton abspalten können. Hier noch einmal verschiedene Darstellungsformen am Beispiel von Hydrogenchlorid (HCl).
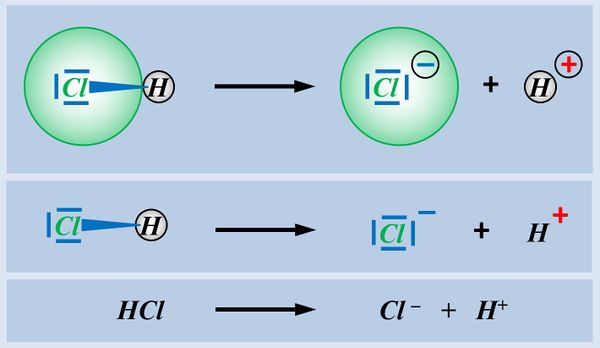
Moleküle, bei denen eine derartige Reaktion möglich ist, nennt man Säuren. Typische Eigenschaften von Säuren sind z.B. der "saure Geschmack" oder "greifen unedle Metalle an". Diese Eigenschaften sind auf das abspaltbare Proton zurückzuführen.
Sicher können sich diejenigen, die Chemie schon länger in der Schule hatten erinnern, dass es zu Säuren einen "Gegenspieler" gibt. Wie heißen diese Gegenspieler?
Basen oder Laugen (als Lauge bezeichnet man in der Regel eine wässrige Lösung einer Base)
Diese Gegenspieler sind in der Lage, die saure Wirkung von Säuren zu neutralisieren, also aufzuheben. Dazu gleich ein Versuch. Vorher noch etwas Theorie: Wenn die saure Wirkung einer Säure darauf beruht, dass die Säure-Teilchen ein Proton abgeben, welche Fähigkeit muss dann ein solches Gegenspieler-Teilchen besitzen, wenn es diese Wirkung aufzuheben vermag?
Es muss in der Lage sein, ein Proton aufzunehmen
Ein einfaches Molekül, dass in der Lage ist, ein Proton aufzunehmen ist NH3 (Ammoniak). Der Vorgang ist hier dargestellt. Beschreibt die Abbildung mit Worten und unter Verwendung von Fachbegriffen:
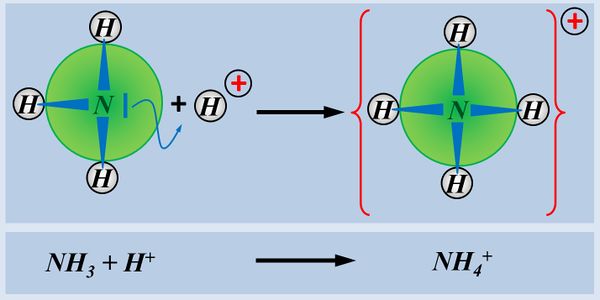
Das Ammoniak-Molekül NH3 stellt sein freies Elektronen-Paar für eine Atombindung mit einem Proton zur Verfügung
Was ist der Unterschied zwischen dieser neu gebildeten Atombindung im Vergleich zu einer "normalen" Atombindung, wie ihr sie früher kennengelernt habt?
Bei der Bildung einer Atombindung sind wir in den vorangegangenen Einheiten davon ausgegangen, dass jeder Partner ein Elektron zur Verfügung stellt. Hier stammen aber beide Elektronen der Atombindung nur vom Stickstoff-Atom. Das Proton hat kein Elektron zur Bindung beigetragen.
Ein freiwilliger Versuch. Ihr benötigt dazu:
- Zitrone(nsaft)
- Bullrichsalz (Tabletten oder Pulver), falls nicht verfügbar ist auch Backpulver möglich.
- 2 kleine Gläschen (z.B. Schnapsgläser)
Durchführung:
- Füllt die zwei Schnapsgläser zur Hälfte mit Leitungswasser. In ein Glas gebt ihr eine Tablette Bullrich-Salz (oder einen halben Teelöffel Pulver oder einen halben Teelöffel Backpulver.
- Anschließend tropft ihr in beide Gläschen die gleiche Menge Zitronensaft (ich habe es mit jeweils 50 Tropfen Z.-Saft ausprobiert) und rührt ca. 1 Minute lang um.
- Probiert von jeder Lösung einen Teelöffel voll (Ihr könnt das noch einmal wiederholen, dann aber bitte keine größeren Mengen mehr von der Backpulver-Lsg. schlucken. Backpulver kann im Magen zur Bildung großer Mengen Gas führen.
Beschreibt das Ergebnis in Form eurer Geschmacks-Empfindung
Die Lösung mit Bullrich-Salz / Backpulver sollte deutlich weniger sauer schmecken. Es kommt aber ein bisschen auf die Zitrone an. Die muss sehr sauer sein, damit der Versuch gut klappt.
Nur kurz zur Erklärung: Bullrichsalz enthält Natriumhydrogencarbonat. In Wasser gelöst entstehen Hydrogencarbonat-Ionen. Diese sind in der Lage Protonen aufzunehmen. Sie fungieren also als Base.
Die sauere Wirkung von Zitronensaft beruht auf der Zitronensäure, die ein (bzw. auch mehrere) Proton(en) abgeben kann. Nachdem diese jedoch von den Hydrogencarbonat-Ionen "abgefangen" werden, entsteht auf der Zunge kein sauerer Eindruck.
Formuliert die Aufnahme eines Protons auf Teilchen-Ebene von folgenden Basen:
- Hydrogencarbonat-Ion
- Sulfid-Ion
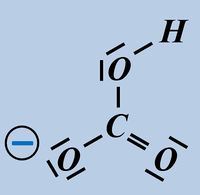
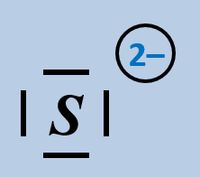
Bitte wirklich erst auf "Lösung" klicken, wenn ihr diesen chemischen Vorgang auf ein Stück Papier gezeichnet habt!
Hast Du wirklich die Lösung schon gezeichnet?
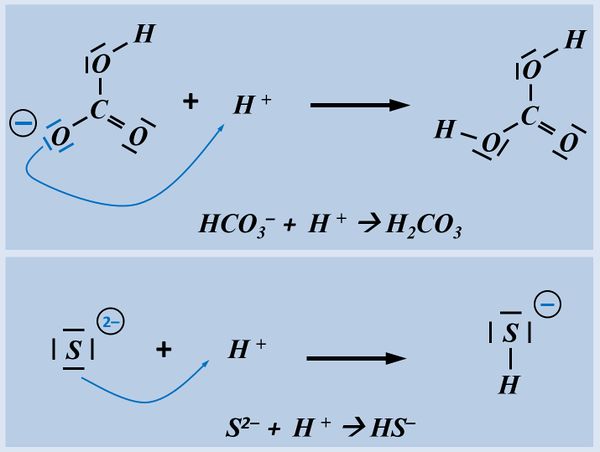
Beim Hydrogencarbonat-Ion könnte es sein, dass ihr ein anderes freies Elektronenpaar für die Bindung zum Proton verwendet habt. Das ist aber falsch! Das Proton wird immer über eines der drei freie Elektronenpaare gebunden, die am Sauerstoff mit der negativen Ladung sitzen (im Bild blau markiert). Schon allein aufgrund der elektrischen Ladung dort, wird das positiv geladene Proton dort hin gezogen.
Beim Sulfid-Ion ist egal, welches Elektronenpaar verwendet wird, das Ergebnis ist faktisch immer das selbe.




